作者简介: 刘丛丛, 女, 1987年生, 广东省药品检验所主管药师 e-mail: 1563561472@qq.com
疫苗中铝佐剂含量是影响疫苗有效性和安全性的重要因素, 如何快速、 准确测定疫苗制品中的铝含量是生产企业、 检验机构的迫切需求。 采用双曲面弯晶的单色聚焦技术, 以基本参数法校正基体效应, 采用30%硝酸溶液、 40 ℃加热25 min对疫苗制品进行预处理, 厚度为4 μm的聚丙烯薄膜为封底材料, 在低电压、 高电流的激发条件下探测300 s, 建立了快速测定疫苗中铝含量的分析方法。 结果显示, 6个不同种类的疫苗基质中铝元素测量值和理论值呈显著正相关关系, 拟合方程相关系数均大于0.998, 方法检测限和定量限分别为0.027和0.090 mg·mL-1。 在0.3~0.7 mg·mL-1加标水平内, 平均回收率为97.6%~102%, 精密度RSD( n=6)为2.4%~6.7%。 90天内同一样品的测定结果变异系数为4.7%。 以ICP-OES、 ICP-MS为参比进行准确度验证, 6个品种70批疫苗制品与参考值具有较好的一致性, 相对误差绝对值不超过10%, 可实现现场检测, 无需依赖大型设备仍可获得准确结果。 研究表明, 采用单色聚焦-能量色散X射线荧光光谱法, 具有无需标准物质、 准确度高、 精密度佳、 检测限低的优点, 可用于现场快速测定疫苗制品中铝佐剂含量, 具有广泛的实际推广意义。
The aluminum adjuvant content in vaccines is an important factor affecting the effectiveness and safety of vaccines. Determining the aluminum content in vaccines swiftly and accurately is an urgent requirement for both production enterprises and inspection institutions. In this paper, the monochromatic excitation technology of a doubly curved crystal was applied to energy dispersive X-ray fluorescence spectrometry, and the matrix effect was corrected by the fundamental parameter method. Samples were pretreated by heating in 30% nitric acid solution at 40 ℃ for 25 minutes. A polypropylene film with a thickness of 4 μm was used as the backing material. Detection was carried out for 300 seconds under the excitation conditions of low voltage and high current, and an analytical method for rapidly determining the aluminum content in vaccines was established. The results showed a significant positive correlation between the measured and theoretical values of aluminum in six vaccine matrices. The correlation coefficients of the fitting equations were all greater than 0.998. The detection limit and quantification limit of the method were 0.027 and 0.090 mg·mL-1, respectively. Within spiking levels ranging from 0.3 to 0.7 mg·mL-1, average recovery rates fell between 97.6% and 102%, with precision RSD ( n=6) recorded at 2.4% to 6.7%. The coefficient of variation for the same sample measured within 90 days was 4.7%. The accuracy was verified with ICP-OES and ICP-MS as references. The results of 70 batches of vaccine products of six varieties showed good consistency with the reference values, and the absolute values of relative errors did not exceed 10%. This method enables on-site testing without reliance on precision equipment while maintaining accuracy. The research indicates that using monochromatic excitation-energy dispersive X-ray fluorescence spectroscopy offers several advantages, including eliminating the need for standard materials, high accuracy, good precision, and a low detection limit. This technique is suitable for rapid on-site determination of aluminum content in vaccines and holds broad practical significance for widespread application.
铝佐剂是目前人类疫苗中应用最为广泛的佐剂, 其中铝含量对疫苗的免疫原性及安全性的影响最为显著[1]。 一方面, 铝佐剂通过储存库效应与免疫刺激效应等机制增强疫苗诱导免疫反应的能力, 起到正向的辅助作用[1]。 另一方面, 铝在人体中可诱导过敏反应并具有神经毒性, 包括疼痛、 硬结、 肿胀等局部不良反应以及导致神经系统损害、 引发巨噬细胞肌筋膜炎等潜在的不安全因素[2]。 因此, 疫苗中铝佐剂的用量需兼顾佐剂的辅助作用及安全隐患。 目前, 全球已上市的疫苗铝佐剂多为0.3~0.5 mg/剂[3], 如何快速、 准确测定疫苗中铝含量是生产企业、 检验机构的实际需求。
目前, 疫苗中铝含量的测定主要有络合滴定法[4]、 紫外分光光度法[5]、 ICP-OES法[6]、 ICP-MS法[3]等, 这些方法都存在样品消耗量大、 分析速度慢等缺点[3]。 能量色散型X射线荧光光谱(ED-XRF)不需要分光晶体精密运动装置和光源冷却装置, 结构简单, 对样品制备要求不高, 易于开发便携式设备[7, 8], 是元素现场快速测定的重要技术手段之一。 然而, 低原子序数元素的荧光产额低, 特征X射线信号弱, 易被初级辐射连续谱的康普顿散射背景淹没[9], 采用传统的ED-XRF分析微量、 痕量的轻元素(原子序数小于20的元素)比较困难[10]。 单色聚焦-能量色散X射线荧光光谱技术(MED-XRF)采用双曲面弯晶(DCC)光学晶体, 将来自光源的连续X射线聚焦并衍射为单色光, 一方面有效提高待测元素的激发效率, 另一方面, 单色化使韧致辐射产生的散射背景大幅降低, 进而使荧光光谱的连续散射背景极大地降低, 大幅提升检测峰背比和灵敏度[11, 12, 13]。 同时, 配合能量分辨率良好的高性能硅漂移探测器SDD, 可将元素分析范围延伸至轻元素甚至超轻元素(原子序数小于11的元素)。 本文基于MED-XRF, 首次建立了人用疫苗中微量铝含量的快速测定方法, 讨论了非均相液体样品的制备和测试条件, 并与ICP-MS、 ICP-OES等方法进行结果比对。
E-lite便携式X射线荧光光谱仪(苏州佳谱科技有限公司, 中国), 激发源为X射线管, 靶材为Cr, 工作电压25 kV, 工作电流0.4 mA, 优化后测试时间为300 s。
ICAP PRO X DUO电感耦合等离子体发射光谱仪(Thermo Fisher公司, 美国); ICAP RQ电感耦合等离子体质谱仪(Thermo Fisher公司, 美国)。
铝标准溶液(国家钢铁材料测试中心钢铁研究总院, 批号: 22033135, 浓度: 1 000 μ g· mL-1; 介质: 10%HNO3), 钪标准溶液(国家钢铁材料测试中心, 批号: 22070435, 浓度: 1 000 μ g· mL-1; 介质: 10%HNO3), 硝酸(优级纯, 广州化学试剂厂); 磷酸(分析纯, 广州化学试剂厂); 盐酸(分析纯, 广州化学试剂厂); 纯水(Milli-Q 制备); 聚丙烯薄膜(4 μ m、 12 μ m, 美国Chemplex公司); 疫苗样品来源于国内5家疫苗生产企业, 包括17批次新型冠状病毒灭活疫苗(Vero细胞)、 14批次重组戊型肝炎疫苗(大肠埃希菌)、 12批次双价人乳头瘤病毒疫苗(大肠杆菌)、 16批次重组乙型肝炎疫苗(酿酒酵母)、 3批次吸附无细胞百白破联合疫苗、 8批次流感病毒裂解疫苗。
1.3.1 标准工作溶液的配制
分别精密量取1 000 μ g· mL-1铝标准溶液0.25、 0.5、 1.0、 1.5、 2.0 mL于5 mL容量瓶中, 用阴性疫苗基质(流感病毒裂解疫苗)溶液稀释并定容至刻度, 配制成含铝浓度为50、 100、 200、 300和400 μ g· mL-1的系列标准工作溶液。
1.3.2 基本参数法及工作曲线
按照MED-XRF设定的参数, 对标准工作溶液进行测定。 根据基本参数法对光管的原始谱、 探测器的探测效率进行理论数据拟合(包括元素拟合、 荧光产额、 康普顿和瑞利散射、 逃逸峰、 叠加峰、 质量吸收系数等参数), 再通过少量的标准工作溶液对理论参数进行迭代处理, 直到测量含量和标准含量线性回归方程接近y=x。 绘制标准曲线, 并将标准曲线内置到XRF测量软件中, 用于实际样品检测。
1.3.3 样品制备
取预混的疫苗样品1.0 mL于离心管中, 加入1.0 mL 30%硝酸溶液, 涡旋混匀, 于40 ℃水浴25 min, 取出冷却至室温, 作为待测样品溶液。 待测样品溶液从套装样品杯硅胶阀处装入样品杯, 放入仪器测量, 获得X射线荧光强度, 通过内置的标准曲线计算得到样品中铝含量。
1.3.4 ICP-OES法与ICP-MS法
精密量取铝标准溶液适量, 用0.1 mol· L-1盐酸溶液逐级稀释配制为1~20 μ g· mL-1浓度的系列标准溶液。 精密量取0.2 mL疫苗试样置于塑料离心管中, 加入0.2 mL 5 mol· L-1盐酸溶液, 室温下放置0.5 h, 待试样完全溶解至溶液澄清后, 加水至10 mL, 即得待测样品溶液。 系列标准溶液和待测样品溶液经ICP-OES测定, 通过标准曲线计算样品中铝含量。
精密量取铝标准溶液适量, 用5%硝酸溶液逐级稀释配制为2.5~80 ng· mL-1浓度的系列标准溶液。 用5%硝酸溶液配制的50 ng· mL-1钪单元素标准溶液, 作为内标溶液。 精密量取0.05 mL疫苗试样置于塑料离心管中, 加入5 mL硝酸, 涡旋混匀, 室温下放置0.5 h, 再取0.05 mL上述溶液用5%硝酸稀释至10 mL, 即得待测样品溶液。 系列标准溶液和待测样品溶液经ICP-MS采用内标法测定, 通过标准曲线计算样品中铝含量。
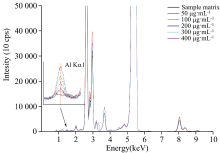
靶材的原子序数越大, X光管压越高, 连续谱强度越大。 因此, 对于轻元素的分析, 通常使用原子序数较小的铬靶。 疫苗样品为液体基质, 由轻基体组成, 辐射的穿透深度可能超过样品的厚度。 为满足液体样品测量的无限厚要求, 一般选择元素的低能辐射作为分析线, 并在低电压(25 kV)下操作[14]。 铝属于第三周期元素, 光谱简单, 谱线数量少, 选取强度较高的Kα 1特征谱线, 其光子能量为1.49keV[14]。 空白样品和样品加标溶液XRF典型图谱见图1。
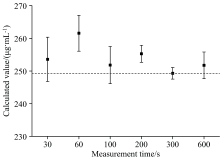
2.2.1 测试时间的选择
由于MED-XRF的测量时间与样品的测试计数率之间并非存在线性关系, 不同的测试时间对结果的稳定性和准确性有较显著的影响。 本研究考察了测试时间为30、 60、 100、 200、 300和600 s时, 浓度为250 μ g· mL-1的铝标准溶液6次平行检测结果的重复性, 结果见图2。 结果表明, 当测试时间为30~100 s时, 测量结果RSD较大, 重复性较差; 测试时间大于100 s后, 测量结果与实际理论值接近, 各次测量结果分布集中, 重现性较好, 且200、 300和600 s的测定结果无显著差异。 兼顾检验准确度和检验效率, 本研究的测试时间为300 s。
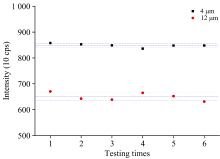
2.2.2 封底薄膜厚度
铝为低原子序数元素, 其K系平均荧光产额只有0.026, 荧光强度低[14], 薄膜的厚度直接影响辐射的透过率。 本研究以浓度为400 μ g· mL-1的标准溶液, 比较了不同膜厚的聚丙烯膜对铝特征荧光谱线强度的影响。 如图3所示, 厚度为12 μ m的薄膜对铝元素分析线的信号强度有显著影响, 测量重复性较差。 为提高分析线的强度, 兼顾防漏能力, 本研究以4 μ m聚丙烯膜为封底材料。
微-痕量轻元素的定量分析是EDXRF分析中最薄弱的方面, 受基体的影响显著[15]。 本研究以基本参数法校正基体吸收-增强效应, 主要包括元素拟合、 荧光产额、 背景拟合、 逃逸峰、 叠加峰、 质量吸收系数等参数。 尽管本研究采用的单色聚焦X射线荧光光谱通过DCC分光、 聚焦后大幅降低了散射背景, 但仍不能获得一条固定波长的谱线, 而是具有一定光谱宽度的谱带; 另外, 样品自身的散射也不容忽视, 因此背景拟合至关重要。 本研究采用康普顿散射和瑞利散射两种散射模型进行的拟合, 准确扣除元素峰的背景信号, 提高信噪比。
本文以重组乙型肝炎疫苗(酿酒酵母)(rHB Vac. (S.c.))、 重组戊型肝炎疫苗(大肠埃希菌)(rHE Vac. (E. coli))、 双价人乳头瘤病毒疫苗(大肠杆菌)(2vHPV Vac. (E. coli))、 新型冠状病毒灭活疫苗(Vero细胞)(ICV (Vero))、 吸附无细胞百白破联合疫苗(DTaP)、 流感病毒裂解疫苗(IIV)为典型代表评价基本参数法对不同疫苗基质的校正效果。 疫苗样品按“ 1.3.3” 处理, 通过稀释或加标配制成铝浓度为0、 50、 100、 200、 300和400 μ g· mL-1的系列标准工作溶液。 铝的理论数据与实际数据的比较结果见图4和表1。 从结果可知, 当铝含量在0~400 μ g· mL-1范围内, 不同疫苗基质中铝含量的实际值和测量值拟合方程线性关系良好, 相关系数r的范围为0.998 2~0.999 9, 回归方程的斜率范围为0.990 5~1.012 4, 数据点基本集中在y=x线上, 不同疫苗基质的均方根误差均小于7 μ g· mL-1, 各测量值的相对误差均小于6%, 测量准确度较高, 说明根据基本参数法拟合的定量模型能有效校正基体吸收-增强效应, 在不同类型的疫苗样品中具有较好的通用性。
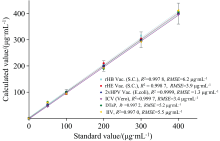 | 图4 不同疫苗基质中铝的标准值与回归计算值相关曲线Fig.4 Calculated value versus standard value of Aluminum in different vaccines |
| 表1 不同疫苗基质中铝含量的测量准确度 Table 1 The goodness of fit of measurement results of the Aluminum content in different vaccines |
2.4.1 预处理试剂的选择
疫苗制品常为非均匀态的悬浊液, 其中铝佐剂通常与抗原吸附结合, 主要通过静电力、 疏水作用及配基交换等方式来实现, 在疫苗中以沉淀形式存在[16]。 对于非均相样品, 其颗粒度及化学组成的不均匀都会发生偏析, 导致样品发射的特征X射线强度的严重偏差, 直接影响分析线的测量强度与浓度的定量关系, 用数学校正的方法难以消除这种影响[14], 有必要对样品进行适当的处理。
本文比较了以水、 硝酸、 磷酸、 盐酸对样品进行预处理的效果。 水作为预处理试剂时, 只对疫苗样品起分散、 稀释的作用, 并未破坏铝佐剂与抗原的吸附, 样品处理液仍呈悬浊态, 导致测量结果显著偏低。 磷酸为《中国药典》三部中铝含量测定选用的预处理试剂, 对于不同吸附类型的疫苗, 磷酸处理方法在酸的浓度、 预处理时间、 预处理温度等方面有较大差异, 且个别品种需要通过煮沸来实现对铝的解吸附, 实验条件较为苛刻。 盐酸作为预处理试剂, 在ICP-OES检测中较为常用, 但在MED-XRF测试中发现, 经盐酸溶液预处理的样品铝含量偏高, 这主要是因为与水和硝酸相比, 盐酸对初级辐射的散射强度差异非常显著[14], 导致分析背景远超数学校正的范围。 采用硝酸作为预处理试剂时, 背景干扰小, 在40 ℃预处理25 min后, 即可实现样品中铝佐剂与抗原充分解离, 样品处理液均匀澄清, 且试验条件温和, 因此本文以硝酸作为预处理试剂。
2.4.2 预处理条件的优化
对疫苗样品的预处理, 硝酸浓度、 反应时间和反应温度是影响试验结果的因素, 可通过正交试验法得到最优的试验结果。 为给正交试验提供一个合理的数据范围, 本文对主要因素硝酸浓度进行单因素试验, 比较了硝酸浓度为2%、 5%、 10%、 20%、 30%、 50%、 80%、 100%对实际样品(重组乙型肝炎疫苗(酿酒酵母), 参考值为0.45 mg· mL-1)测定的影响。 由表2可知, 随硝酸浓度增大, 检测结果及RSD均呈下降趋势, 当硝酸浓度为20%、 30%和50%时, 相对误差绝对值均小于5%, RSD均不大于2%, 测量准确度和精密度较好。
| 表2 硝酸浓度对铝含量测定的影响 Table 2 The influence of HNO3 concentration on the quantitative determination of Aluminum |
在单因素实验的基础上, 以硝酸浓度、 反应时间和反应温度为因素, 设计了3因素3水平正交试验L9(34), 以准确度为评价指标, 优化预处理条件。 试验因素、 水平和结果见表3。 通过直观分析结果可以看出, 硝酸浓度对结果的影响最大, 硝酸浓度为30%, 40 ℃处理25 min是较好的预处理条件。
| 表3 正交实验方案及直观分析表 Table 3 Orthogonal test plan and visual analysis |
2.5.1 检测限和定量限
XRF测量值属于泊松分布, 检出限计算方法和分析领域中常用的计算方法不同。 一般来说, 常用的检出限计算方法有两种, 分别为峰背景计数法和重复测定法[17]。 对于轻元素, 峰背景计数法受样品基体与谱线重叠干扰等影响, 计算的方法检出限和实际检出限有效大差别[18]。 本文采用重复测定法确定方法检测限和定量限, 即在相同实验条件下重复测定低含量样品溶液11次, 以测定值的3倍标准偏差作为检测限, 10倍标准偏差作为定量限, 结果见表4。
| 表4 方法检测限、 定量限、 回收率和重复性 Table 4 Limit of detection, limit of quantitation, recoveries and precisions |
2.5.2 回收率和重复性
对不含铝佐剂的疫苗样品在0.3、 0.5和0.7 mg· mL-1三个水平进行加标回收试验, 各水平制样6份, 结果见表4。 结果表明, 在加标水平内, 平均回收率为97.6%~102%, 精密度RSD(n=6)为2.4%~6.7%, 回收率和重复性良好。
2.5.3 日间精密度
MED-XRF定量采用无标物分析法, 仪器测量的稳定性对结果非常重要。 本文在90天内对实际样品(重组戊型肝炎疫苗(大肠埃希菌), 参考值为0.54 mg· mL-1)进行多次测量, 结果见表5。 结果表明, 90天内对同一样品多次测量的变异系数为4.7%, 数据集中, 方法稳定可靠。
| 表5 方法日间精密度 Table 5 Intra-day precision of this method |
对ICP-OES、 ICP-MS两法的测定结果进行显著性检验(t检验法), 取两者结果不存在显著性差异的样品(t0.1, 4< 2.13)为代表, 两法结果的平均值作为参考值, 考察MED-XRF法的准确度。 结果表明, MED-XRF法对6个品种70批疫苗的测定结果与参考值具有较好的一致性, 相对误差绝对值均不超过10%, 上四分位数、 中位数和下四分位数分别为2.3%、 4.8%和7.6%, 满足不同疫苗中铝含量快速定量分析的要求。
采用ED-XRF测定铝含量的研究主要集中在冶金[19]、 地质[20]等领域, 对样品中微量铝的定量测定研究较少。 苏莹等[7]采用便携式X射线荧光光谱仪快速筛查粉丝中硫酸铝钾(限量值为200 mg· kg-1), 与本研究水平相当。 本文系统地研究了非均相液体样品的制备和测试条件, 采用双曲面弯晶的单色聚焦技术, 以基本参数法校正基体效应, 解决了能量色散型X射线荧光光谱技术对铝元素检测灵敏度低的问题。 结果显示, 不同种类的疫苗基质中铝元素测量值和理论值呈显著正相关关系, 拟合方程相关系数均大于0.998, 检测限和定量限分别为0.027和0.090 mg· mL-1。 在0.3~0.7 mg· mL-1加标水平内, 平均回收率为97.6%~102%, 精密度RSD(n=6)为2.4%~6.7%。 同一样品90天内的日间精密度为4.7%。 与经典光谱法相比, 相对误差绝对值不大于10%, 满足现场快速测定疫苗制品中铝含量的技术要求, 具有制样简单、 分析速度快、 结果可靠等优点。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|