作者简介: 曹 雪, 1992年生,北京理工大学化学与化工学院物理化学研究所博士研究生 e-mail: xuecao_bit@foxmail.com
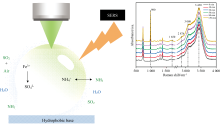
细颗粒物(PM2.5)污染主要由人类活动产生的微米、 亚微米气溶胶颗粒或者微液滴, 但其形成机制尚不清楚, 而缺少相应的有效解决办法。 要实现对我国城市PM2.5污染的精准防控, 取决于我们对二次气溶胶形成机理的深入认识。 当前存在的瓶颈和难点在于气溶胶及其前驱物的关键理化参数(如摄取系数)仍然无法实现准确测量。 这将极大地限制了我们对二次气溶胶的形成、 快速长大、 碰撞重组等演变规律的认识。 因此, 为了认清大气颗粒物形成机制, 必须实现对细颗粒物演变过程中的关键理化参数进行精确测量。 硫酸盐是我国大气PM2.5重要组成部分, 但现有化学模型普遍低估了PM2.5霾污染事件中硫酸盐的浓度, 有关SO2在气溶胶液滴中的表面氧化过程、 液滴中过渡金属离子(TMI)催化过程等还有很多不清楚的地方, 表明我们对大气中SO2的转化机制仍存在认识不足。 获得硫酸盐二次转化动力学数据, 确定二次无机气溶胶的快速长大机制, 准确测量大气中痕量气体在颗粒物表面的摄取反应速率是定量分析大气非均相反应的关键参数。 利用激光共焦显微拉曼光谱仪测量氯化铵液滴中Fe(Ⅲ)催化SO2氧化动力学过程, 根据$SO_{4}^{2-}$的自发拉曼光谱信号随时间的变化, 建立了SO2与单液滴进行非均相反应摄取系数的精确测量方法, 研究了外场条件下痕量SO2气体与单液滴之间的反应动力学过程。 该方法验证了表面动力学过程, 并测定了反应摄取系数。
Fine particulate matter (PM2.5) pollution was mainly caused by micron and submicron aerosol particles or micro-droplets generated by human activities. Still, the formation mechanism remains unclear, and corresponding effective solutions are lacking. The precise prevention and control of urban PM2.5 pollution in China depends on our in-depth understanding of the formation mechanism of secondary aerosols. The current bottleneck and difficulty lie in the fact that aerosols' key physicochemical parameters (such as uptake coefficients) and their precursors still cannot be accurately measured. This will greatly limit our understanding of the evolution laws, such as the formation, rapid growth, and collision recombination of secondary aerosols. Therefore, to understand the formation mechanism of atmospheric particulate matter, it is necessary to accurately measure the key physicochemical parameters in the evolution process of fine particulate matter. Sulfate was an important component of PM2.5 in the atmosphere of China. However, the current chemical models underestimate the sulfate concentration in PM2.5 haze pollution events. There were still many uncertainties regarding the surface oxidation process of SO2 in aerosol droplets and the catalytic process of transition metal ions(TMI) in droplets, indicating that our understanding of the transformation mechanism of SO2 in the atmosphere was still insufficient. Obtaining the kinetic data of sulfate secondary transformation, determining the rapid growth mechanism of secondary inorganic aerosols, and accurately determining the uptake reaction rate of trace gases in the atmosphere on the surface of particulate matter were the key parameters for quantitative analysis of atmospheric heterogeneous reactions. This study employed a laser confocal micro-Raman spectrometer to measure the kinetics of SO2 oxidation catalyzed by Fe(Ⅲ) in ammonium chloride droplets. Based on the temporal variation of the spontaneous Raman signal of $SO_{4}^{2-}$, we established an accurate method for measuring the uptake coefficient of SO2 in heterogeneous reactions with a single droplet. We investigated the reaction kinetics between trace SO2 gas and a single droplet under external field conditions. This method validated the surface kinetic processes, and determined the reaction uptake coefficient.
PM2.5污染给我国社会经济和公众健康造成了显著的负面影响, 特别是在中国华北地区冬季PM2.5霾污染事件中, 硫酸盐气溶胶的快速生成被认为是主要的化学驱动因素[1, 2, 3, 4]。 研究表明, 过渡金属离子(TMI)在气溶胶表面显著加快SO2非均相反应[4, 5, 6], 这也是PM2.5生成的主要途径之一。 人们常用的煤、 石油、 天然气等化石燃料在燃烧过程中释放大量SO2, 为硫酸盐的生成提供大量的前体物质[7]。 尽管已有多项研究关注大气中硫酸盐的生成过程, 但是由于具体生成机理尚不明晰, 加之关键动力学参数的缺失, 导致大气模型在霾污染事件期间对硫酸盐的浓度被严重低估。
已知的硫酸盐生成途径主要包括: SO2在气相中被羟基自由基(OH)氧化; 在液相中被臭氧(O3)[8]、 过氧化氢(H2O2)[9]、 氧气(O2与过渡金属离子相结合)[10]以及有机物[11]等的氧化。 近期的研究进一步指出, 在气溶胶表面发生的过渡金属离子(TMI)催化的非均相氧化反应显著加快SO2氧化[2, 4]。 最近, Wang[2]和Song[4]等, 通过实验室研究及外场观测和模型模拟对华北地区雾霾污染硫酸盐形成过程及机制研究结果表明, Mn2+引导的界面非均相催化反应主导了华北地区雾霾污染硫酸盐的大量生成, 该机制贡献了约92.5%的硫酸盐产生。 Angle等[12]近期研究表明, 微液滴中TMI催化的S(IV)氧化速率明显高于体相溶液中的反应, 这一现象可能与气-液界面的速率增强效应有关, 然而目前尚不清楚当反应发生在气溶胶表面时, Fe(Ⅲ )离子催化反应机理[12]。
评估大气中非均相反应与气相反应的相对重要性并模拟非均相反应对气象物种转化、 大气氧化能力及颗粒物吸湿性等的影响, 需要确定其相关的反应速率。 然而, 计算痕量气体在颗粒物表面被摄取的大气化学非均相反应速率(k)需要考虑以下几个因素: 大气颗粒物的表面积(A), 大气颗粒物的体积(V), 气体分子的平均运动速率(Γ )。 其中, 大气颗粒物的表面积和体积可由外场观测和基本物理化学参数进行计算, 而摄取系数则需要由实验室模拟测定。 痕量气体的摄取系数是指非均相反应中痕量气体被颗粒物表面摄取的概率, 因此它是衡量大气颗粒物反应能力的重要量化指标。 然而, 由于不同的测量方法以及测量过程的差异, 摄取系数在不同情况下有不同的意义; 再加上非均相反应的复杂性, 使其测定过程中存在着很多不确定性。
$X \xrightarrow{\text { 大气化学非均相反应速率, } k} Y$ (1)
本研究中, 利用自发拉曼光谱测量了氯化铵与Fe(Ⅲ )混合种子单液滴与痕量气体SO2动力学过程, 实现了对反应液滴中SO2氧化产物
本文使用的激光共焦显微拉曼光谱仪型号为Renishaw inVia Raman(产地: 英国雷尼绍)(图2), 是一种结合了激光共聚焦显微镜和拉曼光谱仪的先进分析仪器。 该仪器利用激光光源激发样品表面的振动模式, 样品发生拉曼散射, 通过收集拉曼散射光谱来获取样品的信息。 显微共焦拉曼光谱仪以其高灵敏度、 高分辨率和非破坏性的特点而受到广泛应用[13]。 主要的参数指标: 514 nm激光器, 光谱分辨率1 cm-1, 1 800 g· mm-1可转光栅, × 5, × 20, × 50倍物镜, 最小光斑直径为1 μm。
本研究所用的样品池为亚克力材质, 透光率在92%以上, 具有良好的耐腐蚀性和化学稳定性。 样品池底部铺有PTFE(聚四氟乙烯)疏水基底, 液滴在疏水基底表面呈规则球形。 样品池配有进气口和出气口, 进气口用于将干湿载气和反应气送入样品池内部, 出气口连接湿度计/温度计(Center 313), 实现尾气湿度和温度的监测。 为了控制液滴环境氛围, 实验中使用流量计(Alicat 1 L· min-1)控制干湿气的流速比进而控制样品池中的相对湿度(RH)。 实验需要外加反应气时, 如SO2、 NH3等, 需将干气流速减去相应的反应气流速, 从而保持总的干湿气流量的平衡, 以确保湿度一致。 实验过程中, 采用一次性注射器将配置好的1 mol· L-1的NH4Cl溶液喷射到下层疏水基底上, 形成大量的微米级液滴, 随后将样品池密封并连入干湿气和反应气。
配置一系列不同摩尔比的氯化铵/硫酸铵(NH4Cl/(NH4)2SO4)混合溶液, 如表1所示。 不同浓度配比下的NH4Cl/(NH4)2SO4液滴, 在气溶胶含水量与环境湿度达到动态平衡后, 使用E-AIM Model(Ⅲ )按照以下步骤测定液滴内部的实际硫酸盐的浓度。 在不考虑额外的其他微量气体(NH3)的影响, 在给定的湿度条件下吸失水达到动态平衡。 我们可以测定在此湿度下的过饱和NH4Cl/(NH4)2SO4液滴的体积(V), 以及此湿度下液滴内水的质量(
| 表1 作标线溶液的摩尔比以及相对应液滴在RH=80%时的 |
实验所使用条件为: 拉曼激光功率为100 mW(衰减至10%), 积分时长10 s, 累积1次, 拉曼信号采谱范围为100~4 000 cm-1, SO2=1 ppm, NH3=8 ppm, NH4Cl: Fe3+摩尔比为500∶ 1。
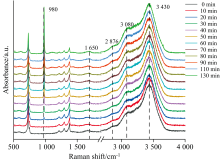
图3是我们测量了在不同反应时间内液滴中Fe3+催化氧化SO2的拉曼光谱图(液滴半径r约为20 μm)。 在0 min时刻, 测量液滴的拉曼光谱信号主要是来自NH4Cl和H2O的特征拉曼峰信号。 其中, 1 650和3 430 cm-1处分别为H2O的弯曲、 伸缩振动峰; 在1 300~1 400 cm-1范围内的三个相邻峰则来自液滴底部疏水基底PTFE薄膜信号; 2 876和3 080 cm-1处为
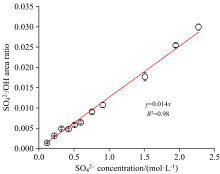 | 图4 根据表1测量的NH4Cl/(NH4)2SO4液滴中 |
随后, 将液滴
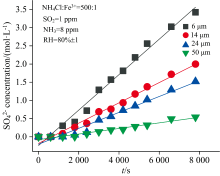
我们在实验中选取不同半径的液滴通入相同的反应气进行反应考察液滴半径对反应过程的影响。 图5是不同半径液滴在反应时间分别为130 min过程中硫酸盐浓度变化的情况。 从图5中可以看到, 当液滴半径从6 μm增加至50 μm时, 液滴中的
我们建立了一个利用拉曼光谱判定过渡金属离子催化的SO2在单液滴中进行非均相氧化反应的方法。 利用物质的量计算公式计算反应过程中液滴内硫酸盐的生成速率。 具体计算过程如下:
假设SO2在Fe(Ⅲ )催化下的氧化反应是表界面反应过程, 则液滴的反应速率dn/dt(mol· s-1)与液滴的表面积成正比。 考虑到硫酸盐生成过程中, 液滴半径变化保持恒定(硫酸铵生成量与种子液滴中氯化铵的量相比可以忽略), 反应仅涉及硫酸根浓度的变化。 在某一恒定湿度条件下, 硫酸铵液滴其中所含的硫酸盐溶质的物质的量n (mol)可由式(4)计算
式(4)中, c(mol)是硫酸铵液滴在某一湿度下的平衡浓度, 可通过E-AIM Model(Ⅲ )模型得到; V(L)为单液滴的体积。 SO2在液滴表面的氧化速率由硫酸盐的生成量推演而来, 即
式(5)中,
其中,
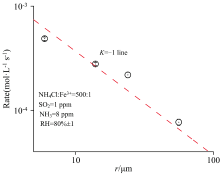
K在式中代表比例系数。 图6中的线性关系表明, 液滴的反应速率(mol· L-1· s-1)正比于液滴半径倒数(1/r), 进一步说明液滴的反应速率与液滴的表面积成正比。 这一现象证明了液滴中Fe3+催化的SO2氧化是一个发生在液滴表面的过程。
基于以上结论Fe(Ⅲ )催化氧化SO2的反应发生在微液滴表面, 根据气体SO2反应摄取系数(
式(10)和式(11)中, Z为SO2分子与液滴的碰撞效率(mol· s-1); 参数R为气体常数(J· mol-1· K-1)、 T为温度(K-1)、
| 表2 拉曼测量不同半径液滴的反应摄取系数 Table 2 Raman measurement of reaction uptake coefficients for droplets of different radii |
表3比较了本研究获得的动力学数据与文献中报道的数据。 根据本实验拉曼光谱的研究, Fe(Ⅲ )催化的SO2氧化主要发生在气溶胶的表面。 在室温和pH~5的条件下, 反应摄取系数
| 表3 室温下SO2非均相氧化动力学 Table 3 Kinetics of heterogeneous SO2 oxidation at room temperature |
我国PM2.5霾污染事件中, 硫酸盐反应速率的快速增加可能源于城市气溶胶中SO2的非均相转化, 这与体相溶液中的S(Ⅳ )氧化有很大不同。 我们使用激光共焦显微拉曼光谱仪直接测量了单液滴中Fe(Ⅲ )催化氧化SO2动力学, 实时原位测量了液滴内
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|