作者简介: 马嘉昊, 1999年生,四川轻化工大学物理与电子工程学院硕士研究生 e-mail: 322085420113@stu.suse.edu.cn
能量色散X射线荧光法(EDXRF)检测大豆中重金属Cd时, 存在大豆组成复杂、 标准样品获取困难和制作成本高等问题。 根据大豆蛋白中巯基可以络合Cd2+的特性, 提出了一种基于标准加入法的固-液混合制样方法, 并结合强度校正模式进行基体校正, 以提高EDXRF检测大豆中Cd的准确性和可靠性。 首先, 通过单因素实验, 优化了可能影响大豆中Cd元素激发效果的7个条件参数。 优化后的实验条件为: 管电压70 kV、 管电流700 μA、 检测时间1 200 s、 样品质量12.00 g、 样品目数≥100目、 压片压力25 MPa和保压时间20 s。 其次, 采用标准加入法制作了Cd加标浓度依次为0.000、 0.100、 0.200、 0.300、 0.400和0.500 mg·kg-1的大豆粉末样品。 在优化条件下, 建立了大豆中Cd的解谱面积与加标浓度之间的标准曲线方程, 该曲线线性度优秀, R2值为0.996 22。 表明大豆中Cd的荧光强度与其元素浓度之间存在显著的线性关系, 大豆对Cd2+具有较好的络合效果。 最后, 通过对比标准加入法和增量法计算的Cd含量, 发现检测结果存在偏差, 偏差来源于其他元素对Cd的吸收增强效应。 由于大豆中Sn元素含量丰富, 其他影响元素的含量较小, 主要考虑Sn对Cd的影响。 根据石墨炉原子吸收光谱法(GFAAS)对大豆中Cd含量的检测结果, 利用强度校正模式拟合得到了Cd含量的校正方程。 另取4份过100目筛的大豆样品进行检测, 在强度校正之后, 能量色散X射线荧光法对同来源样品的检测结果平均偏差由0.048 30下降至0.006 73。 为验证校正方法的普适性, 随机取10份同源大豆样品进行检测校正, 校正后平均偏差由0.035 48降低至0.010 94, 光谱仪校正前后的检测平均偏差由36.32%下降至3.31%。 所提出的固-液混合制样法操作简单, 有效克服了EDXRF在检测大豆Cd时对标准样品及高成本标准物质的依赖。 结合强度校正模式, 校正效果显著, 为大豆中重金属Cd的检测提供了一种新的有效方法。
The energy-dispersive X-ray fluorescence (EDXRF) method for detecting heavy metal Cd in soybeans faces challenges due to the complex composition of soybeans, difficulties in obtaining standard samples, and high production costs. Leveraging the sulfhydryl groups in soy protein that complex with Cd2+, we propose a mixed solid-liquid sample preparation method based on the standard addition method. This, combined with intensity correction for matrix correction, aims to improve the accuracy and reliability of EDXRF for Cd detection in soybeans. First, we optimized seven parameters affecting Cd excitation in soybeans through single-factor experiments. The optimized conditions were as follows: tube voltage of 70 kV, tube current of 700 μA, detection time of 1 200 s, sample mass of 12.00 g, sample mesh size of ≥100 mesh, tablet pressure of 25 MPa, and holding time of 20 s. Next, we prepared soybean powder samples with Cd spiked at concentrations of 0.000, 0.100, 0.200, 0.300, 0.400, and 0.500 mg·kg-1 by the standard addition method. Under the optimized conditions, a standard curve was established between the resolved spectral area and the spiked concentration of Cd in soybean. This curve exhibited excellent linearity with an R2 value of 0.996 22. This indicates a significant linear relationship between the fluorescence intensity of Cd in soybean and its elemental concentration, demonstrating that soybeans have an effective complexation effect on Cd2+. Finally, comparing the Cd content calculated by the standard addition and incremental methods revealed a deviation due to the absorption enhancement effect of other elements, particularly Sn, on Cd. Based on GFAAS results for Cd content in soybeans, a correction equation was derived using the intensity correction model. After intensity correction, the average deviation of the EDXRF method for four 100-mesh soybean samples decreased from 0.048 30 to 0.006 73. Testing ten randomly selected samples validated the universality of the calibration method, with the average deviation decreasing from 0.035 48 to 0.010 94 and the overall deviation reducing from 36.32% to 3.31%. The mixed solid-liquid sampling method proposed in this paper is simple to operate. It effectively overcomes the limitation of the lack of corresponding standard samples for EDXRF in soybean detection. Combined with the intensity correction mode, the correction effect is remarkable, providing a new and effective method for detecting cadmium (Cd) in soybeans.
随着全球人口增长和生活水平的提高, 农产品需求量持续增长。 据美国农业部2024年5月发布的《世界农产品供需预测报告》显示, 世界大豆消费量预计达到4.02亿吨, 较上一年度增加1 821万吨[1]。 中国作为全球最大的大豆消费国和进口国, 供需缺口连续多年超过9 000万吨[2]。 由于对进口的高度依赖, 自2002年以来, 中国农业部两次提出大豆振兴计划, 以提高大豆自给率。 宜宾地区作为大豆振兴战略中西南间套作区的一环, 其豆类作物在地方农业生产中占据重要地位。 当地特产如南溪豆干和豆花饭等, 不仅丰富了人们的饮食选择, 还提高了营养质量。 在如此庞大的消费需求背景下, 确保大豆的安全性, 防止其受到重金属污染, 尤其是镉污染, 已成为保障食品安全与公众健康的当务之急。 因此, 研发准确、 可靠的农产品重金属检测技术对于保障食品安全和人体健康具有重要意义。 目前, 检测大豆中重金属元素的方法主要有电感耦合等离子体质谱法(ICP-MS)和石墨炉原子吸收光谱法(GFAAS), 但这些方法均需要对样品进行消解, 使得检测周期较长。 能量色散X射线荧光检测(EDXRF)是一种快速、 无损的检测方法, 不需要对样品进行消解, 只需将其预处理为机器易于检测的形态(通常为压片), 从而保持了样品本身的完整性。 其检测时间通常小于1 h, 极大提高了检测效率。
EDXRF具有诸多优势, 但也存在局限性。 与ICP-MS和GFAAS等检测法相比, EDXRF需要一系列已知浓度的标准样品进行辅助校正, 且这些标准样品的基质应尽可能与检测样品保持一致。 Otaka等在检测大豆中的微量元素时, 采用了与大豆基质相似的8种标准物质(来源于美国国家标准与技术研究院, NIST)进行定量分析[3], 但标准物质的制作与获取成本较高。 Speranca等在检测香蕉中的Zn时, 通过人工注射七水硫酸锌来模拟基质效应[4]; Byers等在检测蔬菜中的重金属时, 将冻干欧芹与添加了金属标准液的纯水进行旋转蒸发, 制备了湿性植物标准物质来模拟原料蔬菜[5]。 Ferreira等则提出一种反相液-液微萃取(RP-LLME)的方法制备植物油样品并通过EDXRF进行金属元素测定[6]。 而对于加标过程中固液混合导致的不均匀问题, 王小龙等[7]指出, 可采取含巯基的功能化硅胶吸附重金属后与样品混合。 大豆中蛋白质含量丰富且含有巯基, Ding等[8]的研究表明, 大豆蛋白中的含巯基肽(TCPs)对Cd2+具有较高的螯合能力。 基于此特性, 本文拟探究一种结合标准加入法的固液混合方法, 制备含Cd的大豆标准样品, 并利用石墨炉原子吸收光谱法进行验证与校正。
本文针对四川省宜宾地区种植的本土大豆, 提出了一种标准加入固-液混合制样的方法, 旨在解决大豆标准样品制作与获取困难的问题。 同时, 为了减小基体效应对Cd检测结果的影响, 根据所建立的工作曲线与GFAAS的检测结果, 采用强度校正模式进行了校正。
宜宾本地大豆; Cd标准溶液100 μ g· mL-1; 蒸馏水; 医用酒精(乙醇含量95%± 5%)。
能量色散X射线荧光光谱仪CIT3000SMR(荧光靶: W, 探测器: SDD, 四川新先达测控技术有限公司); 新诺手摇压片机SYP-12B; 小型食品烘干机; 电子称(0~500 g, 精度0.01 g); 小型研磨机; 标准尼龙检验筛50目、 100目、 150目、 200目; 陶瓷研钵; 酒精灯; 石棉网; 烧杯; 玻璃棒; 移液枪10~100 μ L(误差范围: ± 1.00%)。
1.3.1 样品前处理
购得宜宾本地大豆后, 首先洗净晒干; 然后为避免重金属污染, 采用陶瓷磨芯研磨机进行粗磨, 并过50目筛网。 相比于大米, 大豆中含有更多的油脂化合物, 不易研磨成细粉。 Otaka等将大豆洗净后在-20 ℃冷冻干燥, 并用球磨机研磨至≤ 50 μ m[3]。 本文则采用边干燥边研磨的方法, 在烘干期间将烘干机温度设置为70 ℃, 并使用陶瓷研钵对大豆粉末进行持续研磨, 直至其通过100目(≤ 150 μ m)、 150目(≤ 100 μ m)、 200目(≤ 75 μ m)筛网, 以研究不同颗粒粒径对激发大豆中Cd特征射线的影响。
1.3.2 制备标准样品
目前的混合制样法主要有固-固法、 固-液法以及最常见的液-液法。 而液-液法常用于ICP-MS检测, 因其简单且稳定, 由于两相均为液体, 混合样品的均匀性好。 王小龙等[7]指出, 在固-液制样中, 标液加入催化剂样品后, 溶剂挥发导致贵金属聚集, 样品表面分布极不均匀, 影响结果的准确性和稳定性。 为解决此问题, 其使用了含巯基的功能化硅胶, 利用巯基吸附贵金属。
大豆样品中含有大量的脂肪和蛋白质, 其中的巯基对Cd2+具有较好的螯合能力。 基于此特性, 本文提出了一种利用标准加入法的大豆加标镉的流程, 此方法还可在一定程度上降低基体效应。
取过50目筛的样品粉末100.00 g, 根据GB 2762— 2017《食品中污染物限量》的规定[9], 大豆中重金属镉(Cd)的限量值如表1所示。
| 表1 GB 2762— 2017中Cd的限量值 (mg· kg-1) Table 1 Limit of Cd in GB 2762— 2017 (mg· kg-1) |
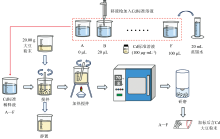
根据国家标准, 将大豆中Cd的浓度限量值分别按照0.5、 1.0、 1.5、 2.0、 2.5倍进行加标。 操作流程如图1所示, 具体步骤如下:
取空白烧杯加入20 mL蒸馏水, 利用移液枪依次向烧杯中加入0、 20、 40、 60、 80和100 μ L的Cd标准溶液(浓度: 100 μ g· mL-1)。 电子秤准确称取20.00 g样品粉末, 用玻璃棒将标液的稀释液引流入样品粉末中, 先后3次添加蒸馏水将烧杯中剩余的稀释液洗入粉末中。 加液后, 粉末样品形成浊液, 充分搅拌后均匀静置。 静置后将浊液置于酒精灯下加热以去除水分, 在加热过程中不断搅拌使浊液受热均匀。 加热至样品无明显流动性后取出, 置于烘干机中, 在70 ℃下烘干8 h直至形成固体。 将所得固体通过研磨机和研钵研磨并过筛, 形成加标样品。
1.3.3 检测条件优化
为确保大豆中Cd特征X射线的最佳激发效果, 对仪器设备的管压、 管流、 检测时间、 样品颗粒粒径、 厚度、 压片压力及保压时间进行了优化。
1.3.3.1 管压管流
Cd为重金属元素, 具有较高的原子序数和质量。 为了实现最佳的激发效果, 管电压通常需要大于待测元素激发电位的3~10倍才能获得最优激发[10]。 欧阳周璇等通过模拟发现在BaSO4荧光靶下, Cd样品在70 kV管电压下有最佳峰背比[11]。 CIT3000SMR采用钨靶, 设置50~70 kV的管电压梯度以进行验证。
取12.00 g过200目筛的样品粉末, 在20 MPa保压20 s制成压片, 将仪器管电流固定为700 μ A, 设置不同的管电压梯度进行检测, 每次检测时间为1 200 s, 检测结果如表2所示。
| 表2 管电压与荧光强度 Table 2 Tube voltage and fluorescence intensity |
取12.00 g过200目筛的样品粉末, 在20 MPa保压20 s制成压片, 将仪器管电压固定为70 kV, 设置不同的管电流梯度进行检测, 每次检测时间为1 200 s, 检测结果如表3所示。
| 表3 管电流与荧光强度 Table 3 Tube current and fluorescence intensity |
1.3.3.2 检测时间
为了获得足够的特征X射线荧光信号, 需要对样品进行较长时间的照射, 以积累足够的计数从而提高数据的准确性和可靠性。 对于大豆中含量较低的Cd元素, 由于其荧光信号较为微弱, 需要更长的检测时间以确保信号的有效捕捉。
取12.00 g过200目筛的样品粉末, 在20 MPa保压20 s制成压片。 在70 kV, 700 μ A下设置不同梯度的检测时间进行测量, 检测结果如表4所示。
| 表4 检测时间与荧光强度 Table 4 Detection time and fluorescence intensity |
1.3.3.3 样品大小
王蕾越等[12]将土样过100目筛以得到实验用基质土。 为了研究颗粒粒径的影响并防止研磨过程中可能的重金属污染问题, 本文采用陶瓷研钵和尼龙标准检验筛, 逐级研磨过50目、 100目、 150目和200目的粉末样品。
分别取10.00 g过50、 100、 150、 200目筛的样品粉末, 在20 MPa保压20 s制成压片。 在70 kV, 700 μ A下进行检测, 每次检测时间为1 200 s, 检测结果如表5所示。
| 表5 目数与荧光强度 Table 5 Meshes and fluorescence intensity |
1.3.3.4 样品质量
为了确保X射线在穿透样品时能够充分激发待测元素的特征射线荧光, 通常要求样品处于“ 无限厚” [13]。 当样品厚度足够大时, 能够激发出足够的特征X射线荧光。 然而, 样品的质量会影响压片的厚度。 考虑到压模的最大装载量为12.00 g, 为了研究样品厚度对检测效果的影响, 分别取8.00、 9.00、 10.00、 11.00和12.00 g样品粉末, 在20 MPa保压20 s制成压片。 在70 kV, 700 μ A下进行检测, 每次检测时间为1 200 s, 检测结果如表6所示。
| 表6 样品质量与荧光强度 Table 6 Weight and fluorescence intensity |
1.3.3.5 压片压力
粉末压片相较于液体或半固体样品, 其中可能存在空气缝隙, 对检测结果产生影响[14]。 压力会影响压片的密度、 均匀性和平整度, 从而影响X射线的穿透能力和荧光信号的强度。 高密度的压片可以减少X射线的散射和衰减, 但过大的压力会导致样品颗粒过度变形, 破坏原始结构, 引入误差。
为了研究压力对检测效果的影响, 分别取10.00 g过150目筛的样品粉末, 在20 MPa保压20 s制成压片。 在70 kV, 700 μ A下进行检测, 每次检测时间为1 200 s, 检测结果如表7。
| 表7 压力与荧光强度 Table 7 Pressure and fluorescence intensity |
1.3.3.6 保压时间
保压时间是影响压片质量的关键因素之一。 合适的保压时间可以确保样品颗粒在压力下充分结合, 形成稳定结构。 若保压时间过短, 样品颗粒可能未完全紧密结合, 导致压片内部存在空隙或分层, 影响激发效果。
为了研究保压时间对检测效果的影响, 分别取10.00 g过200目筛的样品粉末, 在20 MPa保压20 s制成压片。 在70 kV, 700 μ A下进行检测, 每次检测时间为1 200 s, 检测结果如表8所示。
| 表8 保压时间与荧光强度 Table 8 Pressure hold time and fluorescence intensity |
1.3.4 石墨炉原子吸收光谱法检测样品大豆
抽取部分未加标的粉末样品, 按照GFAAS方法进行检测, 以对未加标样品进行定值。 所抽取的样品为充分磨制并均匀混合后的100目大豆粉末样品。
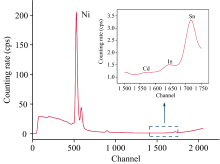
根据CIT-3000SMR检测大豆粉末压片所得光谱图如图2 所示, 道址范围为0~2 048, Cd的道址范围选择为1 540~1 606。
2.1.1 管压管流的选择
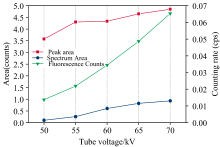
由图3可知, 当管电流固定为700 μ A时, 随着管电压的逐渐增大, Cd的净峰面积和荧光强度都明显上升。 CIT3000SMR的管电压工作范围为0~70 kV, 为了确保最佳激发效果, 选择70 kV作为工作管电压。
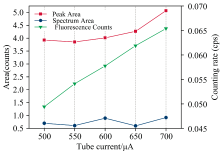
由图4可知, 当管电压固定为70 kV时, 随着管电流的逐渐增大, Cd的计数率与净峰面积明显上升。 CIT3000SMR的管电流工作范围为0~700 μ A, 为了确保最佳激发效果, 选择700 μ A作为工作管电流。
2.1.2 检测时间的选择
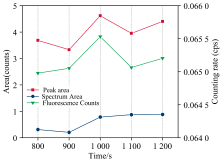
由图5可知, 当固定管电压为70 kV、 管电流为700 μ A时, 随着检测时间的增加, Cd的计数率和净峰面积总体呈上升趋势, 并且在1 000 s以后, 解谱面积趋于稳定。 为了确保最佳激发效果, 选择1 200 s作为检测时间。
2.1.3 样品质量的选择
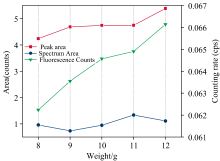
由图6可知, 随着检测样品质量的逐渐增加, 样品中的元素含量增加, 同时压片厚度增加。 在这种情况下, Cd的计数率和净峰面积受到两种因素影响: 压片中Cd元素的总含量和压片的厚度。 当试样质量不足时, X射线将直接穿透样品, 导致检测结果产生偏差[15]。 在确定管电压、 管电流和检测时间后, 当样品质量达到10.00 g时, 其荧光计数值已趋于稳定, 可以认为此时的厚度已经达到“ 无限厚” 的需求。 理论上, 随着质量的增加, Cd含量也将增加, 检测结果会更加准确。 因此, 选择12.00 g样品进行压片。
2.1.4 样品大小的选择
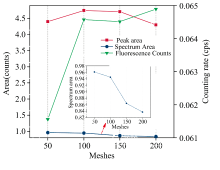
由图7可知, 当检测所用样品粉末的目数从50目增至100目时, 效果最为显著。 从100目到200目, 检测效果差异不大, 荧光计数率与净峰面积都趋于稳定。 这是因为随着样品目数的增加, 颗粒变得更小, 表面积增大, 增加了X射线与样品中Cd的相互作用机会, 从而提高了Cd的荧光产额。 更细的颗粒提高了样品的均匀性, 减少了X射线穿透样品而不与Cd作用的可能性。 然而, 随着目数的进一步增加, 解谱面积逐渐降低。 一个可能的原因是更细的颗粒导致了更多的X射线散射, 产生了背景信号, 从而降低了信噪比, 使解谱面积减小。 综上所述, 当目数增加到100目以后, 对检测效果的影响十分微小。 为了确保解谱面积的准确性, 选择100目以上样品即可。
2.1.5 压力的选择
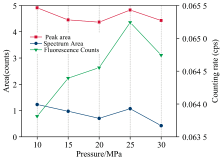
由图8可知, 当压片压力在10~25 MPa增加时, Cd的荧光计数呈上升趋势。 然而, 当压力超过25 MPa后, 荧光计数与解谱面积都呈下降趋势。 综合考虑计数率、 净峰面积和解谱面积, 25 MPa的压力条件下检测效果最佳。
2.1.6 保压时间的选择
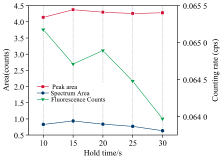
由图9可知, 当压片保压时间逐渐增大时, Cd的荧光计数率呈下降趋势, 而净峰面积和解谱面积变化不大。 为了确保样品的紧实度, 选择20s的保压时间最为适宜。
综上所述, 最佳的检测条件为: 管电压70 kV、 管电流700 μ A、 检测时间1 200 s、 样品质量12.00 g、 颗粒粒径≥ 100目、 压片压力25 MPa、 保压时间20 s。
2.2.1 标准加入法计算Cd浓度
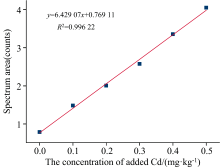
以Cd加标浓度为横坐标, 仪器解谱面积为纵坐标建立标准曲线, 如图10所示。 拟合得出的标准曲线方程为y=6.429 07x+0.769 11, R2=0.996 22, 线性度优秀, 表明样品中Cd的荧光计数与Cd的浓度变化存在有明显线性关系。
曲线与x轴的交点即原本样品中的Cd浓度, 经计算为0.120 mg· kg-1。
2.2.2 增量法计算Cd浓度
假设在该基质中, 加入Cd元素后的荧光强度变化与物质中本身所含Cd元素浓度变化呈线性关系, 则物质中Cd元素的浓度可以按照式(1)计算
式(1)中: cx为基质中待测元素的浓度; cΔ x为待测元素的增加量; Ix为未添加待测元素时的荧光强度; Ix+Δ x为添加待测元素后的荧光强度。
根据样品的加标浓度与解谱面积, 由式(1)计算未加标样品的Cd元素浓度, 计算结果如表9所示。
| 表9 增量法计算样品中Cd浓度 Table 9 Calculated value of Cd by incremental method |
在假设荧光强度变化与基质中元素浓度变化呈线性关系的前提下, 计算结果的平均值显示, 样品中Cd元素的浓度为0.124 mg· kg-1。
2.2.3 GFAAS法检测Cd浓度
委托第三方检测公司对相同来源的大豆样品粉末进行检测, 采用的检验方法为GB 5009.15— 2023(第一法 石墨炉原子吸收光谱法), 检测结果为0.133 mg· kg-1。
对比标准加入法、 增重法与石墨炉原子吸收光谱法的检测结果可知, 大豆对Cd2+的络合效果较好。 如图10所示, Cd的荧光强度与其元素浓度之间存在明显的线性关系, 且线性度优秀。 然而, 检测结果受到其他因素的影响而产生偏差。 偏差可能主要来源于其他元素对Cd的吸收增强效应, 因此需要进行基体校正。
大豆中Sn元素含量丰富, 其峰位与Cd相邻, 且可能对Cd产生吸收增强效应。 由于其他影响元素的含量较小, 其影响相对较小, 因此本文主要考虑Sn对Cd的影响。
2.3.1 强度校正
本文中, 浓度校正模式并不适用, 而强度校正模式更为合适, 因为其只需知道标样中分析元素的浓度, 无需了解其他元素的浓度。 Lucas-Tooth-Price强度校正模式[16]的一般表达式为
式(2)中: Di是校正背景值, 表示方法的平均背景, k0与kij是校正系数, 这些系数与实验条件有关。
标准加入法所建立的曲线方程式为
该方程描述了Cd加标浓度(x)与Cd解谱面积(y)之间的关系。 为了计算元素浓度, 需要对上述方程进行改写, 得到式(4)方程式
此处的截距表示标准加入法中未加标样品中Cd的浓度。 通过将截距消除并代入Cd解谱面积与CIT3000SMR给出的Cd检测值进行比对, 发现存在稳定偏差。 计算所有偏差值的平均值为-0.033 95, 将上述方程式改写为
将Cd解谱面积代入式(5), 计算与CIT3000SMR检测结果的平均偏差为0.003 24, 说明CIT3000SMR的检测计算过程更接近式(5)。
结合式(2)与式(4)可以得到式(6)
式(6)中: cCd代表校正后的浓度, K是从标准加入法所得曲线改写后的斜率, aj为影响因子, ICd为镉的荧光强度, ISn为锡的荧光强度。
代入实验数据并通过Origin进行拟合, 得到cCd的表达式为
2.3.2 结果验证
根据2.1.7中的优化条件, 另外取4份过100目筛的大豆样品进行检测。 将所得ICd与ISn代入式(7)得到校正后检测值, 结果如表10所示。
| 表10 校正前后的检测值对比1( mg· kg-1) Table 10 Comparison of detection values before and after correction 1 (mg· kg-1) |
在经过强度校正之后, 能量色散X射线荧光法对同一样品源的检测结果偏差显著减少。 校正前的平均偏差为0.048 30, 校正后的平均偏差降至0.006 73, 准确度明显提升。
为了进一步验证校正方法的普适性, 随机取十份样品, 并将石墨炉原子吸收光谱法的检测值作为大豆中Cd的实际浓度值。 验证结果如表11所示。
| 表11 校正前后的检测值对比2( mg· kg-1) Table 11 Comparison of detection values before and after correction 2 (mg· kg-1) |
校正前的平均偏差为0.035 48, 校正后降至0.010 94, 表明应用标准曲线斜率进行的强度校正效果显著。
2.3.3 偏差对比
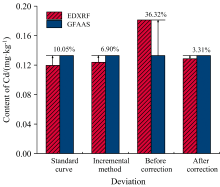
将标准曲线法、 增量法、 基体校正前后的检测值与石墨炉原子吸收光谱法(GFAAS)检测值进行对比, 结果如图11所示, 其中校正前后的检测值为计算后的平均值。 可以看出, 通过标准加入法得到的曲线与强度校正相结合后, Cd的检测平均偏差从36.32%降至3.31%。
采用能量色散X射线荧光(EDXRF)检测法, 结合标准加入法和固液混合制样法, 测定大豆样品中的Cd含量。 首先对大豆样品进行预处理, 并通过单因素实验优化检测条件, 最终确定最佳条件为: 管电压70 kV、 管电流700 μ A、 检测时间1 200 s、 样品质量12.00 g、 颗粒粒径≥ 100目、 压片压力25 MPa、 保压时间20 s。
以加标大豆中的Cd解谱面积与Cd加标浓度建立标准曲线, 拟合得到曲线方程的R2值为0.996 22, 表明Cd的荧光计数与其浓度存在显著的线性关系, 并验证了标准加入固液混合制样法的有效性。 该方法操作简便, 仅需检测样品与标准溶液, 克服了对纯元素标准样品及高成本标准物质的依赖。
使用标准加入法和增量法分别计算样品中的Cd浓度, 并与石墨炉原子吸收光谱法(GFAAS)检测结果进行了比较。 强度校正模式结合线性影响系数对仪器检测值进行校正。 校正前的平均偏差为0.048 30, 校正后的平均偏差为0.006 73。 随机取十份样品进行验证, 校正前的平均偏差为0.035 48, 校正后的平均偏差为0.010 94, 强度校正效果显著。 与GFAAS法对比, 校正后的检测偏差值从36.32%降至3.31%, 与标准曲线法和增量法对比, 偏差分别下降了6.74%与3.59%。
尽管本文提出的方法在校正后显著提高了检测精度, 但仍存在一定的改进空间。 大豆基体成分复杂, Sn元素以外的微量元素可能对Cd的吸收或增强效应产生微弱影响, 而本文校正模型未能完全覆盖。 在未来的研究中, 可进一步考虑大豆基体中其他可能的影响元素, 优化校正模型, 以进一步提高EDXRF方法在检测大豆中Cd含量的准确性和可靠性。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|