作者简介: 朱永炳, 2000年生,南京信息工程大学电子与信息工程学院硕士研究生 e-mail: 202312490194@nuist.edu.cn
静脉用药溶质浓度的定量分析一直是静配中心药物检测的研究热点, 但常规的调配和复核手段都是借助人工操作, 存在药液浓度把控受限、 人工复核压力繁重且低效等问题, 因此提出一种对静脉药物溶质浓度准确、 便捷、 无损的检测方法显得至关重要。 由于传统的近红外光谱对低浓度液体检测有一定局限性, 基于可调谐激光吸收光谱技术(TDLAS), 研究了了一种基于高效注意力机制一维卷积神经网络(ECA-1D-CNN)的葡萄糖混合溶液浓度定量检测模型。 为检测低浓度葡萄糖混合溶液, 以TDLAS技术为基础, 选择光强吸收率最高的980 nm波段作为激光器光源, 通过光电传感器, 获取药物浓度的透射光强信号, 由锁相放大模块解调为二次谐波信号得到一共600个不同浓度的自建数据集, 将样本按8∶2的比例划分为训练集和测试集。 以600个药物浓度透射光强的二次谐波信号作为研究对象, 采用ECA-1D-CNN进行葡萄糖混合溶液浓度的定量检测。 该模型共有4个卷积层, 均采用Relu激活函数激活, 每个卷积层后添加1个BN层, 每两个卷积层添加1个池化层, 在第2个池化层后添加1个ECA, 可以帮助网络模型更好地学习特征之间的关系, 减少参数数量和改善模型的鲁棒性。 首先, 为了凸显1D-CNN模型的优势, 使用相同的原始数据集在PCR、 SVR、 PLSR上进行建模并对比4种不同模型的预测效果。 其次, 在6种不同数据预处理的基础上, 将ECA-1D-CNN模型与1D-CNN模型进行对比, 以决定系数 R2、 绝对误差MAE、 均方根误差RMSE作为评价指标来分析预测模型的泛化能力。 结果表明, SG+Normalization预处理下的ECA-1D-CNN模型效果最优, 该方法能够对6~30 mg·100 mL-1的葡萄糖混合溶液浓度进行有效预测, 其模型训练集 R2可达到0.998, MAE为0.295, RMSE为0.343, 测试集的 R2可达到0.993, MAE为0.498, RMSE为0.691。 采用所提出的方法可以精准的预测静脉用药溶质的浓度, 为智能化静配中心的无损检测提供了新的思路以及应用价值。
The quantitative analysis of intravenous drug solute concentration has always been the research hotspot of drug detection in static dispensing centers. Still, the conventional means of mixing and reviewing are operated manually. There are problems such as limited control of the concentration of the drug solution, laborious pressure of manual review, and inefficiency, so it is crucial to propose an accurate, convenient, and non-destructive detection method for intravenous drug solute concentration. Due to the limitations of traditional near-infrared spectroscopy for the detection of low-concentration liquids, based on tunable laser absorption spectroscopy (TDLAS) technology, a quantitative detection model of glucose mixed solution concentration based on efficient attention mechanism one-dimensional convolutional neural network (ECA-1D-CNN) was investigated. In order to detect the low concentration of glucose mixed solution, based on the TDLAS technology, the 980 nm band with the highest light intensity absorption rate was selected as the laser light source, and through the photoelectric sensor, the transmitted light intensity signal of the drug concentration was acquired, which was demodulated into the second harmonic signal by the phase-locked amplification module to obtain a total of 600 self-constructed datasets of different concentrations, and the samples were divided into training and testing sets in the ratio of 8∶2. Aiming at the second harmonic signal of the transmitted light intensity of 600 drug concentrations as the research object, a glucose mixed solution concentration detection model based on the one-dimensional convolutional neural network model with efficient attention mechanism (ECA-1D-CNN) is proposed, with a total of four convolutional layers, all of which are activated by the Relu activation function, and a BN layer is added after each convolutional layer, a pooling layer is added after every two convolutional layers, and a pooling layer is added after the 2nd pooling layer, and a pooling layer is added after the 2nd pooling layer, and a pooling layer is added after the 2nd pooling layer. Adding 1 ECA after the 2nd pooling layer can help the network model to learn the relationship between features better, reduce the number of parameters, and improve the robustness of the model. First, to highlight the advantages of the 1D-CNN model, the same original dataset is used to model PCR, SVR, and PLSR and compare the prediction effects of the 4 different models. Second, based on six different data preprocessing, the ECA-1D-CNN model was compared with the 1D-CNN model to analyze the generalization ability of the prediction model by using the coefficient of determination R2, the absolute error MAE, and the root-mean-square error RMSE as the evaluation indexes. The results showed that the ECA-1D-CNN model under SG+Normalization preprocessing was the most effective, which was able to effectively predict the concentration of glucose mixed solution from 6 to 30 mg·100 mL-1, and the R2 of the model's training set could reach 0.998, the MAE 0.295, and the RMSE 0.343, and the R2 of the test set could reach 0.993, MAE of 0.498, RMSE of 0.691. The proposed method can accurately predict the concentration of intravenous drug solutes, which provides a new idea and an application value for the nondestructive testing of intelligent static dispensing centers.
静脉注射是临床治疗以及挽救患者生命的重要给药方式。 药液的浓度过高或过低都可能导致治疗效果不佳或患者出现不良反应, 因此准确检测静脉用药的浓度显得至关重要[1]。 常规的静脉注射药物以5%葡萄糖、 0.9%氯化钠(生理盐水)作为溶媒, 搭配盐酸氨溴索、 头孢、 兰索拉唑等溶质, 以应对各种疾病。 随着医疗技术的不断进步, 静脉药物调配中心(PIVAS)作为提供静脉配液服务的关键环节变得愈发重要。 PIVAS的设施和设备是确保药物调配质量的基础, 现代化的设备和先进的辅助设备能够提高药物调配的精准度和效率, 减少人为错误的发生, 不仅降低了药物交叉污染的风险, 还提升了药物调配的质量和安全[2, 3]。 因此, 有关静脉注射药物剂量的把控对于静配中心建设具有重要意义。
近年来, 光谱分析技术在液体检测领域的应用已经取得了显著的进展, 通过分析液体样本的光谱特征, 可以快速、 无损地获取液体的组分信息。 比如在液体浓度的定量分析方法中, 拉曼光谱检测技术[4, 5, 6, 7]、 近红外光谱检测技术[8, 9, 10]、 紫外可见光谱法(UV-Vis)[11, 12, 13]较为成熟。 目前化学计量学结合光谱分析逐渐成为主流分析方法进入液体检测领域, 用于液体的分类以及浓度检测。 余驰[14]等通过近红外光谱建立偏最小二乘(PLS)定量模型, 实现对葡萄糖注射液含量的快速定量分析。 Rhadem[15]等通过多种机器学习的对比, 建立支持向量机回归(SVR)模型对40~500 mg· dl-1范围内葡萄糖水溶液浓度进行有效预测。 Al-Mbaideen[16]等提出了一种PCA-ICR模型, 能够提取葡萄糖的相关信息并从光谱中去除一部分噪声, 相比PLS和PCR模型能更有效预测葡萄糖的浓度。
然而, 针对上述的光谱法结合深度学习对静脉用药溶质浓度的检测研究相对较少且需要依靠光谱仪来完成, 而这种方法需要一套复杂的光学系统。 如何提供一种不依赖于复杂光学系统实现对静脉用药溶质浓度的预测是一个值得研究的问题, 为此本文提出了一种以近红外LD为激光光源, 采用TDLAS技术[17, 18, 19]实现对静脉用药浓度的探测。 在实际检测过程中, 采用波长调制技术能够有效的将微弱的液体吸收信息提取出来, 通过光-电转换方式, 得到一个稳定的二次谐波信号作为溶质浓度信息, 结合ECA-1D-CNN模型实现对静脉用药溶质浓度的预测。 利用本文所提出的方法可以精准预测静脉用药溶质浓度, 为静配中心的智能化提供了可行的办法。
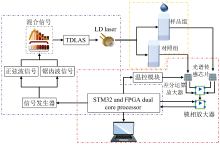
为了采集不同浓度的葡萄糖混合溶液的二次谐波数据, 搭建了如图1所示的静脉药液浓度数据采集装置。 实验装置主要由波长调制、 药液吸收、 数据采集这三部分组成, 分别由紫色框、 黄色框、 红色框标志。
由江苏省人民医院提供的5%葡萄糖溶液和盐酸氨溴索2个药物样品。 药品长期存放在4 ℃的冰箱内, 以保证药品的质量和活性。 按照常规配方和药品说明书的要求, 以5%葡萄糖溶液为溶媒, 盐酸氨溴索为溶质, 按照规定的比例和方法进行混合, 制备成相应的药物剂型。 如表1所示, 为5种不同浓度的盐酸氨溴索-葡萄糖(YS-G)的调配比例, 共计600个药物样本为研究对象。
| 表1 实验数据集 Table 1 Experimental data set |
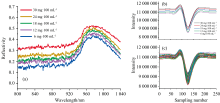
为确保能够得到最佳的透射光强信号, 使用超连续光谱仪对5种不同浓度的药液进行照射, 所测的药液光谱吸收率如图2(a)所示, 在960~1 000 nm波段的光强相比其他波段有较强的吸收峰, 尤其在980 nm附近达到顶峰, 药液的浓度与光强的吸收率成正比, 故本次实验装置采用中心波长λ =980 nm的LD激光器作为激光光源。 实验装置使用频率为1 kHz电平为(300 mV的高频正弦波叠加频率为3 Hz高低电平分别为1.8和0 V的低频锯齿波作为激光器的驱动信号, 实现对LD激光器(980 nm)的波长调制, 得到特定波段的红外激光信号。 通过分光器将红外激光分为两束光强相同的光信号分别照射放有葡萄糖混合溶液的比色皿和空比色皿, 由光电传感器采集这两路光信号, 通过平衡差分法进行相减得到光电传感信号, 再由锁相放大模块对当前波段的差分后的光电传感信号进行解调得到二次谐波信号。 系统解调出二次谐波信号后, 采用十六位高精度模数转换器(ADC)采集电路和串口模块, 配合虚拟仪器(labview)作为上位机进行药液浓度的数据采集。 实验采集的不同浓度药液透射光强二次谐波信号如图2(b)所示, 全部采集数据结果如图2(c)所示。
1.2.1 1D-CNN网络
卷积神经网络(convolutional neural network, CNN)是一种深度学习模型, 常用于图像识别、 语音识别等领域。 1D-CNN主要用于处理一维序列数据, 如时间序列数据、 文本数据等。 在光谱学分析中1D-CNN受到了广泛的应用, 通过1D-CNN模型能够有效地处理光谱数据并提取其中的特征, 从而实现对样本的分类、 定量分析等任务。
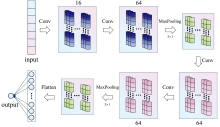
1D-CNN通常包括卷积层、 池化层和全连接层, 其中卷积层通过滑动卷积核提取输入序列中的特征, 池化层用于降维和保留最显著的特征, 全连接层则用于输出最终的预测结果。 如图3示, 本研究提出了一种基于1D-CNN的定量分析模型, 用于静脉用药溶质浓度的预测。
1.2.2 ECA网络
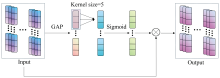
ECA(efficient channel attention)注意力机制是一种用于增强神经网络模型性能的模块。 通过引入高效通道注意力机制, 计算每个通道的重要性权重, 来动态调整特征图中不同通道的贡献程度, 使得模型更加关注重要的特征信息, 能够有效地提升神经网络模型的性能。 ECA网络结构如图4所示。
将输入特征图经过全局平均池化, 根据特征图的通道数计算得到自适应的一维卷积核大小Kernel_size, 公式为
式(1)中, γ =2, b=1, c为维度大小, 得到对于特征图的每个通道的权重。 最后将归一化权重和原输入特征图逐通道相乘, 生成加权后的特征图。
1.2.3 定量分析网络模型的建立
采用1D-CNN网络模型结合ECA注意力机制(efficient channel attention)设计定量分析模型用于处理二次谐波数据, 二次谐波数据共有250个样本点, 共使用了13层网络搭建模型, 主要包含输入层、 卷积层、 池化层、 批量归一化层(batch normalization, BN)、 ECA层、 全连接层、 输出层。 在每层卷积层之后加入BN层, 能够防止梯度消失和爆炸的问题, 计算过程如式(2)— 式(5)。
$\mu_{x}=\frac{1}{n} \sum_{i \in(1, n)} x_{i}$(2)
$\sigma_{X}^{2}=\frac{1}{n} \sum_{i \in\{1, n\}}\left(x_{i}-\mu_{X}\right)^{2}$(3)
$\hat{x}_{i}=\frac{x_{i}-\mu_{X}}{\sqrt{\sigma_{X}^{2}+\varepsilon}}$(4)
$y_{i}=\gamma \hat{x}_{i}+\beta=B N_{\gamma, \beta\left(x_{i}\right)}$(5)
式(2)— 式(5)中: xi∈ X={x1, x2, …, xn}用于处理前数据, yi用于处理后数据; 其中γ 和β 是可学习的参数, 用于缩放和平移标准化后的数据。 采用SGD优化器对模型进行优化更新, Epoch=800, batch size=8。 葡萄糖混合溶液浓度定量分析模型结构如表2所示, 由250× 1矩阵作为输入, 共有4个卷积层, 卷积核大小分别为9× 1、 7× 1、 5× 1、 3× 1, 均采用Relu激活函数, 每个卷积层后添加1个BN层, 每两个卷积层后面添加1个最大池化层, 在第二个池化层后添加1个ECA注意力机制, 再通过全连接层平铺展开映射输出静脉用药溶质的浓度。
| 表2 定量分析模型结构 Table 2 Quantitative analysis of model structure |
通过一维卷积神经网络构建静脉用药浓度预测模型, 采用决定系数(R2)、 绝对误差(MAE)、 均方误差(MSE)和均方根误差(RMSE)来评估模型的性能。 R2用于衡量模型对数据方差的解释能力, 决定系数越接近1表示模型对数据的拟合程度越好。 使用均方误差(MSE)作为损失函数, 用于衡量模型预测值与真实值之间的差异, 损失函数越趋于0, 反映模型的预测准确性和稳定性越好。 RMSE是MSE的平方根与MAE一起提供了更全面的误差评估信息。
为分析不同处理方法对模型的影响, 采用了6种预处理方法, 如图5所示根据预处理的目的能够分为散射校正、 数据归一化、 平滑处理、 均值中心化这四类[20]。 其中多元散射校正(MSC)和标准正态变量(SNV)属于散射校正, 能够消除由于样品表面粗糙度、 颗粒大小等因素引起的散射现象; 平滑处理(SG)可以有效平滑光谱数据, 去除噪声, 保留信号特征, 提高数据质量; 最大最小归一化(Max_Min_Normalization)和SG+Normalization属于归一化处理, 将不同特征的数据值统一缩放到同一范围内, 从而消除特征值的量纲影响, 提高数据的可比性和模型的稳定性; 均值中心化处理(Mean_Centralization)用来消除特征值的位置偏差, 弱化均值对模型结果的影响, 可以提高模型的准确性和解释能力。
为建立一种能够高效、 精准预测静脉用药浓度的模型, 使用原始数据集以确保数据输入的一致性, 将数据集按8∶ 2的方式分为训练集和测试集, 设置相同的随机种子(random_state=42), 通过sklearn库中的主成分回归分析法(PCR, n_components=12)、 支持向量回归(SVR, kernel=‘ linear’ )、 偏最小二乘回归法(PLSR, n_components=16)以及一维卷积神经网络(1D-CNN)构建多种浓度预测模型, 并对4种模型预测结果进行对比分析。 综合四种模型SVR、 PCR、 PLSR和1D-CNN在回归预测任务中的实际表现, SVR、 PCR和PLSR这三种模型在处理复杂数据和特征提取方面受到限制, 预测性能相对较差。 对比4种模型在测试集上的表现如表3所示, 1D-CNN模型能够更好地捕捉数据中的非线性关系和复杂特征, 在4种模型中具有最强的表征能力和泛化能力, 其决定系数达到0.903, MAE为1.917, RMSE为2.661。 另外三种模型的决定系数均低于0.9, MAE和RMSE也都低于预期指标范围, 模型的泛化能力有待提高。 相比之下, 1D-CNN具有更强的表征学习能力和泛化能力, 在信号提取、 特征学习和复杂关系建模等方面具有一定优势。
| 表3 不同模型泛化能力对比 Table 3 Comparison of generalization ability of different models |
为了说明算法的优势, 采用6种不同的预处理方法分别通过1D-CNN和ECA-1D-CNN构建预测模型, 对静脉用药溶质浓度进行预测。 在6种不同预处理实验中, 由表4可以看出, 经过预处理后的数据在ECA-1D-CNN的表现相比1D-CNN有所提高。 对于1D-CNN模型, 未经过预处理的原始数据在模型表现中相对较差, R2在训练集和测试集中分别为0.915和0.903。 尽管SNV、 MSC、 Max_Min_ Normalization和Mean_Centralization预处理后的训练集R2达到0.991、 0.979、 0.981、 0.978, 但他们的测试集R2仅为0.935、 0.915、 0.930、 0.923, 未达到理想的拟合效果。 对于ECA-1D-CNN模型, 经过SG预处理后的的数据能够平滑信号中的噪声, 更好地保留信号的特征和细节, 其决定系数R2在训练集和测试集中分别为0.993和0.981。
| 表4 不同预处理对模型性能的影响 Table 4 Effects of different pretreatments on model performance |
其中SG+Normalization预处理方法在两种模型上的表现最佳, 在SG平滑处理的基础上加入归一化处理, 可以避免不同特征之间的差异对模型训练和栅测的影响。 如图6(a)和(b)所示为ECA-1D-CNN模型的溶质浓度预测值和真实值拟合曲线图, 在该模型上的训练集R2为0.998, MAE为0.295, RMSE为0.343, 模型在测试集上的R2为0.993, MAE为0.498, RMSE为0.691。 相较于传统的1D-CNN模型, ECA-1D-CNN模型的预测结果R2在训练集和测试集上分别提升了0.706%和3.54%, MAE分别降低了51.7%和60.5%, RMSE分别降低了58.6%和60.1%, 大大提高了模型的预测精度。
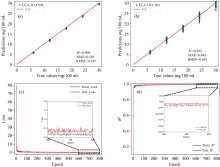 | 图6 训练集回归曲线图(a); 测试集回归曲线图(b); 损失函数曲线(c); 决定系数曲线(d)Fig.6 Regression curve of training set (a); Regression curve of testing set (b); Loss function curve (c); Coefficient of determination curve (d) |
如图6(c)和(d)所示, 分别为SG+Normalization预处理在ECA-1D-CNN模型下的R2和Loss随Epoch变化的曲线。 从图6(c)局部放大图中可以看出, 预测误差较小, Loss损失函数几乎低于0.5并趋于稳定。 从图6(d)局部放大图中可以看出, 决定系数R2在0.99至1之间稳定波动表现出较好的预测能力。 该模型表现出优良的拟合关系, 具有较强的泛化能力。
采用TDLAS技术, 利用不同静脉药物溶液的吸收谱线特点选定最佳的激光器获取最优拟合葡萄糖混合溶液浓度的二次谐波信号, 提出一种基于ECA-1D-CNN模型建立静脉用药溶质浓度的定量检测模型方法。 相比传统的1D-CNN模型在训练集上表现良好而泛化能力较差, 改进后的ECA-1D-CNN模型增强通道特征实现网络性能的改进, 实现深层次静脉用药浓度二次谐波信号的挖掘, 有效提升了静脉用药浓度定量检测模型的预测性能。 为验证本文所提方法的可行性, 利用不同预处理方法分别进行建模, 结果表明SG+Normalization预处理表现最佳, 在ECA-1D-CNN中的训练集R2达到0.998, MAE为0.295, RMSE为0.343, 训练集R2达到0.993, MAE为0.498, RMSE为0.691。 本文提出了一种基于ECA-1D-CNN实现对静脉用药浓度定量检测方法, 填补了静配中心有效复核静脉药物溶质浓度信息的空白, 为静配中心迈向智能化、 信息化、 自动化提供了新的思路。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|