作者简介: 孙中远, 2000年生, 绍兴文理学院化学化工学院硕士研究生 e-mail: 1633660403@qq.com
核磁共振波谱(NMR)和红外光谱(IR)是两种常用的谱学检测方法, 不仅可以用于物质含量分析和分子结构鉴定, 而且还能通过其吸收峰的强度与位置, 从分子层面来表征分子间相互作用位点、 类型和强度等重要微观信息, 已被拓展应用于研究化学反应机理。 CO2资源化利用是当前绿色化学研究热点之一。 离子液体(ILs)具有蒸汽压低、 热稳定性高和结构与性质可调的特点, 作为一种新型、 绿色的催化剂广泛应用于CO2与邻氨基苯腈反应, 能同时活化CO2和邻氨基苯腈, 在无金属、 温和条件下使常压CO2高效化学转化为具有生物活性的喹唑啉-2,4(1H,3H)-二酮及衍生物, 显示出了优异催化性能和潜在应用价值。 因此, 其化学反应机理引起了广大研究者的浓厚兴趣。 掌握化学反应机理是有效调控反应的前提, 而借助正确、 合适的检测方法来表征ILs与反应底物之间的相互作用信息, 是研究化学反应机理的有效途径和关键步骤。 为此, 为了更好地了解和掌握NMR和IR等谱学方法在研究ILs催化CO2与邻氨基苯腈反应机理中的应用及进展, 在简述ILs催化CO2与邻氨基苯腈反应发展的基础上, 首先介绍了NMR和IR技术的自身特点及其在研究该反应机理中所发挥的作用; 其次, 重点聚焦1H NMR、13C NMR、15N NMR、183W NMR、 FTIR和 in-situ FTIR等手段在表征ILs与CO2或邻氨基苯腈相互作用机制、 反应过程中新形成(消失)的基团和形成可能的反应中间体等方面所取得的应用进展, 结合文献调研详细分析了NMR和IR技术在研究化学反应机理中的独特优势与存在的问题, 并提出了可能的解决思路和方案; 最后, 为进一步推广NMR和IR技术应用于化学反应机理研究提出了合理建议, 即利用二维NMR和IR光谱获得更精细的分子结构和相互作用信息, 进一步确定催化剂与底物的相互作用位点与类型, 再结合DFT计算和分子动力学模拟等理论方法获得的反应过程中底物的电子结构和体系的能量变化, 准确地获取反应中间体和过渡态的结构信息, 从而更加清晰地阐明反应机理, 这将迎来NMR和IR在研究化学反应机理的新发展。
Nuclear magnetic resonance (NMR) and infrared (IR) spectra are two commonly used spectroscopic methods, which can not only be used for the analysis of substance content and identification of molecular structure, but also characterize important microscopic information such as intermolecular interaction sites, types and strengths at the molecular level through the intensity and position of the absorption peaks, and have been expanded to be used in the study of chemical reaction mechanisms. The resourceful utilization of CO2 is one of the current hotspots in green chemistry research. Ionic liquids (ILs), with low vapor pressure, high thermal stability and adjustable structure and property, are widely used as a new type of green catalysts for the reaction of CO2 with 2-aminobenzonitrile, which can simultaneously activate CO2 and 2-aminobenzonitrile, and efficiently convert atmospheric CO2 into biologically active quinazoline-2,4(1H,3H)-dione and its derivatives under metal-free and mild conditions, showing excellent catalytic performance and potential application value. Therefore, its chemical reaction mechanism has garnered significant interest from a diverse range of researchers. Understanding the chemical reaction mechanism is a prerequisite for effective regulation of the reaction. Characterizing the interaction information between ILs and reaction substrates, aided by suitable detection methods, is an effective way and a key step in studying the chemical reaction mechanism. For this reason, to better understand the application and progress of NMR and IR spectroscopic methods in the study of the mechanism of IL-catalyzed reaction of CO2 with 2-aminobenzonitrile, based on briefly description of the history and current development of the reaction between CO2 and 2-aminobenzonitrile, we firstly introduce the characteristics of NMR and IR techniques and their roles in the study of this reaction mechanism. Secondly, we focus on1H NMR,13C NMR,15N NMR,183W NMR, FTIR and in-situ FTIR in the characterization of the interaction of ILs with CO2 or 2-aminobenzonitrile, the newly formed (disappeared) groups and the formation of possible reaction intermediates, etc., and combined with the results of the literature, and then the unique advantages and problems of the NMR and IR techniques in the study of the intermolecular interactions and the mechanism of chemical reactions are analyzed, and possible solutions are proposed. Finally, reasonable suggestions are put forward for the further promotion of the application of NMR and IR spectra in the study of chemical reaction mechanisms, namely, using two-dimensional NMR and IR spectra to obtain more refined molecular structure and interaction information, further determining the interaction sites and types between catalysts and substrates, and combining theoretical methods such as DFT calculation and molecular dynamics simulation to obtain the electronic structure of substrates and energy changes of the system during the reaction process, accurately obtaining the structural information of reaction intermediates and transition states, and thus clarifying the reaction mechanism more clearly. This will usher in new developments in NMR and IR spectra in the study of chemical reaction mechanisms.
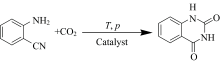
CO2过量排放是造成全球气候变暖的主要原因, 碳捕集与封存(CCS)和碳捕集与利用(CCU)是实现碳中和的两种重要技术[1]。 其中, CCU技术是通过将捕集的CO2转化为高附加值的化工品, 不仅使CO2变成可再生资源, 而且起到了保护环境的作用[2, 3]。 在所报道的CO2化学转化反应中, 以CO2与邻氨基苯腈为底物, 在催化剂作用下制备喹唑啉-2, 4(1H, 3H)-二酮(图1), 引起了研究者的兴趣[4]。 该反应不仅能有效利用CO2, 而且有望替代传统方法来合成具有生物活性的喹唑啉及其衍生物[5, 6, 7, 8, 9, 10]。 目前, 该反应常用的催化剂为有机强碱、 无机碱金属和金属氧化物[11, 12, 13, 14], 一般需在高温、 高压和极性溶剂条件下才能实现CO2的化学转化, 且催化剂重复使用性能有待改善[15]。 例如, 373.15 K时, Sheng等采用有机强碱DBU催化1.0 MPa CO2与邻氨基苯腈反应, 产物的分离产率仅为70%[13]; Yan等以Cs2CO3为催化剂和DMF为溶剂, 373.15 K和1.3 MPa CO2压力时, 分离产率为94%[16]; Rasal等采用La-Mg氧化物作为催化剂, 在3.5 MPa CO2和413.15 K条件下, 分离产率为92%[17]。 因此, 发展一种新型、 绿色的催化剂, 在温和反应条件下实现CO2与邻氨基苯腈反应具有重要意义[18]。
离子液体(ILs)是一类完全由阴、 阳离子组成的室温熔盐, 具有蒸汽压低、 热稳定性高和结构与性质可调的特点, 在催化CO2与邻氨基苯腈反应中表现出优异性能[19, 20, 21]。 例如, Patil等首次报道了将氢氧化烷基咪唑型ILs作为催化剂应用于CO2与邻氨基苯腈反应, 产物产率为90%[22], 表明ILs具有催化CO2化学转化的应用前景。 研究者们后续发展了一系列性质更加稳定的功能化ILs应用于催化CO2与邻氨基苯腈反应, 并对相关研究进展进行了阶段性总结[23, 24]。 例如, Wang等重点关注ILs催化CO2与邻氨基苯腈反应的CO2压力和温度等条件[23]; Zhang等归纳总结了不同类型的ILs催化CO2与邻氨基苯腈反应的性能及其影响因素, 并初步比较了反应机理[24]。 上述工作侧重于总结ILs的种类、 性质和结构对反应性能的影响, 而对ILs与反应底物之间的相互作用机制及反应机理尚未系统分析与比较。 掌握反应机理是调控反应的前提, 而选择合适检测手段来表征ILs与反应底物之间的相互作用, 又是获得反应机理的有效途径[25]。
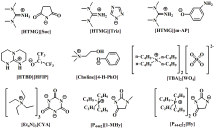
近年来, 核磁共振波谱(NMR)和红外光谱(IR)被广泛应用于表征ILs与反应底物之间的相互作用及探究ILs催化CO2与邻氨基苯腈反应机理, 显示出了特有优势和良好应用前景。 随着谱学技术的发展, 15N NMR、 183W NMR和in-situ FTIR等新型谱学技术也被应用于深入研究ILs催化CO2与邻氨基苯腈反应机理, 进一步发挥了谱学方法在研究反应机理中的作用。 因此, 系统总结NMR和IR技术在研究ILs催化CO2与邻氨基苯腈反应机理的应用进展具有重要意义, 这不仅有利于化学反应的调控, 而且有助于将谱学方法全面应用于化学反应机理研究。 为此, 对NMR和IR两种谱学方法在研究ILs催化CO2与邻氨基苯腈反应机理的应用及进展进行了归纳和评述, 所涉及ILs的结构及缩写见图2。
NMR是一种利用核磁共振现象来测定分子结构的谱学技术, 其化学位移大小决定于原子核外的电子云密度, 这不仅与原子在分子中所处的化学环境有关, 而且还与分子间相互作用相关[26]。 ILs催化CO2与邻氨基苯腈反应时, ILs通过与邻氨基苯腈的氨基(— NH2)、 氰基(— CN)及CO2发生相互作用来活化反应底物, 并引起反应体系中1H、 13C、 15N等化学位移的改变[27]。 因此, 采用NMR来表征底物或ILs的化学位移, 并确定ILs与底物相互作用位点和作用方式, 再结合根据新生成或消失的特征官能团, 可用于推测反应机理[28]。 下面, 详细介绍1H NMR、 13CNMR、 15N NMR、 183W NMR等谱学技术在研究ILs催化CO2与邻氨基苯腈反应机理的应用进展。
通过测定纯ILs和反应底物及两者混合体系的1H NMR图谱, 分析1H NMR化学位移变化, 来表征ILs与反应底物相互作用位点或作用方式, 已被应用于研究ILs催化CO2与邻氨基苯腈反应机理。 例如, Ping等比较了邻氨基苯腈、 [HTMG][m-AP]以及邻氨基苯腈-[HTMG][m-AP]体系的1H NMR化学位移, 发现邻氨基苯腈-[HTMG][m-AP]体系在化学位移为8.29 ppm处出现了一个新峰[图3(a)], 这归属于邻氨基苯腈— NH2中的一个活泼氢原子转移至[m-AP]-阴离子后所形成的[m-AP]-…H…NH氢键复合体的新峰, 表明[m-AP]-阴离子与邻氨基苯腈— NH2之间存在氢键作用, 并由此提出了如下反应机理[图3(b)]: [m-AP]-阴离子首先与邻氨基苯腈的— NH2发生氢键作用使其活化, 活化后的— NH2再与活化的CO2分子发生亲核反应, 经过分子内亲核成环和重排得到喹唑啉-2, 4(1H, 3H)-二酮, 同时使ILs得到再生[29]。 其他文献报道了1H NMR研究[HTMG][Suc]和[HTMG][Triz]等ILs催化CO2与邻氨基苯腈反应机理, 得到了与[HTMG][m-AP]相似的结果[30, 31]。 此外, Shi等[32]和Hulla等[33]在采用1H NMR 研究ILs催化CO2与邻氨基苯腈反应机理时也提出ILs的阴离子能与邻氨基苯腈的— NH2形成氢键, 且这是引发后续CO2转化的关键步骤[34, 35]。 上述结果表明, 采用1H NMR能获得ILs与邻氨基苯腈— NH2之间的相互作用信息, 使其在探究反应机理方面具有显著的优势[36]。
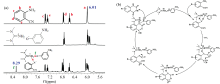 | 图3 邻氨基苯腈-[HTMG][m-AP]体系1H NMR (a)和[HTMG][m-AP]催化CO2与邻氨基苯腈反应机理 (b)[29]Fig.3 1H NMR spectra of 2-aminobenzonitrile-[HTMG][m-AP]mixture (a) and mechanism of [HTMG][m-AP]-catalyzed reaction of CO2 and 2-aminobenzonitrile (b)[29] |
ILs与反应底物相互作用时, 除了会改变1H NMR化学位移, 还会引起13C NMR化学位移的变化。 邻氨基苯腈的— CN 和CO2的羰基(C=O), 均能借助13C NMR谱学进行分析, 并用于判断反应中ILs与底物的相互作用信息[37]。 例如, Phatake 等对比了邻氨基苯腈-[HTBD][HFIP]体系通入CO2前、 后13C NMR图谱, 发现随着CO2的通入, 在160.53 ppm处出现了一个新峰, 这归属于[HFIP]-阴离子与CO2化学作用后新形成碳酸盐的C=O峰, 表明ILs阴离子通过化学吸收活化了CO2[38]; 此外, 作者还发现在[HTBD][HFIP]中加入邻氨基苯腈后, [HFIP]-阴离子的C1的化学位移从68.33 ppm向低场移动至68.57 ppm[图4(a)], 化学位移相对值(|Δ δ |/δ )为0.35%, 作者认为这源于[HFIP]-阴离子与邻氨基苯腈的— NH2的氢键作用降低了阴离子中C1的电子云密度所致[38]。 同时, 当邻氨基苯腈中加入[HTBD][HFIP]后, 邻氨基苯腈— NH2的1H NMR化学位移从5.94 ppm移动至6.01 ppm[图4(b)], |Δ δ |/δ 值为1.18%, 表明[HFIP]-阴离子与邻氨基苯腈的— NH2形成了氢键作用。 因此, 基于NMR谱学确定的ILs阴离子与反应底物的相互作用, 提出了与文献[29]相似的反应机理。 上述结果表明, 13C NMR擅长提供ILs与CO2相互作用及活化CO2的直接证据; 而对于鉴定ILs与邻氨基苯腈的— NH2之间的相互作用, 通过比较|Δ δ |/δ 值可以判断13C NMR谱学的灵敏性不如1H NMR谱学。 因此, 建议将1H NMR与13C NMR相结合, 全面获得ILs与CO2、 邻氨基苯腈相互作用, 为合理推测反应机理提供全面信息。
明确ILs与邻氨基苯腈相互作用位点是研究反应机理的重要组成部分。 功能化ILs的阴离子除了能与邻氨基苯腈的— NH2形成氢键作用外, 还能与邻氨基苯腈的— CN发生相互作用, 这是一种新的反应途径。 ILs的阴离子无论与邻氨基苯腈的— NH2还是— CN发生相互作用, 均会影响— NH2或— CN中15N的电子云密度, 进而影响15N的化学位移。 因此, 15N NMR已被用于确定ILs与邻氨基苯腈的相互作用位点以及ILs催化CO2与邻氨基苯腈反应机理[39]。 本课题组最近研究发现, 在邻氨基苯腈中加入[P4442]2[Hy]后, — NH2的15N NMR化学位移从67.9 ppm移动至69.3 ppm[图5(a)], 而— CN的15N NMR化学位移基本维持在264.0 ppm 左右几乎不变; 与此同时, [Hy]2-中N-的15N NMR化学位移从84.6 ppm移动至85.8 ppm, 这说明[Hy]2-中的N-与邻氨基苯腈的— NH2发生氢键作用并活化了— NH2, 而[Hy]2-阴离子并不与— CN直接作用。 为此, 课题组明确提出[Hy]2-阴离子与邻氨基苯腈— NH2的相互作用强度大于与— CN的相互作用强度, 即[Hy]2-阴离子优先活化邻氨基苯腈的— NH2, 随后被活化的— NH2亲核进攻被[Hy]2-阴离子活化的CO2, 再经过分子内重排、 质子转移和异构化, 最后得到产物并使ILs再生[图5(b)][40]。
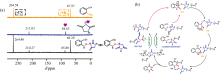 | 图5 邻氨基苯腈-[P4442]2[Hy]体系15N NMR(a)和[P4442]2[Hy]催化CO2与邻氨基苯腈反应机理(b)[40]Fig.5 15N NMR spectraof 2-aminobenzonitrile-[P4442]2[Hy] mixture and mechanism of [P4442]2[Hy]-catalyzed reaction of CO2 and 2-aminobenzonitrile (b)[40] |
除了直接表征反应底物中元素的化学位移外, ILs中元素的化学位移变化也被常用于表征其与底物之间的相互作用, 并研究ILs催化CO2与邻氨基苯腈反应机理。 例如, Kimura等对比分析了邻氨基苯腈-[TBA]2[WO4]体系的183W NMR化学位移, 发现[WO4]2-阴离子的化学位移由纯物质的16.4 ppm向高场移动至混合体系的1.6 ppm[图6(a)], 提出了[WO4]2-阴离子通过与邻氨基苯腈— NH2形成氢键作用活化— NH2, 从而导致[WO4]2-阴离子的化学位移向高场移动[41]。 此外, 向[TBA]2[WO4]通入CO2(0.1 MPa)后, 183W NMR谱图显示[WO4]2-阴离子位于16.4 ppm的峰强度有所下降, 同时在57.8 ppm出现一个新峰, 作者将其归属于新形成的[WO4]2-— CO2复合物; 且随着CO2压力逐渐增加至0.6 MPa, 在22.6 ppm出现一个新峰, 并伴随着16.4和57.8 ppm峰的消失, 作者提出了形成了[WO4]2-— (CO2)2复合物, 上述结果表明[WO4]2-阴离子具有活化CO2能力[41]。 基于183W NMR 结果, 作者提出了如下反应机理[图6(b)]: 首先[WO4]2-阴离子同时活化邻氨基苯腈的— NH2与CO2, 被活化的— NH2亲核进攻被活化的CO2, 形成氨基甲酸中间体, 随后发生质子转移以及分子内重排得到产物, 且作者采用DFT计算验证了上述反应机理。 此外, Kimura等还采用183W NMR研究了CO2与邻苯二胺反应的机理, 进一步证实了183W NMR谱学在揭示反应机理的可行性[42]。
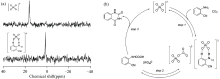 | 图6 邻氨基苯腈-[TBA]2[WO4]体系183W NMR(a)和[TBA]2[WO4]催化CO2与邻氨基苯腈反应机理(b)[41]Fig.6 183W NMR spectra of 2-aminobenzonitrile-[TBA]2[WO4] mixture and mechanism of [P4442]2[Hy]-catalyzed reaction of CO2 and 2-aminobenzonitrile (b)[41] |
NMR谱学具有制样简单、 测试便捷、 分辨率高等优点, 其谱学信号直接反映了ILs和反应底物周围微观环境, 可用于表征ILs与底物之间的相互作用信息, 在探究ILs催化CO2和邻氨基苯腈反应机理中发挥了重要作用。 由于个别元素的NMR信号灵敏度低、 原位检测难度大、 信号容易受氘代试剂种类和样品浓度等因素影响, 在一定程度上制约了NMR手段在反应机理研究中的应用。 随着NMR测试技术的发展和完善, 将在探究化学反应机理中显示出更大应用价值[43]。
IR光谱是基于分子对特定波长红外辐射的吸收而进行分子结构分析的一种谱学技术, 其吸收峰强度和位置与化学键强度和振动方式相关, 主要受分子内部结构因素(如电子效应、 空间效应和分子内氢键效应等)和外部因素(如物态、 溶剂效应、 分子间相互作用等)的影响[44, 45]。 因此, IR光谱能灵敏地反映出物质的特征官能团之间的相互作用信息, 已成研究化学反应机理的有效手段之一。 例如, ILs催化CO2与邻氨基苯腈反应时, ILs化学吸收CO2后新形成C=O和C— O等官能团, 会在中红外区域(4 000~400 cm-1)出现特征吸收峰, 这为确定反应机理提供了有力证据。 目前研究ILs催化CO2与邻氨基苯腈反应机理时, 常采用离线傅里叶变换红外光谱(FTIR)和在线原位红外光谱(in-situ FTIR)两种手段。
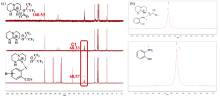
离线FTIR光谱(4 000~400 cm-1)具有灵敏度高、 测试快捷、 不需要额外添加溶剂等优势, 最常用于确定ILs与CO2、 邻氨基苯腈的相互作用。 例如, Liu等比较了[HTMG][Suc]在吸收CO2前后的FTIR光谱, 发现[Suc]-阴离子与CO2作用后在1 612和1 709 cm-1处出现了两个新吸收峰, 分别归属于新形成的碳酸盐(O— COO-)和氨基甲酸酯(N— COO-)中C=O的反对称伸缩振动[图7(a)], 表明[Suc]-阴离子具有活化CO2的性能[31]。 同时, 结合邻氨基苯腈-[HTMG][Suc]体系1H NMR中— NH2化学位移向低场移动[图7(b)], 作者提出了[HTMG][Suc]的阴、 阳离子通过氢键作用共同活化了邻氨基苯腈的— NH2并使其去质子化形成反应中间体, 同时该中间体亲核进攻被阴离子活化的CO2并形成新的反应中间体, 新中间体再依次经过分子内亲核成环、 重排和质子转移, 最终生成产物并重生得到ILs[31]。
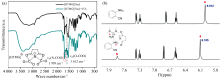 | 图7 [HTMG][Suc]吸收CO2前、 后的FTIR(a)和邻氨基苯腈-[HTMG][Suc]体系1H NMR(b)[31]Fig.7 FTIR spectra of [HTMG][Suc] before and after CO2 absorption (a) and 1H NMR spectra of 2-aminobenzonitrile-[HTMG][Suc] mixture (b)[31] |
Ping等比较了[HTMG][m-AP]-DMF体系通入CO2前、 后的FTIR谱图, 发现后者在1 795 cm-1处出现了一个新吸收峰, 归属于CO2与DMF的N原子发生相互作用后形成的C=O的反对称伸缩振动, 并确定溶剂DMF也参与了CO2的活化[29]。 Zhu等采用FTIR光谱研究[Choline][4-H-PhO]催化CO2和邻氨基苯腈反应机理时, 重点考察了纯[Choline][4-H-PhO]、 纯邻氨基苯腈以及邻氨基苯腈-[Choline][4-H-PhO]体系的FTIR光谱图, 结果显示[Choline][4-H-PhO]与邻氨基苯腈混合后, 纯邻氨基苯腈中位于3 500~3 150 cm-1处的N— H伸缩振动尖锐双峰明显变宽, 表明阴离子与— NH2发生了强氢键作用[46]; 同时, 纯邻氨基苯腈位于2 207 cm-1处的C≡ N伸缩振动峰蓝移至2 211 cm-1, 推测— CN与[Choline]+阳离子中的— OH形成了弱氢键相互作用[46]。 因此, 作者认为[Choline][4-H-PhO]的阴、 阳离子同时活化了邻氨基苯腈的— NH2和— CN, 并提出了一个全新的反应机理: [4-H-PhO]-负责活化CO2和— NH2, [Choline]+则活化— CN, 被活化后的邻氨基苯腈和CO2发生亲核反应, 再经过分子内质子转移与重排, 得到产物并使ILs再生[46]。 上述结果表明, FTIR光谱是表征ILs与CO2、 邻氨基苯腈相互作用的有力工具。
不同于文献报道测量纯物质或单一固定组成的邻氨基苯腈-ILs体系的FTIR光谱[29, 30, 31, 46], 本课题组重点关注邻氨基苯腈-[P4442][1-MHy]体系的FTIR光谱随ILs摩尔分数的变化[47], 发现随着ILs摩尔分数从0增加至0.41, 位于3 462和3 367 cm-1处邻氨基苯腈— NH2的N— H伸缩振动峰强度逐渐减小并伴随波数的红移和峰型由尖峰变为宽峰, 而2 212 cm-1处邻氨基苯腈— CN的C≡ N伸缩振动峰仅强度减弱而波数和峰型却均保持不变, 由此初步确定[1-MHy]-阴离子与邻氨基苯腈— NH2形成了强氢键作用, 且[1-MHy]-阴离子不与— CN直接作用[图8(a)]。 为了深入研究[P4442][1-MHy]催化CO2与邻氨基苯腈的反应机理, 本课题组还测定了不同时间时反应体系的FTIR光谱[图8(b)]。 结果表明, 3 478和3 371 cm-1处邻氨基苯腈的— NH2吸收峰强度随着反应进行逐渐减弱并转变为单峰, 并伴随着2 212 cm-1处— CN吸收峰强度的减弱以及1 714 cm-1 处新峰的出现和强度的增加, 这表明邻氨基苯腈的— NH2直接与ILs作用并转变成了— NH(仲胺), 同时邻氨基苯腈的— CN 和CO2共同参与了反应并形成了新C=O, 由此明确了[P4442][1-MHy]催化CO2与邻氨基苯腈的反应机理[47]。 上述结果表明, 分析邻氨基苯腈-ILs体系的FTIR光谱随体系浓度的变化以及比较不同时间时反应体系的FTIR光谱, 能有更全面获取相互作用信息, 有助于精确推测反应机理。
由于离线FTIR光谱易受取样、 温度、 压力等因素影响, 谱学信号未能完全反映实际反应过程中分子间相互作用信息, 故具有实时在线功能的in-situ FTIR光谱被逐渐应用于监测化学反应过程[48, 49, 50], 其最大优点是能够清晰地实时记录反应过程中物质的分子结构随时间的变化[51], 且红外探头具有测温功能, 从而更加精确地确定反应机理。 目前, in-situ FTIR光谱已经推广研究ILs催化CO2与邻氨基苯腈反应机理。
Yu等以[Et4N]3[CYA]为催化剂和DMSO为溶剂, 研究了CO2与邻氨基苯腈反应, 并采用in-situ FTIR光谱监控了CO2鼓入[Et4N]3[CYA]-DMSO体系时吸收峰的变化, 发现在1 705和1 680 cm-1出现了属于C=O的新谱带, 再结合离线FTIR和13C NMR确定了[CYA]3-阴离子与CO2之间存在着化学相互作用, 通过形成氨基甲酸酯来活化CO2并与邻氨基苯腈反应[50]。 虽然作者采用in-situ FTIR光谱来确定ILs与CO2之间的相互作用, 但他们并未进一步使用in-situ FTIR来实时监控整个反应进程及进行反应机理探究。
本课题组最近采用in-situ FTIR光谱监测了[P4442]2[Hy]催化CO2与邻氨基苯腈反应, 重点分析了反应体系的吸收峰波数和强度随反应时间的变化, 发现1 716 cm-1处的吸收峰强度随反应进程先迅速增强后逐渐下降直至平衡, 该峰归属于[Hy]2-阴离子活化CO2后新形成的C=O 同时1 635 cm-1处归属于N— H弯曲振动峰的强度随反应进程先缓慢下降后略有增加直至平衡, 这归因于[Hy]2-阴离子与N— H之间的氢键作用[40]。 上述结果表明, [Hy]2-阴离子同时活化了CO2和邻氨基苯腈的— NH2。 此外, 1 571 cm-1处归属于邻氨基苯腈芳环骨架振动峰的强度随反应呈现先快速下降后略有增加直至平衡[图9(a)], 这说明芳环上的— CN和— NH2均参与了反应, 形成新基团的同时改变了芳环的电子云密度。 最后, 本课题组还发现in-situ FTIR光谱检测的温度随反应出现先下降后上升的趋势, 而且温度极小值拐点所对应的时间与1 716、 1 635和1 571 cm-1三个吸收峰极值点对应的时间基本一致[图9(b)], 表明反应体系中可能存在中间体, 且中间体的形成是吸热过程, 而中间体转化为产物为放热过程。 基于in-situ FTIR光谱提供的信息, 本课题组结合DFT计算验证了[P4442]2[Hy]催化CO2与邻氨基苯腈反应可能的中间体结构, 并提出了新的反应机理[40]。 上述结果表明, in-situ FTIR光谱在监控反应过程和推测反应中间体方面具有更加显著的优势。
 | 图9 [P4442]2[Hy]催化 CO2和邻氨基苯腈反应的in-situ FTIR[40] |
总之, 无论是离线FTIR还是in-situ FTIR光谱, 它们在谱学原理和解析方法是相同的, 并且在研究ILs催化CO2和邻氨基苯腈反应机理时, 均是借助吸收峰强度和位置的变化来获得反应过程所涉及的相互作用信息[52]。 两者最大的区别为in-situ FTIR光谱是将红外探头直接伸入反应体系实时采集吸收峰信息, 从而提供比离线FTIR光谱更加客观、 精准反映体系微观相互作用的谱学信号[53]。 然而, in-situ FTIR光谱的红外探头的材质一般为金刚石, 其在3 500~1 900 cm-1范围存在着宽吸收峰, 这与ILs催化CO2和邻氨基苯腈反应体系的某些官能团如邻氨基苯腈的N— H和C≡ N的伸缩振动吸收峰重叠, 不利于后续相互作用分析和反应机理研究, 需要借助离线FTIR和15N NMR等谱学进行辅助佐证。 因此, 在研究化学反应机理时, NMR和IR等谱学方法应相互配合, 并结合DFT计算和分子动力学模拟等理论方法[54, 55], 发挥各种方法的优势、 取长补短。 此外, 也要发挥二维NMR和IR等手段在研究分子间相互作用和分子精细结构中的优势[56, 57], 使谱学方法成为研究化学反应机理的最有力工具。
NMR和IR能有效表征ILs与CO2或邻氨基苯腈之间的相互作用信息, 从分子层面揭示ILs催化CO2化学转化的本质原因, 在研究ILs催化CO2与邻氨基苯腈反应机理、 构建ILs结构与催化性能的构效关系中发挥了重要作用。 归纳总结NMR和IR技术研究ILs催化CO2与邻氨基苯腈反应机理取得的进展, 不仅有利于阐明ILs有效催化CO2化学转化的作用机制, 而且能进一步拓展NMR和IR等谱学技术在研究分子间相互作用和化学反应机理中的应用。 随着NMR和IR谱学技术发展和人工智能技术在图谱解析与识别方面的应用, 有望将二维NNR和IR等谱学技术推广至获得更精细的分子结构和相互作用信息、 确定催化剂与底物的相互作用位点与类型, 并将二维NMR和IR谱学与DFT计算、 分子动力学模拟等深度结合, 从而开启NMR和IR在研究复杂化学反应机理的新发展。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|