作者简介: 彭姣玉,女, 1985年生,中国科学院青海盐湖研究所重点实验室及研发中心副研究员 e-mail: pengjy@isl.ac.cn
我国青藏盐湖以富含硼锂而著称, 卤水中硼化学赋存状态随湖水化学类型的不同而发生变化, 其中以硫酸盐型盐湖卤水中硼酸盐的存在形式变化最为复杂, 卤水蒸发过程一般不以固体盐形式结晶析出, 而是以多硼物种形式富集于氯化镁饱和老卤中, 表现出严重的过饱和性, 对后续锂盐和镁盐的分离提取影响较大。 开展盐湖卤水体系中硼酸盐化学形态、 分布规律及离子间作用机制等溶液化学研究对盐湖资源高效开发具有重要的意义。 相比常规拉曼光谱技术, 拉曼积分球基于拉曼散射原理可极大地提高激发光的使用效率和拉曼散射信号, 对硼酸盐溶液结构检测具有拉曼响应信号强、 检出限低、 信噪比高等优点, 为盐卤复杂体系硼酸盐化学形态的定量分析奠定了基础。 利用拉曼积分球开展了盐湖卤水硼酸盐化学形态研究, 阐述了卤水蒸发过程多硼酸根离子的变化规律; 同时借助响应曲面法进行实验设计与优化, 建立了共存盐类干扰回归模型用于盐湖卤水中单硼物种B(OH)3的准确测定。 结果表明, 盐湖卤水浓缩过程中硼不断聚合生成多聚度硼酸根离子如B3O3(OH
Qinghai-Tibet salt lakes are famous for enriching boron and lithium resources. Nevertheless, the chemical species of borate in the brine varies with the chemical type of salt lake. Among them, the existing borate forms in sulfate-type salt lake brine are the most complicated. Generally, the borates do not crystallize out from the brine during the whole evaporation process of brine but accumulate in the bischofite-saturated brine in different kinds of boron species, which are supersaturated with magnesium borates. This phenomenon may significantly impact the subsequent separation and extraction of lithium and magnesium salts. Therefore, the deep research on the chemical forms, species distribution, and their interactions in the salt lake brine is of great significance for the highly efficient development of salt lake resources. Compared with the classical Raman spectroscopy, the simplified Raman integrating sphere, designed based on the Raman scattering principle, can improve the exciting light's efficiency and the Raman scattering signal. It is characteristic of a strong Raman scattering signal, low detection limit, and high signal-to-noise ratio for the characterization of the borate structures, which favors the quantitative analysis of the chemical forms of the borate in the complicated brine system. Based on the above, this study aimed to investigate the chemical forms of borate in salt lake brine using the Raman integrating spheres. It also elucidated the changes of polyborate ions during the brine evaporation process. Secondly, the response surface method was used to explore the effects of the coexisting salts on the determination of B(OH)3 in salt lake brine. The results showed that borates in the salt lake brine could be polymerized to form poly borate ions such as B3O3(OH
青藏高原分布有众多含硼盐湖, 其湖水类型可分为碳酸盐型、 硫酸盐型和氯化物型三大类[1]。 硫酸盐型盐湖卤水中硼的存在形式最为复杂, 湖底沉积的硼酸盐矿物储量大, 种类多。 研究表明[1, 2], 硫酸盐型盐湖卤水蒸发过程硼酸盐一般不以固体盐形式析出, 而是随盐类的浓缩富集而发生复杂的聚合、 缔合等作用, 以四硼酸镁(MgO· 2B2O3)的 “ 综合统计” 形式赋存于氯化镁饱和老卤中, 存在极大的过饱和性, 对硼和其他盐类尤其是锂盐和镁盐的分离提取影响较大。 近年来, 我国高镁锂比盐湖提锂技术得到持续突破[3, 4], 以膜分离技术为代表进行卤水提锂得到了规模化应用。 然而, 盐湖卤水中硼锂伴生, 不同条件下多硼物种的动态转化会降低膜分离技术对硼的选择性, 影响硼锂分离效率, 进而增加后续锂盐产品生产过程的除硼成本, 同时, 膜表面富集的多聚硼酸根离子可与镁离子生成难溶盐, 易产生膜污染, 影响膜使用寿命。 因此, 开展盐卤体系硼酸盐物种分布及作用机制等溶液化学研究对硼锂高效分离具有的重要意义。
溶液中硼物种的化学形态分布规律是揭示不同条件下离子作用机理、 微观水合结构信息的重要途径之一。 文献报道硼酸盐溶液中的硼物种分布计算主要有两种方法, 一种是利用溶液中硼酸分子生成其他硼酸根阴离子的化学平衡常数, 通过物料平衡并结合牛顿迭代法计算给出不同硼物种的浓度分布规律。 20世纪70年代, Hirao等[5]利用不同硼酸根阴离子的化学平衡常数和总硼浓度计算给出了不同pH条件下B(OH)3溶液中各种硼物种包括B(OH)3、 B(OH)
由于硼酸盐溶液中多硼物种的复杂性, 目前利用热力学计算仍很难适用于盐湖卤水复杂体系中硼络阴离子的物种分布计算, 这也导致天然卤水体系中硼酸盐化学形态的定量化研究鲜有涉及, 仍停留在四硼酸盐(MgO· 2B2O3) “ 综合统计” 形式的定性层面, 无法确定溶液中硼络阴离子的化学分布及作用关系。 Raman光谱具有原位、 无损、 水峰干扰小等特点, 一直是研究硼酸盐溶液结构化学的最有效实验手段。 用于结构的定性分析的同时还可对特征硼络阴离子进行定量识别分析。 正硼酸(B(OH)3)是水环境(地下水、 盐湖卤水、 油气水等)中硼的主要形态之一, 既是地壳演化过程中硼元素的主要迁移形态, 也是盐湖卤水中参与聚合作用转化成其他多聚硼酸根阴离子的原始组分, 在硼酸盐地球化学和溶液化学领域中占有重要地位。 本工作利用拉曼光谱开展了盐湖卤水硼酸盐化学形态研究, 同时借助响应曲面法进行实验设计与优化, 利用拉曼积分球研究了盐湖卤水中共存盐类(如NaCl、 MgCl2、 MgSO4和KCl等)对B(OH)3定量分析的影响, 建立相应的回归关系式, 对盐湖卤水中B(OH)3化学形态进行了准确定量分析。 该研究结果可为后续利用光谱实验与模拟计算联用技术开展盐卤体系硼酸盐溶液物种分布及作用机制研究提供新思路和技术支撑。
赛默飞激光显微拉曼光谱仪(DXR, 美国), 拉曼积分球光谱仪(深圳海纳光有限公司, 研制), 优普超纯水机(UPH-I-60L, 18 MΩ ), 梅特勒pH多参数测定仪(S220-K), 赛多利斯电子天平(BSA224S-CW)。 盐湖卤水取自柴达木盆地大柴旦盐湖, 实验主要试剂见表1。
| 表1 实验主要试剂 Table 1 Reagents used in experiments |
DXR激光显微拉曼光谱仪: 用于卤水Raman定性分析, 激光波长532 nm, 光谱范围300~950 cm-1, 输出功率10 mW, 狭缝宽度50 μ m, 曝光时间20 s, 曝光次数20次, 分辨率3 cm-1。
拉曼积分球仪: 用于进行卤水Raman定量分析, 激发波长532 nm, 光谱范围200~2 200 cm-1, 输出功率500 mW, 狭缝宽度100 μ m, 曝光时间1 s, 曝光次数180次, 分辨率3 cm-1, 光栅1 800线。
采用毛细玻璃管用于卤水Raman定性检测, 定量分析则采用一次性塑料移液器移取一定体积待测液滴入聚四氟乙烯样品池, 放置拉曼积分球光路上进行拉曼测试, 每个样品平行测定2次, 以得到准确结果。
称取重结晶硼酸固体配置一定浓度硼酸溶液, 并逐级稀释配置系列低浓度硼酸水溶液, 加入分析纯盐酸调节pH< 5, 定容。 溶液中硼酸浓度采用甘露醇化学滴定法测定, 分析浓度分别为0.00、 1.02、 2.04、 3.05、 4.07、 5.09和6.11 g· L-1, 分析相对误差< 0.5%, 以不含硼酸的水溶液作为空白扣除基底, 采用偏最小二乘法进行基线校正、 特征峰寻峰等预处理。 以H2O在1 640 cm-1处的O— H弯曲振动峰做参比, 进行拉曼定量分析、 绘制曲线。
不同浓缩阶段卤水中共存盐类浓度、 种类对硼酸根离子的拉曼定量检测具有较大的干扰, 主要表现为拉曼基线漂移、 特征峰重叠以及强度响应值偏低等, 影响拉曼的准确定量分析。 采用响应曲面法进行多水平实验设计, 建立干扰模型以消除盐类的干扰。
以原始卤水和2.5倍浓缩氯化钠饱和卤水为参考对象, 利用Minitab17响应曲面中心复合实验设计进行分析, 重点研究NaCl、 KCl、 MgCl2和MgSO4等主要共存盐对硼酸拉曼定量检测的影响。 因子设计水平见表2, 开展5因子5水平1/2正交实验, 其中分辨度为IV, 基础次数32次, 区组为2, 中心点12, 水平从高到低依次标记为: +2、 +1、 0、 -1、 -2, 共64组实验。
| 表2 响应曲面实验因子及水平设定 Table 2 Level setting for the response surface experiment |
对大柴旦原始卤水进行蒸发浓缩, 结晶析盐规律依次为: 石盐(NaCl), 泻利盐(MgSO4· 7H2O)、 光卤石(KCl· MgCl2· 6H2O)和水氯镁石(MgCl2· 6H2O), 对应液相组分含量如表3所示。 原始卤水中氯化钠含量为289.25 g· L-1, 处于饱和状态, 硼含量(以MgB4O7计)为1.47 g· L-1, 蒸发浓缩过程, 液相中硼浓度随卤水浓缩而不断被富集, 最终赋存于氯化镁饱和盐卤中, 对应MgB4O7含量为62.52 g· L-1(DL4), 进一步浓缩结晶析出水氯镁石, MgB4O7的浓度为85.44 g· L-1, 卤水成粘稠状态, 停止蒸发。
| 表3 大柴旦盐湖卤水浓缩过程液相各组分含量 (g· L-1) Table 3 Contents of salts in the brine of Da Qaidamsalt lake during evaporation process |
不同蒸发浓缩阶段对应液相Raman光谱分析如图1(a)所示, 据文献[17]报道, 多硼酸根离子的Raman峰波数范围为400~1 000 cm-1, 由于卤水中共存
 | 图1 大柴旦盐湖卤水不同蒸发阶段液相多硼酸根离子Raman光谱变化规律(a)及其Lorentz多峰曲线拟合(b, c)Fig.1 Raman spectra of borates in Da Qaidam salt lakebrine during evaporation process (a) and its Lorentz multi-peak fitting (b, c) |
| 表4 大柴旦盐湖卤水浓缩过程液相中多硼酸根离子Raman振动光谱归属 Table 4 Assignments of Raman spectrum of borates in the Da Qaidamsalt lake brine during evaporation process |
由图1(b, c)、 表4可知, 在400~950 cm-1之间, 卤水中共存
(1)原始卤水中, 876和744 cm-1处谱峰表明, 硼的主要存在形态为B(OH)3和B(OH)
(2)随着卤水不断浓缩富集, 在630 cm-1附近出现B6O7(OH)
(3)氯化镁饱和老卤中, 由于硼的浓缩富集以及泻利盐的结晶析出, 卤水中630 cm-1附近的B6O7(OH
硫酸镁亚型含硼盐湖卤水动态浓缩过程中硼可通过聚合生成高聚合度硼酸根离子赋存于氯化镁饱和老卤中。 卤水中硼的化学形态变化规律与MgCl2-MgO-2B2O3-H2O体系中[20]硼物种变化一致, 但与钠、 钾、 锂的碱金属溶液体系[6, 7, 8, 9, 10]物种变化关系差别较大。 利用现有文献报道的硼酸根离子化学平衡常数计算碱土金属浓盐溶液体系硼化学物种分布将会存在较大的偏差, 故需深入开展Raman光谱等定量分析技术研究。
2.2.1 响应曲面分析
响应曲面优化实验中不同盐类溶液中B(OH)3的Raman光谱见图2(a), 根据系列硼酸标准曲线[图2(b)], 求得盐水溶液中B(OH)3的分析相对误差见表5。
 | 图2 响应曲面法实验设计Raman光谱(a)及硼酸标准曲线(b)Fig.2 Raman spectra of the response surface experiments (a); and the standard curve of B(OH)3 in solution (b) |
| 表5 响应曲面实验设计及结果 Table 5 The design and results of the response surface experiment |
由表5可知, 实验结果相对误差较大(-45.76%~0%), 表明盐水溶液中共存盐类对B(OH)3的拉曼定量测定存在显著干扰, 需建立干扰模型消除影响。 以各因子NaCl (B)、 MgCl2 (C)和MgSO4 (D)和KCl (E)浓度为响应变量, B(OH)3浓度测定值为因变量得到回归模型如式(1):
B(OH)3(Raman测定值)=0.029+0.893A+3.89× 10-4B+3.02× 10-3C-1.10× 10-2D+1.76× 10-2E+1.39× 10-2A2+5.0× 10-6B2+2.14× 10-4C2+3.45× 10-4D2-1.53× 10-3AB-3.06× 10-3AC+5.56× 10-3AD-5.20× 10-5BD-1.37× 10-3CE (1)
拟合相关系数为99.52%, 对回归方程式(1)进行方差分析, 结果见表6。 由概率水平p值(< 0.05), 共存盐类NaCl的影响最显著, 其次为MgSO4和MgCl2, 且盐类之间存在显著的交互作用, 原因如下:
| 表6 响应曲面实验方差分析 Table 6 Variance analysis of theresponse surface experiment |
(1)溶液中加入共存盐将会导致1 640 cm-1处H2O的O— H弯曲振动峰形和峰强发生变化, 液态水氢键作用受到一定程度破坏, 浓度越大, 影响越明显[16]。
(2)实验中氯化钠浓度接近饱和, 溶液粘稠度大, 自由水分子减少, 硼酸与水分子之间的氢键作用变化, 拉曼光谱特征峰表现为: 878 cm-1处B(OH)3的特征峰面积和峰强降低, 而1 640 cm-1处H2O的弯曲振动峰面积和峰强增大, 即硼酸与水峰面积比值(
(3)溶液中MgSO4浓度与MgCl2浓度相近, 但其影响更明显, 主要因
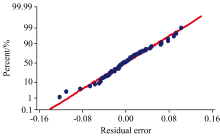
图3为回归残差的正态分布图, 实验数据点基本均匀地分布在一条直线上, 符合正态分布, 表明该回归方程拟合度较好。 为验证该回归模型的准确性, 分别对加入市售2.00和4.00 g· L-1硼酸标准溶液的模拟卤水进行Raman定量分析, 结果如表7所示。 经干扰模型校正后, 硼酸Raman定量检测的相对误差绝对值小于2%, 即测定结果准确度较高。
| 表7 模拟卤水体系中B(OH)3 Raman定量分析(g· L-1) Table 7 Raman quantitative analysis of B(OH)3 in the system of simulated brine (g· L-1) |
2.2.2 盐湖浓缩卤水中总硼浓度定量检测分析方法比较
为检验Raman定量技术对卤水总硼浓度的准确测定, 分别对原始卤水、 2.5倍浓缩卤水中的总硼浓度进行化学滴定、 Raman定量检测和平衡常数牛顿迭代计算分析。 由文献[21]可知, 硼酸盐溶液中当pH小于5时, 硼以B(OH)3形式存在, 而pH大于12.5时呈B(OH
实验中, 原始卤水和2.5倍浓缩卤水的pH分别为7.50和7.14, 化学分析总硼浓度为0.032 8和0.077 3 mol· L-1, 表明卤水中硼物种分布除B(OH)3和B(OH)
利用Matlab软件, 以文献[22]报道298.15 K时5 mol· L-1 NaCl介质中的不同硼物种的平衡常数值为参数进行牛顿迭代计算, 计算如式(2)
ctotal, B=[B(OH)3]+K11[B(OH)3]/[H+]+3K31[B(OH)3]3/[H+]+K32[B(OH)3]3/[H+]2+4K42[B(OH)3]4/[H+]2+5K51[B(OH)3]5/[H+] (2)
式(2)中, K11、 K31、 K32、 K42、 K51分别为B(OH)
图4为原始卤水和2.5倍浓缩氯化钠饱和卤水以及加盐酸后的Raman光谱, 图中981 cm-1处为
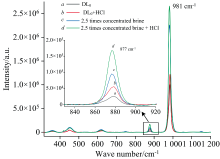 | 图4 不同浓缩卤水及加酸调节pH后Raman光谱Fig.4 Raman spectra of the brine before and after the hydrochloric acid addition |
| 表8 大柴旦盐湖卤水酸化后总硼浓度分析方法比较(g· L-1) Table 8 Analysis comparison of boron concentration in Da Qaidam brine after acidification (g· L-1) |
由表8可知, 当加酸调节卤水pH至强酸性以后(pH< 3), 可认为卤水中的硼物种只有B(OH)3分子一种形态, 牛顿迭代法计算的B(OH)3分子浓度等于总硼浓度, 即化学滴定分析的总硼浓度值; 经Raman干扰模型校正后, 加酸后的原始卤水和2.5倍浓缩卤水中总硼浓度含量与滴定分析值的相对误差绝对值小于4%, 测定结果较准确, 表明Raman定量检测技术可用于卤水总硼浓度的准确测定。
2.2.3 盐湖浓缩卤水中单硼物种B(OH)3分子形态的定量分析
以所建立的Raman定量分析技术, 对原始卤水和2.5倍浓缩卤水中的单硼物种B(OH)3分子进行分析检测, 并探究其变化规律, 结果见表9。
| 表9 大柴旦盐湖卤水中B(OH)3分子定量分析(g· L-1) Table 9 Quantitative analysis of B(OH)3 in Da Qaidam brine (g· L-1) |
平衡常数牛顿迭代法的计算值与Raman光谱法检测的B(OH)3分子含量相差甚远, 且浓缩过程计算所得B(OH)3分子比例并未发生变化, 分析认为由于牛顿迭代计算过程以5 mol· L-1 NaCl介质中的平衡常数、 卤水总硼浓度和测定pH为参考依据, 以离子浓度代替活度处理, 并未考虑其他共存盐类对平衡常数和活度的影响, 导致计算值偏差较大; 当平衡常数一定时, 溶液pH的变化对计算结果存在显著的影响。 由表8可知, 当加酸调节卤水呈强酸性以后(pH< 3), B(OH)3分子含量完全受酸度控制, 其含量占比均为100%。 实验中卤水测定pH为表观pH, 与理论H+浓度存在一定偏差, 且原始卤水与2.5倍浓缩卤水的pH差距不大, 这也导致计算过程中B(OH)3含量占比基本不变。 利用平衡常数牛顿迭代法进行盐湖卤水硼物种分布计算时存在较大的偏差, 有必要建立相关定量分析技术。
由表9可知, Raman回归模型校正后卤水中B(OH)3含量分别占总硼浓度的59.25%和43.72%, 表明原始卤水中接近40%的硼以B(OH)
针对盐卤体系中硼物种分布计算过程中存在较大偏差的问题, 开展了拉曼光谱技术定量分析盐湖卤水硼酸盐化学形态研究, 借助响应曲面法进行实验设计与优化, 建立了共存盐类干扰回归模型用于盐湖卤水中单硼物种B(OH)3的准确测定, 相对误差小于5%, 阐明了蒸发浓缩过程中B(OH)3物种分布的变化规律, 从定量视角初步阐述了卤水富集过程硼氧配阴离子间的聚合作用关系, 为后续盐卤体系硼酸盐溶液物种分布及作用机制研究提供实验依据和理论指导。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|