作者简介: 张 璇,女, 1996年生,福州大学材料科学与工程学院分子材料与工程系硕士研究生 e-mail: 790854468@qq.com
稀土上转换纳米粒子(UCNPs)因其具有毒性小、 化学稳定性好和背景荧光低等优点被用于构建荧光纳米传感器。 通过溶剂热法制备核壳UCNPs, 采用柠檬酸钠对其进行表面配体交换得到水溶性核壳UCNPs(Cit-CS-UCNPs), 以Cit-CS-UCNPs作为荧光传感器的能量供体, 二氧化锰(MnO2)纳米片作为荧光传感器的能量受体, 采用荧光共振能量转移(FRET)机理, 构建了一种用于食品添加剂二氧化氢(H2O2)和叔丁基对苯二酚(TBHQ)检测的荧光纳米传感器(Cit-CS-UCNPs-MnO2)。 通过扫描电镜(SEM)、 荧光光谱和紫外可见吸收光谱(UV-Vis)等分析测试手段对制备的纳米材料的形貌结构和性能进行表征。 考察了猝灭剂浓度、 孵育温度及孵育时间等实验条件对荧光传感体系检测性能的影响。 荧光光谱和UV-Vis实验结果表明, Cit-CS-UCNPs最大发射峰位于654 nm, Cit-CS-UCNPs与MnO2结合后, 核壳UCNPs发生荧光猝灭, 当存在H2O2时, Cit-CS-UCNPs的荧光恢复, 说明在此波段H2O2与MnO2纳米片发生氧化还原反应, MnO2纳米片被还原成Mn2+, 逐渐从Cit-CS-UCNPs的表面解离下来; 存在TBHQ时, Cit-CS-UCNPs-MnO2与TBHQ体系峰位与TBHQ偏移到253 nm, 为TBHQ与MnO2纳米片发生氧化还原反应, 使得Cit-CS-UCNPs-MnO2体系中FRET效应减弱, 荧光强度回升。 SEM结果表明, MnO2纳米片均匀包覆在Cit-CS-UCNPs的周围, 在水中仍可保持良好的分散性, 表明MnO2纳米片修饰到Cit-CS-UCNPs表面。 对猝灭剂高锰酸钾(KMnO4)的浓度进行了优化。 结果表明, 当KMnO4浓度为10 mol·L-1时, 猝灭效率可达90%。 对检测条件进行优化, 结果表明H2O2的检测孵育时间为25 min时, MnO2和H2O2之间氧化还原反应基本完全, Cit-CS-UCNPs-MnO2荧光恢复值最大; TBHQ的检测孵育时间为30 min。 在最佳实验条件下, Cit-CS-UCNPs-MnO2的荧光强度变化比率与H2O2浓度(0~1 000 μmol·L-1)及TBHQ浓度(0~0.6 mmol·L-1)分别具有良好的线性关系。 保持最佳实验条件, 选取食品中存在的代表性金属离子(如K+、 Na+、 Ca2+和Mg2+)和常见的食品添加剂苯甲酸(BA)、 D-葡萄糖(Glu)、 山梨酸钾(PS)、 蔗糖(Suc)、 纳他霉素(Nat)和肌醇(Ino)作为研究对象进行选择性测试, 发现与H2O2相比, Cit-CS-UCNPs-MnO2对其他添加物质没有强烈的反应, 传感器整体荧光信号波动不大, 因此Cit-CS-UCNPs-MnO2对H2O2和TBHQ可进行特异性检测。
Rare earth up-conversion nanoparticles (UCNPs) have been used to construct fluorescent nanosensors because of their low toxicity, good chemical stability, and low background fluorescence. Core-shell UCNPs were prepared using the solvothermal method, and water-soluble core-shell UCNPs (Cit-CS-UCNPs) were obtained by surface ligand exchange with sodium citrate. The Cit-CS-UCNPs were used as the energy donor of the fluorescence sensor, and manganese dioxide (MnO2) nanosheets were used as the energy receptor of the fluorescence sensor. Based on the fluorescence resonance energy transfer (FRET) mechanism, a fluorescence nanosensor (Cit-CS-UCNPs-MnO2) was constructed for the detection of hydrogen dioxide (H2O2) and tert-butylhydroquinone (TBHQ) as food additives. The prepared nanomaterials' morphology, structure, and properties were characterized by scanning electron microscopy (SEM), fluorescence spectrum, and ultraviolet spectrum (UV-vis). The effects of quenching agent concentration, incubation temperature, and incubation time on the detection performance of the fluorescence sensing system were investigated. According to the fluorescence spectra and UV-Vis experimental results, the maximum emission peak of Cit-CS-UCNPs is 654 nm. After the combination of Cit-CS-UCNPs and MnO2, core-shell UCNPs undergo fluorescence quenching. When H2O2 is present, the fluorescence of Cit-CS-UCNPs recovers. The results indicate that H2O2 and MnO2 nanosheets undergo redox reaction at this band, and MnO2 nanosheets are reduced to Mn2+, which gradually dissociates from the surface of Cit-CS-UCNPs. In the presence of TBHQ, the peak of the Cit-CS-UCNPs-MnO2 and TBHQ system was shifted to 253 nm, indicating that the redox reaction occurred between TBHQ and MnO2 nanosheets, and the FRET effect was reduced in the Cit-CS-UCNPs-MnO2 system, and the fluorescence intensity increased. It can be seen from the SEM results that MnO2 nanosheets are uniformly coated around Cit-CS-UCNPs, and maintain good dispersion in water, indicating that MnO2 nanosheets are modified on the surface of Cit-CS-UCNPs. The concentration of the quencher potassium permanganate (KMnO4) was optimized, and the results showed that when the concentration of KMnO4 is 10 mol·L-1, the quenching efficiency can reach 90%. The detection conditions were optimized, and the results showed that when the incubation time of H2O2 was 25 min, the redox reaction between MnO2 and H2O2 was complete. The fluorescence recovery value of Cit-CS-UCNPs-MnO2 was the maximum. The incubation time of TBHQ was 30 min. Under the optimal experimental conditions, the fluorescence intensity of Cit-CS-UCNPs-MnO2 has a good linear relationship with the concentration of H2O2 (0~1 000 μmol·L-1) and TBHQ (0~0.6 mmol·L-1). The optimal experimental conditions were maintained, and representative metal ions (such as K+, Na+, Ca2+ and Mg2+) and common food additives (BA, Glu, PS, Suc, Nat and Ino) in food were selected as research objects. The results showed that compared with H2O2, Cit-CS-UCNPs-MnO2 did not react strongly to other added substances, and the overall fluorescence signal of the sensor did not fluctuate much. Therefore, it can be seen that Cit-CS-UCNPs-MnO2 can detect the specificity of H2O2 and TBHQ.
食品添加剂TBHQ是一种具有高抗氧化能力、 抗菌、 耐高温等优点的高效防腐剂, 主要用于油脂食品, 而当过量摄入TBHQ时, 轻则恶心或腹泻, 重则引发DNA损伤、 胃肿瘤或癌症等, 最大用量需小于0.2 g· kg-1 [1]。 H2O2是一种重要的化学氧化剂, 它具有出色的抗菌特性, 经常作为食品防腐剂添加入牛奶和奶酪中。 食品中残留过量的H2O2可能会对人体健康造成多种不利影响, 如加速衰老过程、 心血管疾病、 严重的肠胃问题、 神经退行性疾病、 癌症等[2], 食品包装中允许的H2O2残留量为29.4 μ mol· L-1[3]。 因此有必要开发一种低成本、 简单而灵敏的传感器用于快速检测食品中的TBHQ和H2O2。
目前一些方法已被用于检测H2O2和TBHQ, 包括气相色谱[4]、 傅里叶变换红外光谱[5]、 高效液相色谱[6]、 流注射分析[7]和电化学方法[8]等。 虽然这些传统方法大多准确灵敏, 但复杂过程、 耗时步骤、 大量试剂消耗和昂贵的仪器限制了其应用。 荧光法因其灵敏、 简单、 快速的优点而被广泛关注, 而该方法的检测效果取决于荧光材料的性能。 开发具有高光化学稳定性、 低潜在毒性和无背景光干扰的荧光材料在荧光传感领域具有重要意义。
具有上转换发光性能的稀土掺杂发光材料在许多领域的应用都得到了很好的研究, 如防伪技术领域[9]、 生物成像[10]、 药物输送、 检测[11]等。 针对食品添加剂的检测, UCNPs是分析检测传感器材料的理想选择。 Kumar[12]等使用Sm(TTA)3Phen和UCNPs制备的有机-无机杂化纳米粒子(HNPs), HNPs溶液中的H2O2能显著淬灭Sm3+的发光强度, 这一特性被用于H2O2的检测, 其最低检测限为8.6 μ mol· L-1。 Chen[13]等基于UCNPs的荧光会受邻苯二胺(OPD)影响发生淬灭的现象, 研制了一种用于H2O2含量测定的新型传感器。 测试结果表明, H2O2可在酸性溶液中将Fe2+转化为Fe3+和· OH, 随后生成的Fe3+和· OH可将OPD氧化, 导致UCNPs发光猝灭。 该传感器具有较好的灵敏度, 然而OPD具有较大的毒性。 Bao[14]等采用三羟甲基氨基甲烷与柠檬酸通过水热法合成含氮碳量子点(N-CQDs), 并基于Fe3+与N-CQDs的络合作用导致荧光猝灭, 借助TBHQ与Fe3+的强络合作用与CQDs产生竞争, 构建“ 关-开” 型荧光探针对TBHQ进行快速检测。 TBHQ的最低检测限为0.031 4 mmol· L-1。 针对这些荧光检测方法灵敏度不够、 具有毒性等缺点, 设计简单、 灵敏、 环保的荧光检测方法仍具有重要意义。
MnO2纳米片具有大的比表面积和宽波长范围的强光吸收能力, 是一种很有前景的荧光淬灭剂, 在开发“ 关-开” 荧光传感系统方面引起了广泛关注。 MnO2纳米片还可以被还原成Mn2+, 有益于环境和人类健康[15]。 本研究采用水溶性UCNPs作为荧光纳米传感器的能量供体, MnO2纳米片作为荧光纳米传感器的能量受体, 构建了Cit-CS-UCNPs-MnO2荧光传感器, 采用其荧光强度信号对检测液浓度的响应, 基于FRET验证了检测方法的可行性, 实现了对H2O2和TBHQ的特异性检测, 为荧光传感器在食品中H2O2和TBHQ的检测方面提供了一种有效方法。 所构建的检测方法具有更低的检测限, 更灵敏且使用的MnO2纳米片被还原后, 有益于环境和人类健康, 具有环保意义。
FluoroMax-4型荧光光谱仪(法国Horiba Jobin yvon公司); LAMBDA 950型紫外-可见近红外分光光度计(美国PerkinElmer有限公司); SUPRA 55型热场发射扫描电子显微镜(德国卡尔蔡司有限公司)。
2-(N-吗啉)乙磺酸(MES)、 叔丁基对苯二酚(TBHQ)、 高锰酸钾(KMnO4)(阿拉丁试剂上海有限公司); 过氧化氢(H2O2)、 氢氧化钠(NaOH)、 纳他霉素(Nat)、 山梨酸钾(PS)、 苯甲酸(BA)、 肌醇(Ino)、 D-葡萄糖(Glu)、 蔗糖(Suc)、 氯化钾(KCl)、 氯化钠(NaCl)、 氯化钙(CaCl2)、 氯化镁· 六水(MgCl2· 6H2O)(国药集团化学试剂有限公司)。 油酸(OA)、 氟化铵(NH4F)、 1-十八烯(ODE)(阿拉丁化学试剂有限公司)。
参照文献[16, 17]并做了少量修改, 制备合成了水溶性UCNPs: 将0.25 mmol的稀土氯化盐(ReCl3· 6H2O)加入到100 mL三颈烧瓶中, 加入6 mL OA和15 mL ODE溶液, 混合均匀。 在氩气气氛下, 以550 r转速磁力, 搅拌15 min, 排除空气。 再缓慢加热至160 ℃, 保温30 min, 使ReCl3· 6H2O完全溶解。 将反应液冷却至室温, 加入2 mL NaLiErF4∶ Tm裸核UCNPs的环己烷分散液, 反应30 min, 缓慢滴加10 mL溶有0.025 0 g NaOH和0.037 0 g NH4F的甲醇溶液, 于室温下保温30 min。 加热反应溶液至80 ℃, 保持30 min。 将混合溶液加热到300 ℃反应90 min。 待反应结束后, 将反应液冷却至室温, 经过离心、 体积比为1∶ 1的乙醇和环己烷混合液洗涤, 即可制得NaLiErF4∶ Tm@NaGdF4∶ Yb UCNPs, 保存于2 mL环己烷中。
称取二水合柠檬酸钠550 mg于100 mL三颈烧瓶中, 加入15 mL一缩二乙二醇和1 mL去离子水。 设置转速为600 r· min-1, 在氩气气氛下, 将混合物升温至110 ℃, 维持1.5 h, 待反应完全后, 冷却至室温。 取1 mL C@20% Yb3+环己烷分散液离心, 重新分散在1 mL氯仿和1 mL甲苯混合液中。 将混合分散液缓慢滴加到三颈烧瓶中, 升温至130 ℃, 持续30 min。 将溶液加热到175 ℃, 反应一段时间, 反应结束后使其冷却到室温。 最后加入体积比为1∶ 1的水和乙醇混合溶液进行离心洗涤, 收集产物, 分散在2 mL去离子水中。
将0.2 mL一定浓度的KMnO4水溶液和0.1 mL MES缓冲溶液依次加入到0.1 mL 4 mg· mL-1 Cit-CS-UCNPs的去离子水分散液中, 于室温下超声作用30 min, 将混合溶液离心, 经去离子水洗涤, 制备MnO2纳米片与Cit-CS-UCNPs-MnO2, 分散在1 mL去离子水中。
对H2O2进行检测步骤与Gu等[18]报道相似, 首先在一系列的2 mL离心管中, 分别加入0.1 mL Cit-CS-UCNPs-MnO2(0.4 mg· mL-1)的水分散液和一系列等体积(0.1 mL)不同浓度的H2O2水溶液, 将其置于水浴锅中孵育一段时间, 获得相应的检测液。 采用FluoroMax-4荧光光谱仪测试检测液的上转换发射强度。 依据检测液发射强度的变化实现对H2O2精准的检测。
Cit-CS-UCNPs-MnO2传感器用于TBHQ的检测步骤与1.4节一致。 检测溶液为0.1 mL Cit-CS-UCNPs-MnO2(0.4 mg· mL-1)的水分散液和一系列等体积(0.1 mL)不同浓度的TBHQ。
图1为Cit-CS-UCNPs-MnO2荧光纳米传感器用于检测H2O2的机理。 该传感器主要由两个部分组成能量供体Cit-CS-UCNPs和能量受体MnO2纳米片。 由于MnO2纳米片在300~700 nm具有宽泛的紫外吸收波段, 而所制备的核壳UCNPs在600~700 nm具有强烈的上转换发射, 最大发射峰于654 nm, 两者波段存在很好的重叠(见图2), 相互结合后会引发FRET过程, 导致核壳UCNPs荧光发生猝灭。 当分别存在H2O2和TBHQ时, H2O2和TBHQ与MnO2纳米片之间会产生氧化还原反应, MnO2纳米片被还原成Mn2+, 逐渐从Cit-CS-UCNPs的表面解离下来, Cit-CS-UCNPs的荧光恢复。 根据Cit-CS-UCNPs在654 nm处发生的荧光变化即可实现对H2O2和TBHQ的检测。
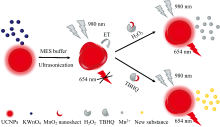 | 图1 Cit-CS-UCNPs-MnO2传感器用于检测H2O2和TBHQ的机理Fig.1 Mechanism diagram of the Cit-CS-UCNPs-MnO2sensor used to detect H2O2 and TBHQ |
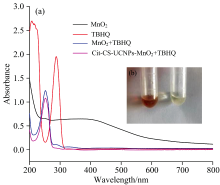
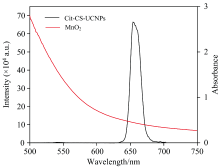 | 图2 Cit-CS-UCNPs的荧光发射光谱和MnO2的紫外-可见吸收光谱Fig.2 Fluorescence emission spectrum of Cit-CS-UCNPs and UV-Vis spectrum of MnO2 |
采用紫外-可见吸收光谱, 探究Cit-CS-UCNPs-MnO2传感器检测TBHQ的可行性。 将一定浓度的TBHQ加入Cit-CS-UCNPs-MnO2溶液中, Cit-CS-UCNPs-MnO2(654 nm)的荧光强度恢复。 由图3(a, b)可知, 当MnO2纳米片或Cit-CS-UCNPs-MnO2与TBHQ反应后, 测量反应溶液会在253 nm出现新的峰。 由此推测可能存在以下机理: TBHQ与Cit-CS-UCNPs-MnO2中的MnO2纳米片产生氧化还原反应, 生成新的物质, 使得MnO2纳米片分解, Cit-CS-UCNPs-MnO2体系中FRET效应减弱, 使得荧光强度回升, 具体生成产物还有待探究。 由图3(b)可以直观地发现, 在添加TBHQ后Cit-CS-UCNPs-MnO2分散液颜色由红棕色变为淡黄色, 进一步说明MnO2纳米片发生分解, 导致溶液颜色变浅。
图4(a)中MnO2纳米片是高锰酸钾水溶液和MES缓冲溶液超声作用得到的产物, 结合对应的能谱图[图5(a)]和元素映射图[图5(b)], 验证了在MES缓冲液的作用下, KMnO4可以被还原成无定形的MnO2纳米片。 图4(b)为Cit-CS-UCNPs-MnO2分散在水中的SEM图, 由图显示MnO2纳米片均匀包覆在Cit-CS-UCNPs的周围, 在水中Cit-CS-UCNPs-MnO2仍可保持良好的分散性好, 表明MnO2纳米片在Cit-CS-UCNPs的表面组装成功。
 | 图4 (a)MnO2纳米片和(b)Cit-CS-UCNPs-MnO2的SEM图Fig.4 SEM images of (a) MnO2 nanosheet and (b) Cit-CS-UCNPs-MnO2 |
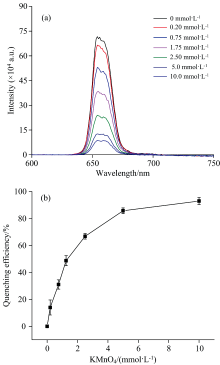
为了证明Cit-CS-UCNPs-MnO2荧光纳米传感器对H2O2和TBHQ的检测能力, 首先研究了MnO2纳米片是否会导致Cit-CS-UCNPs的荧光强度猝灭。 图6测试结果, 随着MnO2修饰的Cit-CS-UCNPs的形成, Cit-CS-UCNPs在654 nm处的荧光强度会逐渐下降。 验证了Cit-CS-UCNPs与MnO2纳米片可以构成FRET体系, 进而实现了能量从Cit-CS-UCNPs到MnO2纳米片的转移[18]。 为后续检测分析应用奠定了基础。 进一步了考察不同浓度KMnO4(0~10.0 mmol· L-1)对检测体系的影响。 观察图6(a)发现, 随着KMnO4浓度由0 mmol· L-1增至10 mmol· L-1, Cit-CS-UCNPs的荧光强度逐渐递减, 当KMnO4浓度达到10 mmol· L-1时, Cit-CS-UCNPs荧光强度到达最低值。 结合图6(b), 当KMnO4浓度为10 mmol· L-1时, 猝灭效率可达90%, 此时猝灭效率曲线走势也逐步趋平缓。 因此采取10 mmol· L-1作为KMnO4的反应浓度。
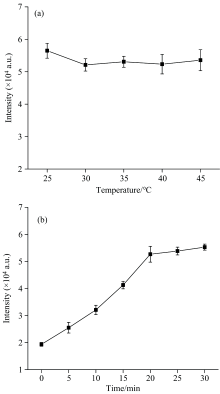
为了得到更高灵敏度的检测体系, 对培育温度和时间进行调控。 在探究不同培育温度的检测过程中, 设置各参数如下: 0.1 mL的H2O2(1 000 μ mol· L-1), 0.1 mL的Cit-CS-UCNPs-MnO2(0.4 mg· mL-1), 孵育为30 min, 孵育温度设置为25~45 ℃。 观察图7(a)发现, 在25~45 ℃的温度范围内, Cit-CS-UCNPs-MnO2荧光强度变化不大, 存在小范围浮动, 说明该传感器的荧光恢复信号受孵育温度影响不明显。 在一定温度区间内, 该传感器稳定性较高。 考虑到实验操作的便捷性, 选定25 ℃作为检测孵育温度。 在探究不同培育时间的检测过程中, 其他条件保持相同, 测量0~30 min孵育时间内相应的Cit-CS-UCNPs-MnO2荧光信号, 由图7(b)可知, 随着孵育时间的延长, Cit-CS-UCNPs-MnO2荧光信号逐渐恢复, 约20 min趋于平衡。 证明了当孵育时间达到20 min时, MnO2和H2O2之间氧化还原反应基本完全, Cit-CS-UCNPs-MnO2荧光恢复值最大。 为了保证反应进行彻底, 选定25 min作为后续实验的孵育时间。
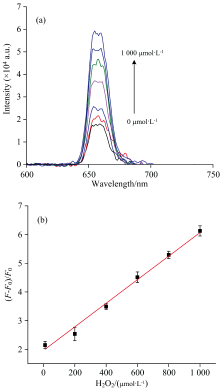
保持最佳的检测条件, 采用Cit-CS-UCNPs-MnO2荧光纳米传感器对H2O2进行检测。 如图8(a)为传感器的上转换荧光光谱随H2O2浓度变化, 结果表明随着加入H2O2浓度的提高Cit-CS-UCNPs-MnO2传感器的UCL强度不断提高, 当H2O2浓度为1 000 μ mol· L-1时, UCL荧光信号恢复最大。 如图8(b)所示, 绘制标准工作曲线, 建立工作方程。 其中荧光强度变化比率定义为(F-F0)/F0, F0为H2O2浓度为0 mg· L-1时的检测溶液荧光强度, F为H2O2浓度分别为0、10、 200、 400、 600、 800和1 000 μ mol· L-1时的检测溶液荧光强度。
Cit-CS-UCNPs-MnO2在654 nm的荧光强度变化比率与H2O2的浓度呈线性关系, 线性方程为: y=0.004 1x+0.196 3, R2=0.992。 由公式3σ /K(其中, σ 为标准偏差, K为线性曲线斜率)[19], 求得相应检测限为1.50 μ mol· L-1。 表明在一定浓度范围内, Cit-CS-UCNPs-MnO2荧光纳米传感器可以实现对H2O2的快速、 灵敏检测。
2.4.3 特异性检测
为了进一步探究Cit-CS-UCNPs-MnO2荧光纳米传感器对H2O2检测的选择性, 选取一些食品中存在的代表性金属离子(如K+、 Na+、 Ca2+和Mg2+)和常见的食品添加剂(BA、 Glu、 PS、 Suc、 Nat和Ino)作为研究对象进行选择性测试。 首先将0.1 mL去离子水、 H2O2和选取的典型物质分别加到0.1 mL Cit-CS-UCNPs-MnO2(0.4 mg· mL-1)中配置空白样(Blank)和相应的检测样品, 其中选取的典型物质浓度为H2O2浓度(6 mmol· L-1)的10倍。 再将反应液在25 ℃下孵育25 min, 测量其UCL强度(见图9)。 对Cit-CS-UCNPs-MnO2的荧光恢复情况进行评估, 发现与H2O2相比, Cit-CS-UCNPs-MnO2对其他添加物质没有强烈的反应, 传感器整体荧光信号波动不大, 由此可知Cit-CS-UCNPs-MnO2对H2O2有一定选择性。
通过优化培育温度和时间来提高Cit-CS-UCNPs-MnO2荧光纳米传感器的检测性能。 在优化培育温度的过程中, 各参数为: 0.1 mL的TBHQ(0.6 mmol· L-1), 0.1 mL的Cit-CS-UCNPs-MnO2(0.4 mg· mL-1), 孵育为30 min, 孵育温度范围设定在25~45 ℃。 由图10(a), 在25~35 ℃的孵育温度下, Cit-CS-UCNPs-MnO2荧光强度保持平衡, 当温度高于35 ℃, 则出现小幅下降, 分析认为由于温度升高, 部分TBHQ被离心管内的氧气氧化, 导致性能下降。 考虑到孵育温度不宜过高, 为了更好地防止温度变化对TBHQ性能影响, 选取25 ℃作为检测孵育温度。 在优化培育时间的过程中, 保持其他参数相同, 记录0~30 min孵育时间内相应的Cit-CS-UCNPs-MnO2的UCL强度。 由图10(b)可知, 传感器的荧光强度随着孵育时间的延长逐渐增强, 在约25 min达到最高值, 30 min时基本持平。 表明了当孵育时间达到25 min时, MnO2和TBHQ之间反应基本结束, 为了确保反应完全选定30 min作为后续实验的孵育时间。
保持最佳的检测条件, 采用Cit-CS-UCNPs-MnO2荧光纳米传感器对TBHQ进行检测。 如图11(a)传感器的上转换荧光光谱随TBHQ浓度变化图显示, 该传感器的UCL强度随着加入的TBHQ浓度的增加而有所回升, 当TBHQ浓度为0.6 mmol· L-1时, UCL强度达到最高值。 与H2O2检测制图方法一致, 绘制“ 荧光强度变化比率-TBHQ浓度” 标准工作曲线, 建立工作方程。 由图11(b)可知, 在0~6.0 mmol· L-1的浓度范围内, Cit-CS-UCNPs-MnO2在654 nm的荧光强度变化比率与TBHQ的浓度呈两段式线性关系, 线性方程分别为: y=4.583x+1.918, R2=0.998和y=1.237x+6.171, R2=0.992。 由公式3σ /K, 计算可得检测限为0.001 3 mmol· L-1。 Cit-CS-UCNPs-MnO2对TBHQ的良好响应, 说明了构建的荧光纳米传感器可靠。 在一定浓度范围内, 该传感器可以实现水溶液中TBHQ的检测, 具有检测范围宽、 检测限较低和快捷灵敏等优势。
2.5.3 特异性检测
为了验证Cit-CS-UCNPs-MnO2荧光纳米传感器对TBHQ检测具有一定的选择性, 选取一些食品中存在的代表性金属离子与常见的食品添加剂作为特异性检测对象进行选择性测试, 结果如图12。 将0.1 mL去离子水、 TBHQ(10 mmol· L-1)和选取物质(60 mmol· L-1)分别加到0.1 mL Cit-CS-UCNPs-MnO2(0.4 mg· mL-1)中配置检测样, 于25 ℃下孵育30 min, 记录检测液的荧光强度信号值。 观察图12检测液的荧光强度变化可知, 除了TBHQ外其他检测物即使在较高浓度的添加情况下, 也不会引起Cit-CS-UCNPs-MnO2的UCL强度发生显著的变化, 整体荧光恢复不明显。 证明Cit-CS-UCNPs-MnO2对TBHQ选择性良好。
为了进一步验证本方法对真实样品测定的可行性, 选取超市购买的牛奶, 参照文献[20]对其进行处理, 经0.22 μ m微孔滤膜过滤并静置30 min后, 每份样品平行做3次加标回收实验, 结果见表1。 样品平均回收率为93.2%~102.0%, 相对标准偏差(RSD)小于4.4%, 表明本方法可用于实际样品中H2O2和TBHQ的检测。
| 表1 实际样品中H2O2和TBHQ加标回收率 Table 1 Determination of recoveries of H2O2and TBHQ spiked in actual samples |
采用Cit-CS-UCNPs和MnO2纳米片之间的FRET效应, 构建了用于检测H2O2和TBHQ的Cit-CS-UCNPs-MnO2荧光纳米传感器。 通过SEM、 荧光光谱和UV-Vis等对粒子的形貌结构和性能进行表征。 对猝灭剂浓度进行优化, 结果表明KMnO4的最佳浓度为10 mol· L-1时, 猝灭效率可达90%且基本达到平衡。 对检测条件进行优化, 结果表明H2O2的检测孵育时间为25 min时, TBHQ的检测孵育时间为30 min。 在最佳实验条件下, Cit-CS-UCNPs-MnO2的荧光强度恢复率与H2O2浓度(0~1 000 μ mol· L-1)呈良好的线性关系, 检测限为1.50 μ mol· L-1; 与TBHQ浓度(0~0.6 mmol· L-1)呈两段式线性关系, 检测限为0.001 3 mmol· L-1。 保持最佳实验条件, 选取食品中存在的代表性金属离子(如K+、 Na+、 Ca2+和Mg2+)和常见的食品添加剂(BA、 Glu、 PS、 Suc、 Nat和Ino)作为研究对象进行对照试验, 结果证明与H2O2和TBHQ相比, Cit-CS-UCNPs-MnO2对其他添加物质没有强烈的反应, 传感器整体荧光信号波动小, 说明Cit-CS-UCNPs-MnO2对H2O2和TBHQ可进行特异性检测。 实际样品的平均回收率为93.2%~102.0%, RSD< 4.4%, 证明本方法在环境安全及食品检测等领域具有潜在的商业应用价值。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|