作者简介: 孟庆阳, 1994年生,天津大学精密仪器与光电子工程学院博士研究生 e-mail: qymeng@tju.edu.cn
溶解氧浓度的准确测定在医疗应用、 海洋监测、 工农业生产等领域中, 起到至关重要的作用。 本篇论文提出了一种比率式光纤溶解氧传感器, 以四乙氧基硅烷(TEOS)和正辛基三乙氧基硅烷(Octyl-triEOS)为前驱体的有机改性硅酸盐(ORMOSILs)作为载体基质, 选用三(4,7-联苯-1,10-邻菲啰啉)二氯化钌(Ru(dpp
The accurate measurement of dissolved oxygen concentration plays a crucial role in medical applications, marine monitoring, industrial and agricultural production, and other fields. A ratiometric optical fiber dissolved oxygen sensor is proposed. Organic modified silicates (ORMOSILs) using tetraethoxysilane (TEOS) and triethoxyoctylsilane (Octyl-triEOS) as precursors as carrier matrices, tris(4,7-diphenyl-1,10-phenanthrolin) ruthenium(II) dichloride complex (Ru(DPP
溶解氧浓度的准确测定在医疗应用、 海洋监测、 工农业生产中具有至关重要的作用[1, 2, 3]。 因此, 开发出一种准确、 稳定、 快速响应的溶解氧传感器尤为重要。 目前溶解氧的测量方法有碘量法、 Clark电极法等传统方法[4]。 碘量法是测定溶解氧的经典方法, 但步骤和化学反应复杂, 无法进行溶解氧的原位检测。 与碘量法相比, Clark电极法能够实现实时测量, 然而, 电极和薄膜会持续老化, 导致传感器需要频繁校准。 光纤化学溶解氧传感器[5]通常是基于氧分子与荧光或磷光分子在载体基质中的碰撞猝灭原理制备的, 相比于传统溶解氧传感器, 具有不耗氧、 操作简单、 成本低和抗电磁干扰等优点。 2016年, 熊艳等[6]将一种微型传感器集成在光纤表面, 通过倏逝波诱导荧光猝灭实现了氧含量的测定。 三(2, 2-联吡啶)钌荧光团被固定在有机改性硅酸盐(ORMOSILs)薄膜中, 并被涂在光纤表面。 通过对光纤表面倏逝波激发和荧光猝灭的集成, 该传感器成功地实现了小型化。 2020年, Xiong等[7]基于钌络合物的荧光猝灭, 设计了一种频率域全内反射(TIR)光流控溶解氧传感器。 结果表明测量分辨率为0.2 ppm, 响应时间小于1 min。 这种光流控溶解氧传感器有作为水监测和生物医学应用的原位平台的潜力。 2021年, 卞正兰等[8]通过在塑料光纤端部涂覆生物相容性PEGDA(聚乙二醇双丙烯酸酯)水凝胶膜制备了溶解氧传感器, 响应时间在10 s以内, 有望应用于生物医学领域的溶解氧监测。
为了提高氧传感器的灵敏度, 需要长寿命的氧敏感染料。 钌(Ⅱ )络合物[9, 10]中的Ru(dpp
在本研究中, 设计了一个光纤溶解氧传感器, 利用溶胶-凝胶工艺, 以四乙氧基硅烷(TEOS)和正辛基三乙氧基硅烷(Octyl-triEOS)作为前驱体, 制备了多孔的有机改性硅酸盐, 作为载体基质, 采用Ru(dpp
在光源的激发下, 氧敏感染料产生荧光, 由于氧的荧光猝灭原理, 荧光强度下降, 通过检测氧敏感染料猝灭的程度, 达到检测氧浓度的目的。 荧光强度与氧浓度的关系可以用Stern-Volmer方程描述[15]
式(1)中, I0和I分别表示在无氧和有氧条件下的荧光强度; [O2]表示氧的浓度; K为Stern-Volmer猝灭常数。
虽然仅使用Ru(dpp
式(2)中, R0和R分别表示无氧和有氧条件下的染料荧光强度比, IAFC0和IAFC分别表示无氧和有氧条件下香豆素的荧光强度。
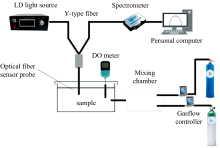
图1展示了实验系统装置原理图。 在气体流量计的控制下, 氧气和氮气在气体混合室内混合, 得到九种氧气浓度, 将混合气体通入样品溶液中, 通过AS720溶解氧仪测量样品溶液的溶解氧浓度, 作为溶解氧浓度的标准数据。 光源的发射波长为405 nm, 经过传感膜的激发后产生荧光, 荧光传输至光谱仪, 最终在电脑上保存荧光光谱, 进行数据处理。
溶解氧传感实验所需的化学试剂包括: 四乙氧基硅烷(TEOS, 纯度98%, 凯玛特(天津)化工科技有限公司); 正辛基三乙氧基硅烷(Octyl-triEOS, 纯度98%, 天津希恩思奥普德科技有限公司); Triton X-100(北京浩赛科技有限公司); Ru(dpp
405 nm光源(长春镭仕光电科技有限公司); 1 000 μ m Y型分叉光纤(FC/PC-UV1000/1500, 合束端0.6 m, 两个分支各1 m, 北京首量科技股份有限公司); 1 000 μ m纤芯传感光纤(FC/PC-BGUV1000/1500-0.6, 长度0.6 m, 北京首量科技股份有限公司); USB2000+便携式光纤光谱仪(海洋光学); AS720溶解氧仪(ASONE亚速旺); 不锈钢减压器。
首先将4 mL TEOS和0.2 mL Octyl-triEOS混合成前驱液, 将1.25 mL 乙醇和0.4 mL 0.1 mol· L-1盐酸加入到溶胶溶液中, 并封盖进行磁性搅拌1 h, 并在搅拌过程中, 添加0.1 mL Triton-X-100。 将4 mg Ru(dpp
TEOS和Octyl-triEOS通过溶胶-凝胶工艺, 在室温下发生水解缩合反应, 形成致密的凝胶, 将Ru(dpp
用偏光显微镜(CX40P)观察光纤端面的传感膜, 对旋涂在光纤端面的传感膜的厚度进行了表征, 物镜放大倍数为10倍, 厚度为569 μ m, 如图2所示, 刻度已在图中标注。
基于TEOS制备的凝胶骨架为亲水性, 影响传感膜性能。 而使用疏水性的有机修饰前体的增加, 会形成正硅氧烷, 几乎不被离子渗透, 可以被氧气和其他小分子气体渗透, 可以显著提高传感膜的性能。 正辛基三乙氧基硅烷中的辛基对水的亲和力较低, 可以增加传感膜的疏水性, 提高氧气分子的渗透。 为了表征传感膜的疏水性, 对旋涂在光纤端面的传感膜进行了水接触角的测试, 测得传感膜的水接触角为81° , 通常接触角θ < 5° , 认定表面为超亲水性表面; 5° ≤ θ < 75° 时, 认定表面为亲水性表面; 75° ≤ θ ≤ 150° 时为疏水性表面, 证明形成的传感膜具有疏水性。
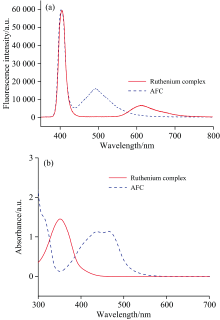
图3显示Ru(dpp
用制作的光纤化学传感器对不同的溶解氧浓度进行了测量, 测出的荧光光谱如图4所示。 在光源激发下, AFC和Ru(dpp
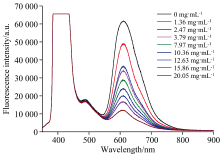 | 图4 不同溶解氧浓度下传感器荧光发射光谱Fig.4 Fluorescence emission spectra of sensor at different dissolved oxygen concentrations |
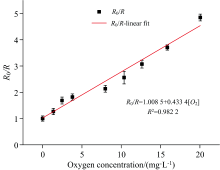
分别采集了AFC在490 nm处的荧光强度和钌络合物在605 nm处的荧光强度, 并根据式(2)绘制了Stern-Volmer方程曲线。 如图5所示, 该溶解氧传感器的相对荧光强度与溶解氧的浓度具有较好的线性关系, 说明凝胶中几乎所有Ru(dpp
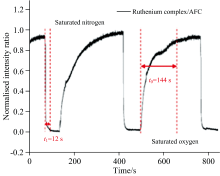
图6是在水中测量得到的响应时间曲线, 响应时间是指平衡值强度读数发生90%变化所需要的时间。 从图中可以看出, 无论在饱和氮溶液中还是在饱和氧溶液中, Ru(dpp
式(3)中, ti为饱和氮溶液到饱和氧溶液的响应时间, to为饱和氧溶液到饱和氮溶液的恢复时间。 根据式(3), 计算出该传感膜的不对称因子为12, ASY因子的大小取决于传感膜基质的扩散系数[16]。 这种现象, 可以用膜内外不同氧气浓度的渗透来解释, 在从饱和氮溶液到饱和氧溶液时, 传感膜外的氧气含量为100%, 膜内氧气含量也会从0%迅速达到100%。 但从饱和氧溶液到饱和氮溶液时, 传感膜外的氧气含量为0%, 膜内的氧气则会缓慢流出, 从而产生在膜内较长的停留时间, 从而恢复时间长于响应时间。
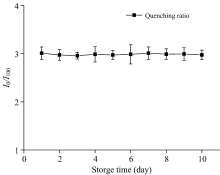
保持光源稳定, 检测在同一溶解氧浓度环境下Ru(dpp
基于荧光猝灭原理提出了一种比率式光纤化学溶解氧传感器, 采用Ru(dpp
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|