作者简介: 李长明, 1990年生, 长春光华学院工程技术研发中心讲师 e-mail: 83463808@qq.com
灭蝇胺是一种白色结晶粉末状的应用于各种瓜果类、 茄果类、 豆类及多种叶菜类农业生产中的昆虫杀虫剂, 广泛应用农业生产等领域。 灭蝇胺的大量使用对生态环境有极强的破坏性, 危害人类身体健康。 因此, 对蔬菜农业生产过程中的灭蝇胺农药残留的快速检测技术的需求十分迫切。 表面增强拉曼光谱技术(SERS)具有高灵敏度、 高准确度以及样品准备简单等优点, 已经成为农药残留检测领域的热点研究技术; 密度泛函理论(DFT)可用于分子结构与性质的理论模拟及拉曼光谱的计算。 基于密度泛函理论对引入金纳米团簇基底灭蝇胺分子的表面增强拉曼光谱进行计算, 采用Multiwfn软件结合VMD软件探究了灭蝇胺分子表面静电势分布, 基于B3LYP/6-31++G(d,p)基组对结合4个Au原子团簇形成的灭蝇胺—金纳米团簇复合物采用B3LYP方法, 对灭蝇胺分子中与Au纳米团簇可能配位的原子使用6-31++G(d,p)基组, Au原子团簇使用LANL2DZ赝式基组, 进行灭蝇胺—金纳米团簇复合物的结构优化与表面增强拉曼光谱计算, 获得灭蝇胺分子的拉曼散射光谱和灭蝇胺分子与Au4聚体吸附的表面增强拉曼光谱, 并进行特征峰指认和比较。 由分子静电势分布可知, Au纳米团簇可能与灭蝇胺分子中的N1、 N3和N5原子位置处形成配位, 与C6H10N6分子形成C6H10N6-4Au纳米团簇化合物。 计算对比分析了N1、 N3和N5原子配位形成的C6H10N6-4Au的拉曼光谱, 由于Au原子团簇的侵入, Au原子团簇与N1、 N3和N5配位形成的C6H10N6-4Au分子Raman光谱特征峰最大增强分别达到4.0倍、 1.4倍和3.2倍, 且Raman谱峰出现了选择增强, 并且谱峰位置发生一定程度的红移或者蓝移。 研究结果为SERS技术用于蔬菜表面农药残留的快速检测奠定了理论基础。
Cyromazine is a white crystalline powder insecticide used in the agricultural production of various melons and fruits, solanaceous fruits, beans, and leafy vegetables. It is widely used in agriculture and other fields. However, the massive use of Cyromazine will be extremely destructive to the ecological environment and will endanger human health. Therefore, there is an urgent need for rapid detection technology of Cyromazine pesticide residues in the process of vegetable agricultural production. Surface-enhanced Raman spectroscopy (SERS) has the advantages of high sensitivity, high accuracy and simple sample preparation and has become a hot research technology in the field of pesticide residue detection. Density function theory (DFT) can be used for theoretical simulation of molecular structure and properties and calculation of Raman spectra. The surface-enhanced Raman spectra of Cyromazine molecule introduced into gold nanoclusters are calculated based on the density functional theory; the software of Multiwfn and VMD are used to explore the surface electrostatic potential distribution of herbicidal strong molecules. Based on the B3LYP/6-31++G(d,p)basis set, the structure optimization and Surface Enhanced Raman spectroscopy calculation of the Cyromazine-gold nanoclusters complex formed by combining 4Au atomic clusters are studied. The 6-31++G(d,p)basis set is used for the atoms in the Cyromazine molecule that may coordinate with the Au nanoclusters, and the LANL2DZ pseudo basis set is used for the Au Atomic Clusters. The Raman spectra and the surface-enhanced Raman Spectra of Cyromazine are obtained, and the characteristic peaks are identified and compared. According to the molecular electrostatic potential distribution, Au nanoclusters may form coordination with N1, N3 and N5 atoms in the C6H10N6 molecule and form C6H10N6-4Au nanoclusters. The Raman spectra of C6H10N6-4Au coordinated by N1, N3 and N5 atoms are calculated and analyzed, the maximum Raman spectral enhancement of C6H10N6-4Au molecules coordinated by Au clusters and N1, N3 and N5 is 4.0 times, 1.4 times and 3.2 times, respectively, and the position of the spectral peak has a certain degree of red shift or blue shift. The research results lay a theoretical foundation for the rapid detection of pesticide residues on the surface of vegetables by SERS technology.
灭蝇胺(C6H10N6)又称为N-环丙基-1, 3, 5-三嗪-2, 4, 6-三胺, 是一种白色结晶固体, 对于水果和蔬菜表面的蝇类害虫驱除具有较好的效果, 属于新型高效、 低毒、 含氮杂环类杀虫剂。 灭蝇胺作为高效、 低毒生态农药, 对白菜, 番茄和黄瓜生产中的潜蝇、 生姜存储期的蕈蚊等多种作物虫害效果显著[1, 2], 已广泛应用于各种瓜果类、 茄果类、 豆类及多种叶菜类农业生产中。 在农业蔬菜生产中大量使用灭蝇胺, 能够防治害虫危害, 提高蔬菜种植产量; 而过量使用灭蝇胺杀虫剂, 会造成蔬菜表面存在较高浓度的农药残留, 造成许多潜在的生态环境危害。 滥用农药污染生态环境, 危害人类身体健康。 因此, 建立一种高效、 快速、 原位的准确检测蔬菜表面灭蝇胺农药残留的方法迫在眉睫。 目前国内外人们常用的农药残留检测方法主要有液相色谱-串联质谱法[3]、 超高效液相色谱法[4], 生物测定法[5]等。 这些常规的农药残留检测方法具有仪器设备昂贵、 操作繁琐、 样品制备复杂、 分析时间较长等缺点。
拉曼光谱是一种基于拉曼散射原理的振动光谱, 拉曼光谱特征谱线对应唯一分子特征结构, 被称之为分子指纹光谱。 一般检测条件下, 物质的拉曼光谱信号较弱, 对于蔬菜表面的低浓度农药残留检测比较困难。 表面增强拉曼光谱技术(surface-enhanced Ramanspectroscopy, SERS)采用表面粗糙处理后的金、 银等贵重金属作为分子活性基底, 能够增强拉曼散射光谱达到104~106倍[6], 具有高灵敏度、 高准确度以及样品准备简单等优点, 能够检测吸附在金、 银等表面的低浓度待测量分子。 密度泛函理论方法(density functional theory, DFT)结合拉曼光谱方法共同研究物质已经成为当前的一种有效的研究手段。 Ismail Abdulazeez等[7]运用DFT计算了普鲁卡因分子的SERS光谱, 结果来源于普鲁卡因分子中的N原子与Ag表面相互作用。 Nandita Maiti等[8]指出氨基聚羧酸分子与金属原子结合至少有两种可能的结合方式, DFT预测表明氨基聚羧酸分子通过N原子和O原子直接吸附到Ag表面, 使得拉曼信号增强。 涂一树等[9]结合密度泛函理论和典型的二阶Mø ller-Plesset扰动理论方法对灭蝇胺分子进行了化学计算分析, 并将红外光谱与拉曼光谱结合, 分析了灭蝇胺的电子性质与振动模式。 陈玉锋等[10]运用DFT理论计算了杀草强分子的Raman光谱并且分析了杀草强和Ag可能吸附的位置。 谈爱玲等[11]采用SERS技术及DFT理论对农药毒死蜱进行了检测, 理论分析了毒死蜱分子与Ag2和Ag3结合后的SERS光谱增强以及拉曼谱峰频移。
基于DFT理论对杀草强分子的SERS谱进行了研究, 通过对灭蝇胺分子静电势的分析, 寻找了该分子与Au原子配位的合适位置。 分别对灭蝇胺分子与4个Au配位的复合物(C6H10N6-4Au)的SERS谱进行分析, 为研究灭蝇胺分子的SERS增强机理以及SERS技术在农药残留检测中的应用提供理论依据。
密度泛函理论(density functional theory, DFT)是探索多电子体系电子结构的方法。 采用计算分析为GaussView5.0和Gaussian09软件。 基于DFT理论, 在B3LYP/6-31++G(d, p)基组水平上对灭蝇胺分子结构进行优化。
运用Multiwfn结合VMD软件计算灭蝇胺分子的表面静电势分布, 以此获得灭蝇胺分子与Au纳米团簇配位结合的原子位置。 基于B3LYP/6-31++G(d, p)基组对灭蝇胺— 金纳米团簇复合物的表面增强拉曼光谱进行计算, 对结合4个Au原子团簇形成的灭蝇胺— 金纳米团簇复合物采用B3LYP方法, 对灭蝇胺分子中与Au纳米团簇可能配位的原子使用6-31++G(d, p)基组, Au原子团簇使用LANL2DZ赝式基组, 进行灭蝇胺— 金纳米团簇复合物的结构优化与Raman振动频率计算。 灭蝇胺分子的振动模式通过VEDA4软件进行分析, 在实验室内的DELL工作站上进行量子化学计算。
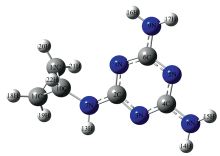
灭蝇胺分子式为C6H10N6, 由C、 H、 N元素组成, 分子量为166.18, 是一种白色结晶固体, 易溶于水。 灭蝇胺的分子构型用GaussView5.0构造, 理论计算采用Gaussian09量子化学软件。 基于DFT理论, 采用B3LYP/6-31++G(d, p)基组对灭蝇胺分子结构进行优化并计算振动频率, 优化后的灭蝇胺分子空间结构如图1所示。 计算得到的灭蝇胺分子的Raman振动频率均大于0, 未发现虚频, 证明优化后为稳定结构。
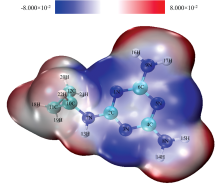
分子静电势是判断C6H10N6分子与Au纳米团簇可能配位原子位置的有效途径[12], 可对灭蝇胺分子的表面增强拉曼光谱机制进行解析。 基于Multiwfn和VMD软件计算得到灭蝇胺分子的静电势分布如图2所示。 红色区域表示亲核区域, 蓝色区域则表示亲电区域。 从灭蝇胺的分子表面静电势图中可以看出, 若想要使金属Au与灭蝇胺分子配位, 理论上Au原子应该选择蓝色区域位置。 C6H10N6分子中的N1、 N3和N5原子附近的表面静电势平均值分别为-20.30、 -20.73和-21.23 kcal· mol-1, 并且附近没有正值区域, 因此Au纳米团簇可能与灭蝇胺分子中的N1、 N3和N5原子位置处形成配位, 与C6H10N6分子形成C6H10N6-Au纳米团簇化合物。
灭蝇胺分子具有六个活性氮原子, 可与金原子配位并实现电子转移, 从而实现C6H10N6分子拉曼光谱的化学增强。 DFT理论计算研究结果表明, 4Au纳米团簇与分子结合可形成稳定的化合物结构, 能将4Au纳米团簇标示为分子的SERS基底, 实现分子的表面增强拉曼光谱[13]。 优化后的灭蝇胺分子与Au纳米颗粒配位体系的分子如图3(a, b, c)所示, 计算结果中无虚频, 表明优化后的C6H10N6-4Au分子是稳定的。 对于N配位Au后, 可以看到含C、 N的杂环化合物的夹角发生细微变化。 4Au-C6H10N6(N1)的C2-N1-C6的夹角为115.63° , N原子与Au原子之间的距离为2.15 a.u., 四个Au原子组成的二面角为176.20° , 两个Au原子与N1及相邻的C2所构成的二面角为90.66° 。 4Au-C6H10N6(N3)的C2-N3-C4的夹角为116.20° , N原子与Au原子之间的距离为2.13 a.u., 四个Au原子组成的二面角为176.79° , 两个Au原子与N3及相邻的C2所构成的二面角为90.35° 。 4Au-C6H10N6(N5)的C4-N5-C6的夹角为115.93° , N原子与Au原子之间的距离为2.14 a.u., 四个Au原子组成的二面角为179.65° , 两个Au原子与N5及相邻的C4所形成的二面角为88. 81° 。 从两个Au原子与N(N1, N3, N5)原子及相邻的C原子所形成的二面角都接近于90° , 说明Au原子团簇与C6H10N6分子中的N原子配位后所构成的平面与含C、 N的杂环化合物几乎构成面面垂直。
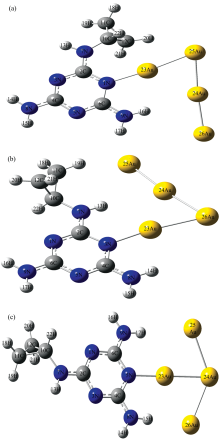 | 图3 C6H10N6-4Au配合物分子结构图 (a): C6H10N6-4Au(N1); (b): C6H10N6-4Au(N3); (c): C6H10N6-4Au(N5)Fig.3 C6H10N6-4Au molecular structure diagram (a): C6H10N6-4Au(N1); (b): C6H10N6-4Au(N3); (c): C6H10N6-4Au(N5) |
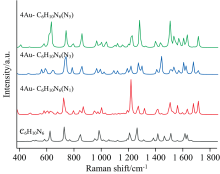
图4为C6H10N6分子及其分子中N1、 N3、 N5原子与Au原子配位的Raman光谱, 振动模式如表1所示。 从图4中可以看出, 加入金纳米原子后, C6H10N6的Raman光谱, C6H10N6-4Au(N1)、 C6H10N6-4Au(N3)和C6H10N6-4Au(N5)3个分子体系中的Raman特征峰存在一定的频移, 且Raman特征峰强度有明显增强。 在C6H10N6分子中, Raman谱峰729 cm-1对应N— C伸缩振动、 C— N— C面内弯曲振动和N— C— N面内弯曲振动, Raman光谱强度较弱。 在C6H10N6-4Au(N1)中谱线红移至724 cm-1处, 且Raman光谱增强了1.2倍; Raman谱峰1 211 cm-1对应了C6H10N6分子中H— C— C面内弯曲振动, 光谱强度较弱, 在C6H10N6-4Au(N1)中蓝移至1 222 cm-1处, 且由一弱峰变成了强峰光谱增强了4.0倍。 Raman谱峰1 510 cm-1对应了C6H10N6分子中H— C— N面内弯曲振动, Raman光谱强度较弱, 在C6H10N6-4Au(N1)中红移至1 509 cm-1处, Raman光谱强度增强了1.5倍。
| 表1 C6H10N6(N1, N3, N5)SERS光谱特征峰归属 Table 1 SERS spectral characteristic peak attribution of C6H10N6 |
当Au纳米颗粒与灭蝇胺C6I10N6分子中的N3原子结合配位时, C6H10N6-4Au(N3)分子体系的Raman光谱特征峰强度有明显增强。 在C6H10N6分子中, Raman谱峰847 cm-1对应了C— C伸缩振动、 C— C— C面内弯曲振动和H— C— C面内弯曲振动, Raman光谱强度较弱, 在C6H10N6-4Au(N3)中谱线蓝移至854 cm-1, 且Raman光谱强度增强了1.2倍; Raman谱峰1 383 cm-1对应了C6H10N6分子中H— N— C面内弯曲振动和H— C— N面内弯曲振动, 光谱强度较弱, 在C6H10N6-4Au(N3)中蓝移至1 410 cm-1处, 且Raman光谱强度增强了1.4倍; Raman谱峰1 417 cm-1对应了C6H10N6分子中H— N— C面内弯曲振动和H— C— N面内弯曲振动, Raman光谱强度较弱, 在C6H10N6-4Au(N3)中蓝移至1 444 cm-1处, 且由一弱峰变成了强峰, 光谱增强了2.3倍。
当Au纳米颗粒与灭蝇胺C6H10N6分子中的N5原子结合配位时, C6H10N6-4Au(N5)分子体系的Raman光谱特征峰有明显增强。 在C6H10N6分子中, Raman谱峰623 cm-1对应了N— C伸缩振动和C— N— C面内弯曲振动, 对应一较弱的Raman谱峰, 在C6H10N6-4Au(N5)中蓝移至631 cm-1处, 且Raman光谱强度增强了2.4倍; 在C6H10N6分子中, Raman谱峰847 cm-1对应了C— C伸缩振动、 C— C— C面内弯曲振动和H— C— C面内弯曲振动, 对应一较弱的Raman谱峰, 在C6H10N6-4Au(N5)中蓝移至854 cm-1处, Raman光谱增强了2.0倍; 在C6H10N6分子中, Raman谱峰1 211 cm-1对应了H— C— C面内弯曲振动, 对应一较弱的Raman谱峰, 在C6H10N6-4Au(N5)中蓝移至1 219 cm-1处, Raman光谱强度增强了1.2倍; 在C6H10N6分子中, Raman谱峰1 261 cm-1对应了N— C伸缩振动、 C— C伸缩振动和N— C— N面内弯曲振动, 对应一较弱的Raman谱峰, 在C6H10N6-4Au(N5)中蓝移至1 282 cm-1处, 且出现了较强的光谱增强, Raman光谱强度增强了2.0倍; 在C6H10N6分子中, Raman谱峰1 383 cm-1对应了H— N— C面内弯曲振动和H— C— N面内弯曲振动, 对应一较弱的Raman谱峰, 在C6H10N6-4Au(N5)中蓝移至1 402 cm-1处, Raman光谱强度增强了1.8倍; Raman谱峰1 510 cm-1对应了C6H10N6分子中H— C— H面内弯曲振动, Raman光谱强度较弱, 在C6H10N6-4Au(N5)中蓝移至1 511 cm-1处, 且由一弱峰变成了强峰, 光谱增强了3.2倍。
Au原子的接入增强了N— C、 C— C之间的伸缩振动和H— N— C面内弯曲振动、 H— C— N面内弯曲振动、 H— C— C面内弯曲振动、 C— N— C面内弯曲振动。 Raman光谱的增强效果集中在600~1 500 cm-1区域。 通过对比分析, 发现灭蝇胺分子在N1、 N3和N5上连接Au原子的Raman增强程度最高, 均呈现了Raman光谱选择性增强, 基于DFT计算的C6H10N6分子SERS增强机制主要来源于电子转移导致的化学增强。 Au原子团簇与N1、 N3和N5配位形成的C6H10N6-4Au分子Raman光谱特征峰最大增强分别达到4.0倍、 1.4倍和3.2倍。 根据Herzber-Teller表面选择规则, 得出含C、 N的杂环化合物接近并垂直金表面, 从而导致N原子和金原子团簇形成配位, 产生电荷转移效应[14], 分子极化率增大使得C6H10N6分子的Raman光谱出现了选择性增强, 并有一定的Raman频移。
基于密度泛函理论, 基于GaussView5.0和Gaussian09软件理论计算了灭蝇胺分子的表面增强拉曼光谱, 分析探讨灭蝇胺分子与Au原子团簇配位的原子位置对拉曼光谱选择增强以及增强因子的影响。 由分子静电势分布可知, Au纳米团簇可能与灭蝇胺分子中的N1、 N3和N5原子位置处形成配位, 与C6H10N6分子形成C6H10N6-4Au纳米团簇化合物。 计算对比分析了N1、 N3和N5原子配位形成的C6H10N6-4Au的拉曼光谱, 由于Au原子团簇的侵入, Au原子团簇与N1、 N3和N5配位形成的C6H10N6-4Au分子, Raman光谱特征峰最大增强分别达到4.0倍、 1.4倍和3.2倍, 且Raman谱峰出现了选择增强, 谱峰位置发生一定程度的红移或者蓝移。 研究结果为SERS技术用于蔬菜表面农药残留的快速检测奠定了理论基础。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|