作者简介: 王方原, 1988年生, 桂林电子科技大学光电工程学院副研究员 e-mail: wangfy@guet.edu.cn
木质素是自然界中第二丰富的天然聚合物, 广泛存在于各种陆地植物的木质部中, 利用木质素拉曼光谱对植物种类进行快速无损鉴别具有重要的应用价值。 但由于木质素大分子构型非常复杂, 对其拉曼特征光谱的仿真研究一直存在困难。 利用Gaussian16W中包含的B3LYP密度泛函方法结合6-311G(d, p)基组, 构建出三种木质素单体及其三种同种木质素单体构成的二聚体以及三种异种木质素单体构成的二聚体, 提出了一种利用木质素的三种基本结构单体及其二聚体仿真分析木质素大分子拉曼光谱特征的方法。 首先计算了三种单体的基本构型、 轨道能级和电子空间分布, 并分析了三种木质素单体拉曼光谱和振动模式的特点。 随后利用不同组合方式的β-O-4二聚体的光谱谱峰特征, 解释了特征谱峰信号位置漂移的成因, 提出了判断木质素大分子信号特征的主要依据。 研究结果表明, 1 712 cm-1谱峰信号最强且位置稳定, 振动归属为碳碳双键伸缩振动, 该振动归属引起的特征峰可以作为木质素大分子最主要的信号特征; 1 642 cm-1谱峰信号振动归属为芳香环骨架振动, 仅受芳香环甲基数量影响产生劈裂, 该振动归属引起的特征峰不仅可以作为识别木质素大分子最主要的信号特征也可以作为木质素内三种单体含量的判据; 1 352 cm-1谱峰信号振动归属为HC=CH原子链摇摆振动, 附近的特征峰受单体种类和聚合方式共同影响, 在木质素大分子拉曼光谱中会形成信号包络, 可以作为鉴别木质素的一个辅助判据。 该研究对于复杂分子的光谱特征及其物理机制的仿真具有一定的借鉴价值, 同时也能为植物检材的拉曼光谱分析方法提供理论指导。
Lignin is the second most abundant natural polymer in nature. It widely exists in the xylem of various terrestrial plants. The rapid and nondestructive plant species identification using lignin Raman spectroscopy has great application prospects. However, due to the complex configuration of lignin macromolecules, it is difficult to study the Raman spectra of lignin macromolecules using first-principles calculations. In this paper, using the B3LYP density functional method included in Gaussian16W combined with the 6-311G(d,p) basis set, three lignin monomers and dimers composed of three homologous lignin monomers and three heterologous lignin monomers were constructed. A dimer composed of lignin monomers was proposed, and a method was proposed to use the three basic structural monomers of lignin and their dimers to simulate and analyze the Raman spectral characteristics of lignin macromolecules. Firstly, the geometric configurations, orbital energy levels and electronic spatial distributions of the three monomers are calculated, and the characteristics of Raman spectra and vibrational modes of the monomers are analyzed. Then, the spectral peak characteristics of β-O-4 dimers with different monomer combinationsare compared to explain the frequency shift and shape change of the characteristic peaks. The results showed that the 1 712 cm-1 peak is the strongest Raman signal. The vibration is attributed to carbon-carbon double bond stretching vibration, and the characteristic peak caused by the vibration attribution can be used as the most important signal characteristics of lignin macromolecules. The 1 642 cm-1 peak signal is only affected by the amount of aromatic ring methyl. The vibration is attributed to aromatic ring skeleton vibration, which can be used as a criterion for the content of three monomers in lignin. The characteristic peak near 1 352 cm-1 belongs toHC=CH atomic chain sway vibration, which is affected by the type of monomer and the mode of polymerization, and a signal envelope may be formed in the Raman spectrum of lignin macromolecules, which can be regarded as an auxiliary criterion for the identification of lignin. The results provide a reference for the simulation of the spectral characteristics and physical mechanism of complex macromolecules and also provide theoretical guidance for the Raman spectral analysis of plant samples.
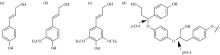
在自然界中, 木质素[1]是位于纤维素之后第二丰富的天然聚合物, 广泛存在于各种陆地植物的木质部中。 木质素的主要功能包括通过形成木质素-碳水化合物复合物来强化植物细胞壁, 抵抗微生物的攻击, 并通过降低细胞壁的渗透性在水分运输中发挥关键作用[2, 3]。 木质素是由苯丙烷单元通过碳-碳键和醚键连接而成的无定形大分子聚合物, 包括了甲氧基、 羟基、 羧基、 芳香酚环等官能团, 具有非常复杂的三维结构。 图1给出了木质素的三种基本苯丙烷结构的三种单体, 即紫丁香基苯烷单体(S型)、 愈创木基苯烷单体(G型)、 对羟苯基丙烷单体(H型)[4, 5]。 三种苯丙烷单体通过β -O-4, α -O-4, β -β , β -1, β -5和5-5等碳-碳键或碳-氧键连接形成木质素大分子聚合体。 如图1(d)所示为木质素单体间的两种主要连接方式, 其中β -O-4芳醚键连接所占比例最高, 约为50%左右, 远远高于其他醚键[6, 7]。 不同植物所含有的木质素存在三种单体结构的比例差异, 例如草本木质素同时包含H、 G、 S三种木质素结构单体, 针叶材木质素主要由G型木质素单体组成(约90%), 而阔叶材木质素主要由G和S型木质素单体组成(约各50%)[8]。 因此, 根据不同植物检材中木质素及其基本单体的相对含量差异, 就能实现植物科属的快速鉴定, 具有重要的研究价值和应用前景。
拉曼光谱能反映物质的分子结构的特征信息, 具有快速、 简单、 无损、 可重复检测的特点, 广泛应用于分子化学结构研究和化学组成分析[9, 10]。 在2006年, Agarwal[11]采用激光共焦拉曼显微镜测定了黑云杉木材细胞壁中木质素和纤维素的分布以及木质素的拉曼光谱; 在2014年, Gierlinger[12]使用扫描拉曼显微镜测定了杨木中木质素的拉曼特征峰分布; 在2016年Cogulet等[12, 13]对白云杉中木质素拉曼特征峰进行了测量。 上述研究中测得的木质素特征峰波数范围都主要落在1 100~1 800 cm-1之间, 且分别对木质素的拉曼特征峰的振动归属进行了分析和解释。 虽然木质素的拉曼光谱实验研究已经得到了很好的发展, 但是由于木质素大分子的原子数量较多、 结构相对复杂, 因此关于木质素拉曼光谱的理论仿真工作还相对较少。
为了克服大分子仿真计算的困难, 本文提出了一种通过三种木质素苯丙烷单体及其β -O-4二聚体的仿真拉曼光谱, 来开展木质素大分子拉曼特征光谱仿真研究的方法。 本文首先对三个基本单体结构进行几何结构优化, 得到稳定的分子构型, 并对其能级结构和轨道特征进行对比和分析。 其次, 根据三种单体结构的仿真拉曼光谱和振动归属, 分析不同单体结构的拉曼信号特征及其识别方法, 并与其他文献的木质素实验测量结果进行对比验证。 在此基础上, 将其两两之间利用β -O-4成键方式进行组合, 观察β -O-4成键方式对三种单体结构拉曼信号特征的影响, 为利用植物中木质素基础单体含量差异的进行拉曼光谱定量分析提供理论依据。
利用Gaussian16W软件实施第一性原理仿真计算, 分子结构的哈密顿量[14]表达式如式(1)
式(1)中, TN表示原子核的动能, Te表示电子的动能, V是势能项(包含了所有电子与电子之间, 核与核之间, 电子与核之间的相互作用势能)。 仿真计算过程采用密度泛函DFT的方法, 将电子能量划分表达式为
式(2)中, ET为动能项(由电子运动引起)[15], EV包括原子核与电子间的吸引作用和原子核与原子核之间的排斥作用[15, 16], EJ描述电子与电子之间的排斥作用, EXC表示电子之间交换关联作用[17, 18]。
利用密度泛函DFT的B3LYP方法在6-311G(d, p)的基组环境下对木质素的三个基本单体结构进行几何结构优化。 木质素基本单体的分子结构是否达到最优几何构型, 取决于其原子与原子之间的受力情况和分子整体的能量值。 当原子间受力和分子整体能量都达到最小值后, 优化完成且结构稳定。 优化后的木质素单体结构如图2所示。 优化后的木质素单体分子所有的碳原子都在同一平面上, 且S型木质素除去碳-碳双键以上的部分, 下半部分的苯环和两个甲氧基具有高度对称性, 这也显示出其优化后分子都具有较高的稳定性。
 | 图2 优化后的木质素单体结构图 (a): 优化后的H型木质素; (b): 优化后的G型木质素; (c): 优化后的S型木质素Fig.2 Optimized lignin unit structure (a): Optimized H-type lignin; (b): Optimized G-type lignin; (c): Optimized S-type lignin |
三种木质素单体分子前线轨道信息如表1所示, 这些木质素单体分子结构在HOMO上, 电子的占据数均为两个, 而LUMO无电子占据。 S型木质素的能隙为4.608 eV, G型木质素为4.754 eV, H型木质素为4.874 eV。 从整体上看, 三种木质素单体结构的能隙差都达到了4.5 eV以上, 表明其本身化学的稳定性均良好; 由于甲氧基的存在, G型木质素和S型木质素的分子的能隙相比于H型木质素顺次减小。
| 表1 三种木质素单体分子前线轨道信息 Table 1 Molecular frontier orbital information of three lignin units |
从轨道电子空间分布情况看, 三种木质素单体的电子云差异不大, 在HOMO的电子云主要分布在苯环与侧链结构连接处的碳原子上、 侧链上的碳碳双键部位、 苯环与羟基、 甲氧基连接处的碳原子上以及在羟基与甲氧基的氧原子部位, 并且在侧链结构的连接处碳原子上及两侧、 碳碳双键和侧链的对位位置电子云浓度高。 HOMO的电子云主要就是由这部分的原子贡献的, 表明这些原子化学活性较强, 当发生化学反应时, 该部位的原子容易向外游离电子[19], 形成反应位点。 在侧链上的末端处位置以及甲氧基末端的甲基(— CH3)处的原子对HOMO的贡献很小, 基本无电子云, 这些部位的结构稳定性好, 基本不参与化学反应。 从LUMO上进行对比, 同样三种木质素的电子云差异也不大, 并且其电子云主要集中在侧链与苯环相连的两个碳原子、 苯环未被替代的两个碳原子以及羟基的碳原子上, 表明这些原子对LUMO的贡献占主要地位, 其亲和电子的能力强, 在反应过程中容易吸收游离的电子。 在侧链的末端以及甲氧基的甲基上基本无电子云, 这部分的位置对LUMO的贡献几乎为零, 对电子的亲和能力较弱, 在化学反应过程中, 该部分位置基本不吸收其他电子。
这三种木质素单体的HOMO-LUMO的电子云分布的结果与大分子木质素的主要连接方式相符合。 如占据连接比例50%以上的β -O-4芳醚键, 其就是单体木质素的碳碳双键断裂与苯环侧链的羟基脱氢相连。 包括苯丙烷侧链的其他连接方式α -O-4、 γ -O-4等, 都表明仿真优化的单体电子云分布符合实际情况。
利用木质素单体的分子振动模式计算得到拉曼光谱如图3所示, 其中横坐标为波数, 纵坐标为拉曼信号强度。 从中可以得出H、 G、 S型木质素单体分别在1 328、 1 656、 1 712, 1 352、 1 648、 1 720, 1 360、 1 632、 1 720 cm-1等位置有明显的拉曼特征峰, 且特征峰强度也较强。 这三种木质素单体拉曼特征峰的分布范围大体相同, 原因是他们的分子结构除了甲氧基数量以外整体结构基本相同, 振动归属主要为碳氢键摇摆振动、 芳香环骨架伸缩振动、 碳碳双键伸缩振动等。 如图2中所示, 碳氢键摇摆振动主要由碳碳双键旁的H2和H4贡献, 芳香环骨架伸缩振动由苯环上碳原子之间连接键伸缩及苯环末端羟基连接键摇摆贡献, 碳碳双键伸缩振动由图中C1和C3连接双键伸缩及C1和C3旁氢键角摇摆变化贡献。 S型和G型木质素单体在1 448和1 544 cm-1处有特征峰而H型木质素单体没有这个特征峰, 原因是该特征峰为甲氧基的的弯曲振动导致; H型木质素分子的苯环没有甲氧基, 故没有该处的特征峰。 从光谱图中还可以看出在1 248 cm-1处H型木质素特征峰强度显著高于S型和G型木质素, 该谱峰对应芳香环骨架碳氢键摇摆振动。 因为S型和G型木质素芳香环骨架两边具有甲氧基基团, 苯环稳定性相比H型木质素更好, 故在此1 248 cm-1对应的碳氢键摇摆振动效果弱于H型木质素。 因此, 可以根据上述几个特征峰将H型木质素与S型和G型木质素区分开来。 三种木质素单元的特征峰振动归属如表2所示。
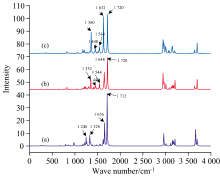 | 图3 木质素单体拉曼光谱图 (a): H型木质素单体; (b): G型木质素单体; (c): S型木质素单体Fig.3 Raman spectrum of lignin monomer (a): H-type lignin unit; (b): G-type lignin unit; (c): S-type lignin unit |
| 表2 木质素单体特征峰振动归属 Table 2 Vibration attribution of characteristic peaks of lignin units |
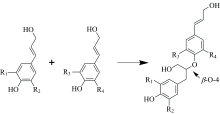
考虑到木质素大分子的拉曼光谱不仅含有三种单体的特征信号, 同时也应该包括各单体两两结合时所形成的化学键对应的拉曼谱峰以及该化学键成键后对原有拉曼特征谱峰的影响。 本文选取连接中占比最高的β -O-4芳醚键将上述三种木质素单体两两结合形成二聚体结构, 来反映该成键效应的影响。
如图4所示, 将木质素单体以β -O-4这种结合方式进行组合, 并进行结构优化和拉曼光谱计算, 计算结果如图5和图6所示。 从图5和图6可以看出, 同种或者异种木质素单体聚合后的拉曼光谱特征峰也大体相同, 在1 330、 1 642和1 714 cm-1附近都有明显特征峰, 且在1 642和1 714 cm-1处的特征峰强度最大, 最为明显。 该结果与单体的特征峰位置接近, 说明β -O-4连接方式对这几个振动模式的影响不大, 故拉曼光谱在1 330、 1 630和1 714 cm-1这些位置的特征峰可以作为识别检测物质中存在木质素大分子的有效判据。 其中S-S二聚体和G-G二聚体在这两处特征峰的强度明显高于H-H二聚体, 由于1 642 cm-1附近处的特征峰振动是芳香环骨架的弯曲振动导致的, 而芳香环骨架两侧的氧甲基数量对其特征峰的强度造成一定影响, 所以S-S二聚体和G-G二聚体在1 642和1 714 cm-1这两处的特征峰强度会大于H-H二聚体。
 | 图5 同种木质素单体的二聚体拉曼光谱 (a): H-H型二聚体; (b): G-G型二聚体; (c): S-S型二聚体Fig.5 Dimer Raman spectrum of two identical lignin units (a): Combination of H and H; (b): Combination of G and G; (c): Combination of S and S |
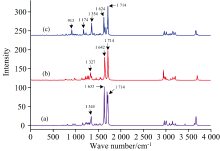 | 图6 异种木质素单体的二聚体拉曼光谱 (a): S-H型二聚体; (b): G-H型二聚体; (c): S-G型二聚体Fig.6 Dimer Raman spectrum of two different lignin units (a): Combination of S and H; (b): Combination of G and H; (c): Combination of S and G |
对比图6异种木质素单体二聚体拉曼光谱, 各二聚体在波数1 714 cm-1处都有最强的拉曼信号, 振动归属为碳碳双键伸缩振动, 且该拉曼谱峰波数与单体光谱基本保持了一致。 对比图5中第二强度特征峰波数位置, H-H二聚体、 G-G二聚体、 S-S二聚体其特征峰波数分别为1 656、 1 642和1 624 cm-1, 特征峰随着甲氧基团数量增加发生相应的红移, 这与三种木质素单体的特性保持一致。 而在图6中, 相应的谱峰则产生了劈裂, 并且劈裂的双峰与其所含木质素单体成分相对应。 故对于木质素大分子聚合体来说, β -O-4连接方式对碳碳双键伸缩振动模式的影响不大, 也不影响单体中甲基对芳香环骨架振动的能量调制效果, 因此可以通过检测这两个特征峰来表征木质素大分子, 并且进一步的还可以根据1 642 cm-1谱峰的劈裂情况来判断其中所含有的三种基本单体的相对丰度。
同时, 在异种木质素单体二聚体拉曼光谱中, G-H二聚体、 S-H二聚体、 S-G二聚体在1 327、 1 345和1 354 cm-1也有明显特征峰的出现。 这三处特征峰的振动归属相同, 都是甲氧基上碳氢键摇摆振动, 但是与图5和图6中相应谱峰的位置并不能完全对应, 说明该振动模式受到β -O-4连接方式的影响较大, 故仅可以将其作为木质素大分子的一个辅助判据, 而不能通过该谱峰有效判断各木质素单体的成分比例。 在实际情况中, 由于不同连接方式和不同单体配对方式的影响, 该波数附近受到多个相近拉曼信号的叠加, 很可能会在拉曼光谱上形成一个包络结构。
对比文献[11-13, 20]实验中的有关木质素拉曼光谱的数据, 本文仿真结果在谱峰位置上有少许误差, 但是振动归属都基本吻合, 文献中芳香环振动对应的拉曼信号为1 610 cm-1附近, 碳碳双键的拉曼信号为1 660 cm-1附近, 其中芳香环拉曼信号在不同样品中特征峰信号虽然较强, 但是谱峰最高点位置、 半高宽、 形状等参数会随样品种类改变或测量植物部位改变出现略微变化, 因为不同植物中不同木质素单体的含量比例会发生变化, 故产生这一现象与本文中结论吻合。 文献中测量碳碳双键信号时频率较为稳定, 不会随着样品变化或测量部位转移而发生大的改变。 本仿真方法通过分析拉曼信号的振动特性, 能够有效解释实验测量信号的变化规律和物理机制, 证明了本方法的有效性, 并且为木质素的拉曼光谱鉴别提供了理论指导, 可以对不同植物的木质素拉曼光谱分析提供一定参考。
通过对三种木质素单体的第一性原理仿真计算得到了G、 S、 H型木质素单体的基本构型、 轨道能级和电子空间分布, 并根据分子振动模式特征计算了各单体的拉曼光谱。 本文对比了三种单体的拉曼特征谱峰及其振动归属, 说明了其主要特征峰的异同, 并根据分子结构特征和振动能量的差异给出了解释。 最后本文以β -O-4连接方式计算了同种和异种单体组合得到的二聚体拉曼光谱, 并结合参考文献的实验测量结果, 对木质素大分子的拉曼特征信号的成因进行了理论分析, 并给出了光谱分析的信号判据。
在木质素单体和二聚体的拉曼光谱信号中, 信号强度最好的两个特征峰位置分别是1 712和1 642 cm-1, 1 712 cm-1振动归属碳碳双键伸缩振动, β -O-4连接方式对该谱峰无显著影响, 因此该振动归属引起的谱峰可以作为木质素大分子存在的一个主要判据。 1 642 cm-1附近对应的振动模式为芳香环骨架的弯曲振动。 该谱峰的频率漂移可以反映甲基对芳香环振动能量的调制效果, 并且β -O-4连接方式对该特征峰的影响不大, 因此根据1 642 cm-1附近特征峰的劈裂情况可以有效反映木质素大分子中三种单体的相对含量。 最后, 位于1 352 cm-1附近的特征峰主要由碳氢键的摇摆振动产生, 并且会受到单体种类和聚合连接方式的共同影响, 因此在木质素大分子中往往以信号包络的形式存在, 引起这三处特征峰的的振动归属在对比文献中都能对应, 故可以作为木质素大分子的一个辅助判据。
上述研究成果是对大分子拉曼光谱仿真分析方法的一种有益探索, 也可以为不同植物的木质素拉曼光谱分析提供一定参考。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|