作者简介: 程昌鸿, 1999年生,安徽理工大学材料科学与工程学院本科生 e-mail: chengchanghong2021@163.com
工业染料的大规模生产和广泛应用给地球生态带来了相当大的影响, 对水环境污染非常严重, 而传统色谱和光谱工具难以检测到微弱的光谱和化学信息, 因此开发便携快速的检测技术至关重要。 表面增强拉曼光谱(SERS)是一种与纳米技术相结合的新型分析技术, 可以实现单分子量级化学物质的检测, 但潜力容易受到SERS 基底的增强能力、 稳定性等普适性问题限制。 研究提出了一种简单而通用的策略, 制备了一种基于疏水性有机半导体双(二氰基亚甲基)-封端-二噻吩并[2,3-d; 2',3'-d]苯并[2,1-b; 3,4-b']-二噻吩(4CN-DTmBDT)薄膜为衬底的新型SERS复合基底。 首先通过旋涂法制备有机半导体衬底, 该π共轭有机半导体具有分子结构可控、 生物相容性、 光电特性可微调、 成膜形态参数可控等优势, 衬底表面具有疏水性使纳米银粒子(AgNPs)在其表面形成紧密咖啡环, 制备有机半导体-纳米银SERS复合基底, 探究基底拉曼信号的增强效果。 同时提出了一种该有机半导体与纳米银粒子的协同增强机制, 并对增强能力与增强机理进行了相关研究。 结果表明, 紧密咖啡环的形成减小了银纳米颗粒之间的空间, 检测时通过浓缩分析物, 从而增强了热点效应。 对以有机染料为探针分子罗丹明6G(R6G)的检测限低至1×10-8 mol·L-1, SERS增强因子(EF)达1.30×106, 对于疏水性更优异的PDMS与纳米银粒子复合基底检测限为1×10-5 mol·L-1, 说明单独的纳米银粒子对R6G探针信号增强能力有限, 同时证明研究采用的有机半导体与银纳米粒子之间通过协同效应进一步显著提升基底拉曼信号, 而且灵敏度高、 重复性好。 该SERS复合基底对1×10-4和1×10-8 mol·L-1 R6G染料检测的相对标准偏差(RSD)分别为8.3%和4.7%。 实验表明该有机半导体-纳米银复合基底在废水中染料痕量分析领域具有良好的应用潜力。
Large-scale production and wide application of industrial dyes have considerably impacted the Earth's ecology. Water pollution is very serious. Traditional chromatographic and spectral tools cannot detect weak spectral and chemical information. Therefore, the development of portable and rapid detection technology is essential. Surface-enhanced Raman spectroscopy (SERS) is a new analytical technique combined with nanotechnology, which can realize the detection of single molecular weight chemical substances. However, the potential is easily limited by the universality of SERS substrate enhancement ability and stability. In this study, a simple and general strategy was proposed to prepare a hydrophobic organic semiconductor bis (dicyanomethylene)-end-capped-dithieno [2,3-d; 2',3'-d] benzo [2,1-b; 3,4-b']-dithiophene (4CN-DTmBDT) film is a new SERS substrate. Firstly, the organic semiconductor substrate was prepared by the spin-coating method. The π-conjugated organic semiconductor has the advantages of controllable molecular structure, biocompatibility, fine-tuning of photoelectric properties and controllable film-forming morphological parameters. The substrate surface has hydrophobicity, which makes silver nanoparticles (AgNPs) form a tight coffee ring on its surface. The organic semiconductor-nano silver SERS composite substrate was prepared to explore the enhancement effect of the Raman signal of the substrate. This study proposed a possible synergistic enhancement mechanism between the organic semiconductor and silver nanoparticles, and the enhancement ability and mechanism were studied. The results showed that the formation of tight coffee rings reduced the space between silver nanoparticles, and the hot spot effect was enhanced by concentrating the analyte. The detection limit of rhodamine 6G (R6G) with organic dye as the probe molecule was as low as 1×10-8 mol·L-1, and the SERS enhancement factor (EF) was as high as 1.30×106, while the detection limit of PDMS and silver nanoparticles composite substrate with better hydrophobicity was 1×10-5 mol·L-1. At the same time, it was proved that the substrate Raman signal was further enhanced by the synergistic effect between the organic semiconductor and silver nanoparticles in this study, the sensitivity was high, and the repeatability was good. The relative standard deviations (RSD) for detecting 1×10-4 and 1×10-8 mol·L-1 R6G dyes were 8.3% and 4.7%, respectively. Experiments show that the organic semiconductor-nano silver composite substrate has good application potential in trace analysis of dyes in wastewater.
工业染料的大规模生产和广泛应用给地球生态带来了相当大的影响, 对水环境污染非常严重, 危害整个生态系统和人类身体健康[1, 2]。 然而痕量染料组分的检测和鉴定极具挑战性, 传统色谱和光谱工具难以检测到微弱的光谱和化学信息[3]。 表面增强拉曼光谱(surface-enhanced Raman spectroscopy, SERS)散射具有高灵敏度[4]、 高重复性[5]和高增强能力[6]等优势, 可以作为污染物检测的有力工具, 对废水中有机染料的检测具有重要的应用价值[1]。 SERS检测核心技术是制备良好稳定性、 高灵敏度基底材料[7, 8]。 常用的传统贵金属基底材料如金、 银等, 由于不能对目标分子进行特异性识别, 且存在易氧化、 成本高、 重复性差、 光谱稳定性差等问题[7], 限制了SERS检测技术在实际应用中的发展潜力[9]。
现有报道的各种SERS活性材料中, 无机半导体因具有带隙可调、 激子形成稳定和激发波尔半径较大等独特性质而引起了越来越多的关注[8, 9, 10, 11]。 然而单一无机半导体基底的增强能力弱于贵金属及过渡金属的基底[12]。 因此, 通常将CuTe[13],
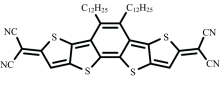
本工作提出一种简单通用的策略, 采用旋涂法制备疏水性有机半导体4CN-DTmBDT(分子结构如图1)衬底, 在其表面使银纳米粒子(silver nanoparticles, AgNPs)聚集形成紧密咖啡环, 制得有机半导体-纳米银新型复合SERS基底。 选用罗丹明6G(Rhodamine 6G, R6G)染料作为探针分子, 滴加在制备好的有机半导体复合基底上进行SERS检测, 探究有机分子半导体与纳米银复合SERS基底拉曼增强效果。 本研究为检测水体环境中的痕量污染物提供了一种简单可靠的方法。
Tecnai G220透射电子显微镜(美国FEI公司); KW-4A旋转涂膜机(上海鑫有研电子科技有限公司); Omini-λ5008i光栅光谱仪(北京卓立汉光仪器有限公司); iVac-316-CCD 安道尔CCD相机(北京先锋泰坦科技有限公司); Laser785-5HS 785 nm 激光器、 RPB-785-1.5-SS光纤探头(上海如海光电科技有限公司); UV1901PC 紫外-可见分光光度计(上海奥析科学仪器有限公司); S-3000N扫描电子显微镜(上海天美仪拓实验室设备有限公司)。
甲苯(C6H5CH3, 分析纯)、 柠檬酸钠(C6H5Na3O7, 分析纯)、 硝酸银(AgNO3, 分析纯)、 罗丹明6G(R6G, 分析纯)均购自国药集团化学试剂有限公司。 聚二甲基硅氧烷(PDMS, 预聚体)和Sylgard 184(固化剂)购自上海道康宁有限公司。 双(二氰基亚甲基)-封端-二噻吩并[2, 3-d; 2', 3'-d]苯并[2, 1-b; 3, 4-b']-二噻吩(4CN-DTmBDT, 夏德斌合成[20]); 实验用水为去离子水。
采用Lee-Meisel法(化学还原法)制备AgNPs[21]。 在250 mL三口烧瓶中加入36 mg AgNO3和200 mL去离子水, 在油浴加热和磁性转子搅拌条件下至沸腾, 在剧烈搅拌条件下将4 mL质量分数为1%的柠檬酸钠水溶液迅速加入, 保持微沸状态搅拌加热1.5 h, 然后停止反应, 反应物自然冷却至室温, 将产物以10 000 r·min-1的转速离心五分钟, 沉淀物分散在4 mL水溶液中, 形成纳米银溶胶。
有机半导体薄膜基底制备。 称取0.064 7 g有机半导体溶解在5 mL甲苯中, 搅拌10 min得到有机半导体溶液。 将载玻片放置于旋转涂膜机片托上, 旋涂转速调至6 000 r·min-1, 匀胶时间为9 s, 用微量移液器移取100 μL有机半导体溶液并迅速滴于载玻片中间, 待载玻片停转后, 得到有机半导体薄膜基底。
在干燥后的有机半导体薄膜基底上制备AgNPs咖啡环。 移取2.0 μL纳米银溶胶并滴于有机半导体薄膜上, 放入鼓风干燥箱中, 在60 ℃下干燥5 min, 即可制得有机半导体-纳米银复合基底。
配制不同浓度梯度的R6G溶液, 取1 μL R6G溶液滴到有机半导体-纳米银复合基底上, 自然干燥, 形成叠加的咖啡环。 对咖啡环进行拉曼光谱检测, 在配备了785 nm激光拉曼光谱仪上进行。 选择激光器功率30 mW、 积分时间5 s和积分次数1次, 对不同浓度染料进行拉曼检测, 并对光谱及特征峰进行拟合处理和分析。
2.1.1 UV-Vis分析
使用紫外-可见分光光度计(ultraviolet and visible spectrophotometry, UV-Vis)测量AgNPs的光谱。 在AgNPs制备时发生的还原反应中, 柠檬酸钠起到还原剂和稳定剂双重作用, 柠檬酸钠和AgNO3反应完成, 通过进一步处理制得的纳米银溶胶呈银灰色。 纳米银溶胶的紫外可见光谱图如图2所示, 图中显示的表面等离子吸收峰波长431 nm, 表明制得的溶液中存在AgNPs[1, 21]; 谱图中431 nm的吸收峰峰形较宽, 表明制得的纳米银溶胶中颗粒粒径分布较宽。 将纳米银溶胶保存在4 mL离心管中, 在阴凉处避光放置半个月后, 其UV-Vis光谱谱图并未发生明显变化, 表明产物稳定性好。
 | 图2 AgNPs的紫外可见光谱图; 插图为纳米银溶胶实物图Fig.2 UV-Vis spectrum of AgNPs; the illustration shows the actual nano-silver sol |
2.1.2 TEM分析
使用透射电子显微镜(transmission electron microscope, TEM)表征AgNPs的分散性和形态。 纳米银溶胶的TEM图像如图3(a)所示, AgNPs分散良好, 粒径分布均匀, 其中球形形貌占多数; 颗粒平均直径为(66.7± 4.0)nm[图3(b)]。
2.2.1 有机半导体衬底表面亲疏水性
为了确定有机半导体表面为疏水性, 通过对有机半导体薄膜进行接触角测量。 将1 μL 1×10-4 mol·L-1 R6G溶液滴在有机半导体薄膜上其接触角如图4所示, 测得表面的接触角105.32°, 衬底表面为疏水性。
2.2.2 咖啡环检测区域
取2.0 μL纳米银溶胶滴在有机半导体薄膜衬底上, 放入鼓风干燥箱中干燥后形成有机半导体-纳米银复合基底, 再将1.0 μL 1×10-3 mol·L-1 R6G溶液滴在有机半导体复合基底上, 继续干燥后形成R6G咖啡环如图5(a)所示。 由图5(b)可见, 咖啡环部分重叠区域的SEM图像, 两环重叠区域边缘明显。
为探究对咖啡环不同区域检测对拉曼信号增强效果的影响, 在图5(a)的5个不同位置进行拉曼信号检测。 由图5(c)可见, 在两环重叠区域观察到的R6G特征峰信号明显, 而在圆环其他重叠区域及中心区域特征峰强度较弱, R6G咖啡环与AgNPs咖啡环完全重叠位置的特征峰远强于R6G咖啡环与AgNPs咖啡环未完全重叠位置的特征峰, 因此拉曼信号在R6G染料上的最佳检测区域为R6G咖啡环与AgNPs咖啡环完全重叠位置, 后续如无特殊说明, 所有数据的检测区域均为R6G咖啡环与AgNPs咖啡环完全重叠位置的拉曼数据。 在没有R6G探针分子的情况下, 在有机半导体-纳米银复合基底上进行了拉曼光谱检测, 其结果如图5(c)中e所示, 说明有机半导体-纳米银复合基底检测波长范围不具有拉曼特征峰, 说明该基底对R6G的SERS光谱没有背景影响, 不会干扰R6G染料的检测。
2.2.3 检测区域的拉曼信号重复性
为了验证该有机半导体复合基底对高浓度和低浓度探针分子检测的可重复性, 在有机半导体-纳米银复合基底上分别滴加1×10-4和1×10-8 mol·L-1 R6G染料为探针分子制备咖啡环, 对AgNPs咖啡环与R6G咖啡环重叠部分[图5(a)中a区域]的八个不同位置(a1, a2, a3, a4, a'1, a'2, a'3, a'4)进行拉曼检测如图6(a)和(c)所示。 测试结果如图6(b)和)d)所示, 在环上a1—a4及a'1—a'4八个位置均可以清楚地识别R6G染料特征峰, 其相对标准偏差(RSD)分别为8.3%和4.7%, 此结果表明, 该有机半导体复合基底检测低浓度检测物的拉曼信号仍具有良好的重复性。
2.3.1 R6G染料溶液与有机半导体衬底拉曼
制备不同浓度梯度的R6G纯溶液, 依次滴加1 μL 1×10-9~1×10-2 mol·L-1 R6G溶液进行拉曼光谱检测。 通过旋涂法制备疏水性PDMS衬底与AgNPs咖啡环的复合基底, 随着R6G纯溶液浓度的降低特征峰基本消失, 当R6G纯溶液浓度低至1×10-6 mol·L-1拉曼信号已检测不出, 其检测限为1×10-5 mol·L-1, PDMS-AgNPs复合基底拉曼光谱图7(a)所示。 在有机半导体衬底上直接滴加R6G溶液形成咖啡环进行拉曼检测, 其检出限可达到1×10-3 mol·L-1, 其拉曼光谱如图7(b)所示。 其增强效果可能主要由于咖啡环的形成浓缩了R6G染料导致, 说明单一有机半导体衬底的拉曼增强效果较弱, 单独的纳米银对R6G探针信号增强能力有限。
2.3.2 有机半导体-纳米银复合基底对R6G的拉曼光谱表征
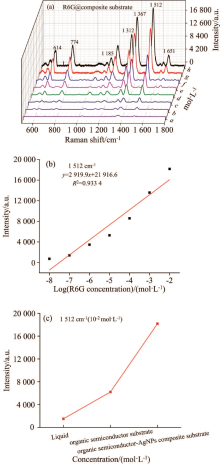
有机半导体-纳米银复合基底的拉曼光谱测试。 将1 μL R6G溶液滴于有机半导体-纳米银复合基底上, 放入鼓风干燥箱中干燥形成咖啡环后对其进行表面增强拉曼光谱检测。 图8(a)为不同浓度R6G探针分子吸附在机半导体-纳米银复合基底上的拉曼光谱。 随着探针分子浓度的降低, SERS信号强度下降趋势明显, 浓度降低到1×10-9 mol·L-1时, 已有部分拉曼峰无法分析。 该基底检测限度为1×10-8 mol·L-1。 谱图中614, 774, 1 185, 1 312, 1 362, 1 512和1 651 cm-1处检测到七个清晰的R6G特征峰[26, 27, 28]。 结果表明有机半导体-纳米银复合基底可以作为SERS活性基底。 为进一步探究SERS信号强度和R6G探针分子浓度的关系, 选择1 512 cm-1的特征峰值研究。 如图8(b)所示, 探针分子的拉曼峰强度与浓度之间呈现出良好的线性相关关系, 拟合之后的线性系数为0.933 4。 图8(a)显示了R6G分子在SERS基底上的检测极限1×10-8 mol·L-1, 计算可得该SERS基底对R6G水溶液的EF为1.30×106, 拉曼增强效果明显。 将R6G溶液、 R6G溶液滴加在有机半导体衬底、 R6G溶液滴加在有机半导体-纳米银复合基底之间在1 512 cm-1左右拉曼检测的特征峰信号强度关系分析, 可以得到检测效果为有机半导体4CN-DTmBDT衬底<PDMS-AgNPs复合基底<有机半导体-纳米银复合基底, 如图8(c)所示。
SERS信号增强可能归因于不同的机制。 从根本上说, 可以用两种被广泛接受的主要增强机制来解释整体的SERS效应: 电磁和化学增强机制[29]。 由于大多数有机半导体的带隙之差较大, 通常实验中785 nm(1.58 eV)激光能量不足以产生, 故电磁对SERS信号的贡献主要来自沉积在有机半导体膜上的岛状AgNPs。 值得注意的是, 有机半导体与AgNPs复合基底的增强因子(106~108)明显高于纯金属的纳米结构基底(104~105)[12], 这些数据表明了有机半导体与AgNPs之间存在对SERS协同增强效应。 因此, 除了电磁增强外, 另一个重要因素可能是化学增强在有机半导体/AgNPs/R6G界面中的电荷转移过程通过放大分子极化性来增强SERS信号。
据以往文献报道, 银的功函数为-4.26 eV。 P型有机半导体4CN-DTmBDT分子的最高占据分子轨道(HOMO)和最低未占据分子轨道(LUMO)能级分别为-5.90和-4.56 eV[20], 带隙值为1.34 eV, 实验中785 nm激光能量足以产生有机半导体的表面等离子体共振。 作为拉曼探针R6G分子的LUMO和HOMO水平位置分别为-3.4和-5.7 eV, 带隙值为2.3 eV(见图9), 在激光下无法激发R6G分子, 其化学增强机制可能有两个过程使电荷从基底转移到R6G。 在激光激发下, 有机半导体衬底产生电子和空穴, 价带中的一个电子首先被激发到银导带。 此时, 在银的价带中也产生了一个空穴, 可以与底层的P通道有机半导体进一步离域和稳定, 将进一步加速电子-空穴对的分离, 并促进电荷转移机制。 然后被激发电子通过共振隧道从衬底快速转移到R6G分子LUMO以上的匹配能级。 另一个过程是由于R6G的LUMO能级和有机半导体的LUMO能量差约为1.16 eV, 有机半导体可以直接将产生的激发电子快速转移到R6G分子LUMO以上的匹配能级。 最终两个过程中产生的激发电子转回有机半导体-纳米银衬底与空穴进行重组。 因此, 该复合SERS基底优越的性能可以归因于AgNPs、 有机半导体4CN-DTmBDT分子和R6G分子的协同作用以及有效的电荷转移。
通过简单通用的策略, 制备了有机半导体-纳米银协同增强拉曼信号的SERS基底, 探究拉曼信号的增强机理, 结果表明, 与传统基底相比疏水性有机半导体与AgNPs制备的复合基底通过协同作用显著提高拉曼信号, 对R6G染料的检测限低至1×10-8 mol·L-1, 基底具有良好稳定性、 高灵敏度。 基于有机半导体为衬底的SERS平台具有良好的检测特性, 表明有机半导体-纳米银复合基底在用于对废水中染料进行痕量分析、 食品安全以及环境监测等诸多领域具有应用潜力。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|