作者简介: 何 遥,女, 1996年生,安徽大学物质科学与信息技术研究院硕士研究生 e-mail: hyaohfei@163.com
在全球范围内频繁发生芬太尼类物质滥用与致死案件, 人体中芬太尼类物质的检测与识别愈发重要。 芬太尼类物质在经过人体一段时间后, 仍有一部分原体随着尿液排出, 因此可通过检测尿液中芬太尼类物质反映其毒品滥用史。 表面增强拉曼光谱(SERS)具有快速、 高灵敏、 易操作等特点, 适合尿液中芬太尼类物质的现场检测与分析。 但尿液中尿素等物质的背景峰与芬太尼类物质SERS特征峰高度重合, 芬太尼类物质特征峰被尿液背景峰所掩盖, 这对尿液中芬太尼类的光谱识别造成了很大的干扰。 结合Voigt线型建立谱峰解析模型, 对尿液与芬太尼类物质重叠部分进行谱峰分析。 针对SERS光谱噪声与荧光等因素对谱峰解析模型的干扰, 采用无约束Nelder-Mead算法对模型进行优化与计算, 利用该算法对迭代参数初始值不敏感的特点, 提高谱峰解析模型的准确度。 根据SERS光谱半峰宽的特征对解析峰集合进行筛选, 对SERS光谱的尿液背景峰进行扣除, 以还原芬太尼类SERS光谱1 000与1 030 cm-1处谱峰特征。 实验结果与现象表明, 利用Voigt线型建立的谱峰解析模型对尿液中芬太尼类SERS光谱拟合度均达到99%以上, 能够通过解峰集合的筛选还原尿液中芬太尼类SERS光谱特征, 还原光谱与芬太尼类特征峰的半峰宽与峰比例等特点均高度一致。 在空白尿液SERS光谱进行解析时, 其解析峰集合中不含有芬太尼类物质的特征谱峰, 可以有效区分空白尿液与含芬太尼类物质尿液。 利用相似系数(HQI)对还原光谱片段(935~1 100 cm-1)进行识别, 能有效区分尿液中奥芬太尼、 呋喃芬太尼、 乙酰芬太尼三种芬太尼, 并提升光谱之间的区分度。 该解析模型有望为尿液中芬太尼类的识别与判断提供解决实际问题的途径。
Fentanyl substance abuse and death cases frequently occur worldwide, and the detection and identification of fentanyl substances in the human body are becoming increasingly important. After some time in the human body, some of the fentanyl substances are still discharged with urine, so the history of drug abuse can be reflected by detecting fentanyl substances in the urine. Surface Enhanced Raman Spectroscopy ( SERS ) is fast, sensitive and easy to operate, which is suitable for the field detection and analysis of fentanyl in urine. However, the background peaks of urea and other substances in urine are highly coincident with the SERS characteristic peaks of fentanyl, and the characteristic peaks of fentanyl are covered by the background peaks of urine, which causes great interference with the spectral identification of fentanyl in urine.In this paper, the spectral peak analysis model is established based on the Voigt line, and the spectral peak analysis of the overlapping part of urine and fentanyl is carried out. Because of the interference of SERS spectral noise and fluorescence on the peak analytical model, the unconstrained Nelder-Mead algorithm is used to optimize and calculate the model. The algorithm is insensitive to the initial value of iterative parameters to improve the accuracy of the peak analytical model. According to the characteristics of the half-peak width of the SERS spectrum, the analytical peak set was screened, and the urine background peak of the SERS spectrum was deducted to restore the spectral peak characteristics of the fentanyl SERS spectrum at 1 000 and 1 030 cm-1.The experimental results and phenomena show that the spectral peak analysis model established by the Voigt line shape has a fitting degree of more than 99% for the SERS spectrum of fentanyl in urine and can restore the SERS spectrum characteristics of fentanyl in urine through the screening of the peak solution set. The characteristics of the half-peak width and peak ratio of the reduced spectrum and the characteristic peaks of fentanyl are highly consistent. When the SERS spectrum of blank urine is analyzed, the analytical peak set does not contain the characteristic peaks of fentanyl substances, which can effectively distinguish blank urine from urine containing fentanyl substances. The reduced spectral fragment (935~1 100 cm-1) was identified by the hit quality index (HQI), which can effectively distinguish Ofentanyl, Furanyl and Acetylfentanyl in urine and improve the discrimination between spectra. This analytical model is expected to provide a way to solve practical problems for the identification and judgment of fentanyl in urine.
1972年, 美国食品药品监督管理局正式批准芬太尼为静脉麻醉剂[1]。 近年来, 由于芬太尼类物质具有更强麻醉作用, 早已替代传统毒品成为全球流行的第三代毒品。 2017年芬太尼成为美国药物滥用致死排行榜榜首, 致死人数高达2.9万人, 是海洛因的1.8倍[2]。 据美国国家法医实验室信息系统统计, 仅2019年芬太尼类出具报告100 378例, 比2018年增加了12%[3]。 在2012年至2015年国内累计仅发现6份芬太尼类物质, 但在2016年却发现了66份芬太尼类物质, 是前三年的11倍[4]。 我国在2018年已经有25种芬太尼类物质被列入管制的新精神活性物质, 占所有新精神活性物质的15%[5]。 走私与生产芬太尼类物质的案件数在我国不断攀升, 而且新型芬太尼类物质也不断涌现, 严重威胁公共安全与人们健康, 因此检测与分析此类毒品具有重要意义。
芬太尼类物质经过人体吸收与代谢后[6], 仍然会存在一定原体随着尿液排出。 表面增强拉曼光谱(surface enhanced Raman spectroscopy, SERS)可以反映待测物的信息以进行物质的识别。 利用金、 银等贵金属纳米材料作为增强基底, 目标物的SERS信号可以百万倍的放大, 甚至能够达到超灵敏的单分子检测水平, 因此可以利用SERS对复杂体系中的痕量物质进行检测。 SERS增强原理普遍认为有两种: (1)基于光-贵金属纳米材料的光学特性引起电磁场增强的物理增强机制[7, 8]; (2)基于分子-贵金属纳米材料相互作用而产生的更具分析物特异性的化学增强机制[9, 10]。 一般情况下, 化学增强由于其作用效果较弱。 化学增强中主要的电子效应被理解为非共振变化、 分子激发共振增强和电荷转移共振的累积而导致分子极化率的改变。 因此, 影响SERS光谱谱峰特征的主要因素为分子电子结构、 振动模式与振动频率。 然而尿液背景峰与芬太尼类物质SERS光谱特征峰存在高度重叠, 芬太尼类SERS光谱强特征峰1 000与1 030 cm-1处谱峰特征几乎完全被尿液背景峰掩盖, 这对尿液中芬太尼类物质SERS光谱的识别造成很大的干扰。 尿液背景峰的扣除与芬太尼类SERS光谱特征还原对光谱识别具有重要意义。
通常分析复杂混合物成分时会使用谱峰分解模型, 再根据解析出的谱峰进行分析与计算[11]。 计算时, 线型以及迭代算法的选择较为重要, 其将直接影响解析模型的速度与正确度。 通常解析模型所使用的线型为高斯, 迭代算法为非线性最小二乘法[12]。 但这并不适合SERS光谱的谱峰解析, 因为SERS光谱具有较强的噪声与荧光干扰[13], 且使用平滑去噪算法[14, 15]会影响其解析结果正确性。 非线性最小二乘法进行迭代计算时受约束条件与初始值预估等诸多因素干扰, 容易出现无法求解的现象。 尿液中芬太尼类SERS光谱重叠严重, 过度使用平滑去噪会对谱峰解析造成影响, 无法求解出准确结果, 影响后续尿液背景扣除与芬太尼类SERS光谱特征还原。 噪声与荧光信息对SERS光谱的干扰, 导致其很难对迭代参数的初始值进行准确预估, 这直接影响谱峰分解的速度与精确度[16]。
选择Voigt线型建立谱峰解析模型, 对尿液与芬太尼类重叠SERS光谱片段935~1 100 cm-1进行谱峰分析。 为解决SERS光谱具有噪声与荧光干扰等问题, 选择对初始值并不敏感的无约束非线性优化算法(Nelder-Mead算法)[17]作为参数迭代的算法。 利用其对SERS光谱进行谱峰分解, 防止出现不收敛与过拟合的情况。 根据SERS光谱特征半峰宽与峰高的特征对解析峰集合进行筛选, 设计合适的条件对含芬太尼类SERS光谱的尿液背景峰进行扣除, 并还原芬太尼类SERS光谱特征。 利用相似系数(hit quality index, HQI)作为光谱判别条件, 对还原后的SERS光谱片段进行识别, 区分尿液中奥芬太尼、 乙酰芬太尼与呋喃芬太尼三种芬太尼。
在SERS光谱中, 尿液与芬太尼类在1 000与1 030 cm-1两处特征峰高度重合。 芬太尼类物质主要特征峰几乎被尿液背景峰所覆盖。 为了提取出芬太尼类SERS光谱, 利用算法对尿液背景峰进行扣除, 还原芬太尼类物质原本SERS光谱特征, 建立尿液与芬太尼类SERS光谱解析模型, 通常使用高斯线型进行谱峰解析, 拉曼谱峰实际线型更贴近劳伦兹线型[18]。 但是由于检测仪器与样本的不同, 实际SERS光谱特征峰更接近Voigt线型。 Voigt线型定义如式(1)所示[19]
式(1)中, α 为高斯-劳伦兹系数; β 为峰高; x为拉曼位移; ω 为峰位; φ 为半峰宽, 可直接影响Voigt线型。 待解析光谱则可视为n个Voigt峰之间的叠加。 如式(2)所示
式(2)中, θ i为解析模型中第i Voigt线型的需要求解的参数。 针对以上解析模型, 一般使用非线性最小二乘法对n以及需要求解的参数进行迭代, 寻找其最优解。 由于噪声干扰与荧光背景, 结合对初始值不敏感的无约束非线性优化算法(Nelder-Mead算法)进行参数迭代。
尿液与芬太尼类SERS光谱谱峰大多为单峰与重叠峰。 在进行单峰谱峰解析时, 光谱片段噪声与荧光背景不多, 可直接对其进行迭代计算。 但尿液中芬太尼类SERS光谱1 000与1 030 cm-1处为重叠峰。 在进行重叠峰分解时, 其为多个谱峰的叠加且噪声等干扰较多, 不能单独进行分解, 需对其进行联合分解, 并考虑其重叠部分。 本文提出在进行谱峰解析前直接设定需要解出谱峰的个数N, 并对其进行迭代参数粗略的预估与设计。 对重叠峰的谱峰分解步骤如下所示:
(1)载入光谱片段, 去基线, 并对处理后的光谱进行峰值归一化;
(2)初始化分解峰集合Ω ={}与光谱解析峰的个数N=1;
(3)对ω (峰位)、 φ (半峰宽)与α (高斯-劳伦兹系数)进行预估;
(4)利用Nelder-Mead算法进行迭代, 并计算拟合光谱与原始光谱的误差, 然后将拟合峰存入Ω 中;
(5)若误差小于0.1, 则其算法结束, 集合Ω 即为背景光谱的所有解析峰, 若误差大于0.1, 则需拟合峰的个数N+1, 返回步骤(3)继续算法。
在步骤(3)中对ω (峰位)的预估的方法与峰个数N与光谱起始位置有关, 将光谱平均分成N等份, 以分割线的位置作为ω (峰位)的预估值。 等份的长度作为φ (半峰宽)的预估值。 α (高斯-劳伦兹系数)初始值为0.4。
为了还原其中芬太尼类物质SERS特征峰, 不仅需要对其进行谱峰分解, 还需扣除尿液背景峰。 在进行谱峰解析后, 根据拉曼特征峰的特点对分解峰进行滤除, 自动扣除尿液背景干扰, 还原芬太尼类SERS光谱。 利用SERS光谱特征半峰宽对芬太尼类光谱进行还原步骤如下所示:
(1)载入光谱片段, 并对光谱进行谱峰解析, 得到其分解峰集合Ω ;
(2)计算原始光谱1 000与1 030 cm-1处半峰宽x1与x2;
(3)若集合Ω 中解析峰半峰宽xΩ ∈ [x2, x1], 则该分解峰计入芬太尼类SERS光谱分解峰中, 反之则计入尿液背景峰中;
(4)对芬太尼类SERS光谱分解峰集合进行拟合, 并在标准品数据库中进行搜索, 用相似系数HQI作为物质分类的标准, HQI计算公式如式(3)所示:
(5)遍历光谱库中标准品SERS光谱后, 匹配系数最大且高于85%的标准谱为最终结果。
式(3)中, A为待识别光谱数据, B为数据库中光谱数据, A与B的第一行为光谱拉曼位移第二行为光谱相对位移。
SERS增强基底由安徽中科赛飞尔科技有限公司提供。 呋喃芬太尼、 乙酰芬太尼与奥芬太尼均来自安徽省公安厅物证鉴定中心。 在整个实验过程中使用的超纯水为18.25 MΩ · cm。
尿样来自于中国科学院合肥肿瘤医院, 分别将三种芬太尼加入到人的尿样中, 分别制备成含有50, 10, 1和0 mg· kg-1三种芬太尼类物质的模拟尿样。
手持式拉曼光谱仪由安徽中科赛飞尔科技有限公司提供, 具体配置为: 焦距为7.5 mm, 光谱分辨率为7 cm-1, 光斑范围1 μ m2, 激光波长785 nm, 最大功率为500 mW。 数据分析所用软件为: Matlab 2016b。 电脑配置为: Intel core i7-9750 H。
在进行谱峰分解时, 需要选择合适的线型对光谱片段进行解析。 线型的选择与解析结果密切相关。 通常使用高斯线型对光谱谱峰进行解析, 但是其拟合效果较差, 无法较精准拟合原始光谱, 容易出现峰位偏移与峰形畸变。 检测仪器与检测样本的不同, 洛伦兹线型并不能还原芬太尼类标准品的拉曼特征, 几乎无法对模型进行求解。 但高斯线型与劳伦兹线型特点相结合的Voigt线型对谱峰进行分解, 其对尿液中芬太尼类物质特征有较为准确的解析, 它能够扣除尿液背景峰, 还原芬太尼类物质拉曼特征峰。 三种函数线型如图2所示。
 | 图2 Voigt线型、 洛伦兹线型和高斯线型三种函数线型的对比Fig.2 Comparison of the Voigt, Lorentz and Gaussian line types of functions |
由图2可以看出这三种线型的半峰宽、 峰高与峰位一致时, 差距主要在谱线下半部分。 谱线的半峰宽主要分为均匀半峰宽、 非均匀半峰宽和综合半峰宽这三大类。 洛伦兹线型属于均匀半峰宽的谱线轮廓, 是理论中符合拉曼光谱特征的线型。 高斯线型是多普勒频移效应导致的非线性半峰宽, 是大部分谱峰解析时使用的线型。 Voigt线型则是典型的综合半峰宽, 其谱线展宽并不是单一存在而是多种的叠加, 但高斯线型与洛伦兹线型是单一谱线半峰宽的线型。 然而在实验中导致谱线展宽的因素并不唯一, 所以选择Voigt线型设计谱峰解析模型。 洛伦兹线型在此解析方法中无法得出结果, 图3仅展示高斯线型与Voigt线型的解析结果对比图。
 | 图3 高斯线型与Voigt线型的解析结果对比图Fig.3 Comparison of the resolution results for Gaussian and Voigt line shapes |
通过图3可以看出使用高斯线型与Voigt线型对尿液中奥芬太尼SERS光谱同一片段进行谱峰解析时, 虽然两者拟合光谱与原始光谱相似度均超过0.99, 但是在上图中也能明显看出Voigt线型的拟合效果明显优于高斯线型的拟合效果, 高斯线型拟合结果明显出现峰位的偏移。 且在解析峰集合中高斯线型解析结果中也并不含有奥芬太尼特征的解析峰, 而Voigt线型解析峰中包含奥芬太尼特征的解析峰。 这为尿液基质背景峰的扣除以及芬太尼类特征峰的还原提供了基础条件。
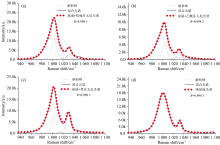
尿液背景峰与芬太尼类拉曼特征峰在1 000与1 030 cm-1几乎完全重合。 而在芬太尼类SERS光谱中特征峰也在1 000与1 030 cm-1处, 由此对尿液中芬太尼类混合SERS光谱高度重合部分935~1 100 cm-1进行谱峰解析。 解析结果大致如图4所示。
由图4可知, 在进行谱峰分解后得出的是一个Voigt峰的集合。 集合中包含芬太尼类物质拉曼峰和尿液背景峰。 根据拉曼峰特征对Voigt峰的集合进行筛选, 提取其中芬太尼类SERS光谱, 扣除尿液背景峰。 通过分析尿液与芬太尼类标准品SERS光谱1 000与1 030 cm-1两处拉曼特征峰进行分析, 发现其在半峰宽处有较大的差异。 根据这一特点设置条件, 对Voigt峰的集合进行筛选。
首先计算原始光谱1 000与1 030 cm-1处半峰宽x1与x2, 将集合Ω 中解析峰半峰宽xΩ 与其进行对比, 若解析峰半峰宽xΩ 在x2与x1之间, 则该分解峰计入芬太尼类SERS光谱分解峰中, 反之则为尿液背景峰。 最后对芬太尼类还原光谱进行拟合, 作为扣除尿液背景后还原的芬太尼类光谱。 其还原效果如图5所示。
根据图5可以看出, 尿液中芬太尼类SERS光谱还原效果较好。 还原后的芬太尼类光谱与标准品SERS光谱相似度均在95%以上, 且1 000与1 030 cm-1两处光谱的半峰宽与峰比例几乎一致, 符合芬太尼类SERS光谱特征。 因此, 可利用还原后芬太尼类SERS光谱进行光谱类别判断。
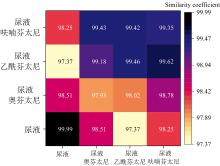
由于尿液背景中与芬太尼类强信号峰1 000与1 030 cm-1高度重合, 直接对两种物质进行建库与识别时, 仅依靠峰位的识别方法已经无法进行区分。 而使用相似度识别方法也并没有较大的差距, 光谱之间的相似度均达到99%以上。 对于仪器分辨率不高的手持式拉曼而言几乎无法进行区分。 同样, 与芬太尼类标准品SERS光谱进行匹配时, 其也几乎无法准确识别。 尿液中芬太尼类SERS光谱匹配情况如图6所示。
根据图6可知, 尿液中芬太尼类SERS光谱的识别效果并不理想。 对光谱强信息片段进行谱峰分解并还原的光谱进行种类识别发现, 其识别效果有一定程度上的提高。 虽然仍然无法通过峰位的方法进行识别与区分, 但是由于其高度还原了芬太尼类SERS光谱的特征峰特征, 包括半峰宽、 峰高以及峰比例。 因此可以利用芬太尼类标准品SERS光谱进行建库, 再利用相似系数作为判断依据进行识别。
尿液中芬太尼类SERS光谱识别步骤如下所示。 首先使用芬太尼类标准品SERS光谱数据进行建库, 并对其进行平滑去噪处理; 接着对待识别光谱进行谱峰解析并扣除尿液背景还原SERS光谱特征; 然后进行相似系数计算; 最后得出对应芬太尼类别。
根据图7可知, 相比未进行还原的尿液中芬太尼类SERS光谱而言, 其识别效果有一定程度的改善。 且具有一定的区分度, 在一定程度上可以减少分辨率较低的手持式拉曼检测仪数据识别的问题。 在对数据分解还原的过程中, 对于纯尿液光谱数据而言, 还原光谱仍然保留纯尿液光谱特征, 分解峰集合中。 这表明所建立的数学模型适合进行尿液中某些物质的SERS光谱识别与分析。
针对上述中纯尿液与尿液中芬太尼类SERS光谱进行谱峰分解时产生的不同情况进行分析, 在纯尿液进行1 000与1 030 cm-1处进行谱峰分析时, 其并不会分解出含有芬太尼类的谱峰。 而尿液中含有芬太尼类物质时, 则可利用谱峰解析出含芬太尼类光谱的特征峰, 并根据还原光谱对芬太尼种类进行有效区分。 针对此种情况将从以下两个方面进行探究: 一是混合光谱, 二是分子振动。
在进行尿液中芬太尼类SERS光谱分析时, 发现尿液中不同种类的芬太尼其特征峰1 000与1 030 cm-1的半峰宽与峰高之间具有一定差距。 芬太尼类标准品SERS光谱的半峰宽和峰高与纯尿液本身具有较大的差距。 尿液中的芬太尼类SERS光谱在半峰宽与峰高间也存在着较大的差异。 纯尿液拉曼特征峰与芬太尼类拉曼特征峰的差异如图8所示。
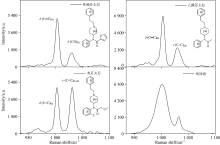 | 图8 尿液与芬太尼类拉曼特征峰及其振动模式Fig.8 Raman characteristic peaks of urine and fentanyl and their vibration modes |
由图8可知, 纯尿液SERS光谱在1 000 cm-1处特征峰半峰宽较宽, 而芬太尼类在此处半峰宽都较窄。 且纯尿液与芬太尼类SERS光谱1 000与1 030 cm-1之间的峰高比例也不同。 而尿液与芬太尼类物质不会发生新的化学反应, 所以当两种物质混合在一起时光谱也会具有半峰宽与峰高上的特征。 而谱峰分解模型中半峰宽与峰强对解析结果有影响, 所以采用此方法可以还原芬太尼类拉曼特征峰, 扣除尿液背景干扰。 芬太尼类SERS光谱特征峰半峰宽与峰高不同的原因是分子振动模式与振动频率的不同。 图8中包含三种芬太尼1 000与1 030 cm-1处的分子振动模式。 ν 为伸缩振动, δ 为面内变形振动。
由图8可以看出三种芬太尼两处特征峰的振动位置与振动模式均不相同, 乙酰芬太尼1 000 cm-1处谱峰归因于B2上C=C的面内弯曲振动, 1 030 cm-1处谱峰归因于pip上C— C伸缩振动[20]。 呋喃芬太尼分子在1 000 cm-1处则是B1上C=C两个单取代的面内弯曲振动造成的, 1 030 cm-1处的峰位来源于B2上C=C拉伸与C— H弯曲的组合振动[11]。 奥芬太尼其1 000 cm-1处强峰是由B2上C=C的面内振动产生, 1 030 cm-1处则是B1与B2上C=C伸缩组合振动引起。 这种振动模式与位置的差异直接导致SERS光谱的差异, 可通过还原光谱对其进行种类区分。
利用Voigt线型建立谱峰解析模型, 并结合Nelder-Mead算法进行迭代分析, 计算出最优分解峰集合。 针对SERS光谱具有噪声与荧光背景等问题, 使用对初始值不敏感的无约束非线性优化算法对模型进行解析, 避免出现过拟合与解不出的问题。 针对由于尿液中尿素等物质背景峰与芬太尼类SERS特征峰高度类似而产生的光谱叠加问题, 对尿液中芬太尼类拉曼光谱935~1 100 cm-1光谱片段进行谱峰解析, 以还原芬太尼类拉曼光谱1 000与1 030 cm-1处拉曼谱峰特征, 与芬太尼类标准品拉曼光谱相似度均超过95%。 根据芬太尼类拉曼光谱特征峰半峰宽特点, 设计尿液背景扣除与芬太尼类拉曼特征峰还原条件, 对最优分解峰集合中Voigt峰进行筛选与滤除, 最终将符合条件的谱峰拟合作为芬太尼类还原光谱。 利用相似系数HQI进行物质判别依据, 实现了尿液中芬太尼类拉曼光谱识别, 提高了识别的准确度。 此解析体系也可对尿液中或者毛发中冰毒的强信号峰1 000与1 030 cm-1的扣除与还原具有一定的效果, 有望为复杂基质中目标毒物的识别与判断提供解决实际问题的途径。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|