作者简介: 郑培超, 1980年生, 重庆邮电大学光电工程学院教授 e-mail: zhengpc@cqupt.edu.cn
锶元素是人体不可缺少的微量元素, 饮用富锶矿泉水可以为人体补充锶。 目前用于检测富锶矿泉水中锶元素的常规分析方法如原子吸收光谱法、 原子荧光光谱法、 离子色谱法、 电感耦合等离子体-原子发射光谱法/质谱法等, 具有检测灵敏度高、 检测稳定性好的优点, 但是相关仪器体积庞大, 价格昂贵, 能耗高, 有些还需要使用惰性/特殊气体, 不适合现场、 实时和在线连续监测。 因此, 发展小型化、 低成本、 快速的光谱检测对锶元素的有效测量具有重要意义。 溶液阴极辉光放电-原子发射光谱法是近年来发展迅速的水体金属离子测量方法, 具有检出限低、 成本低、 小型化等优点。 因此, 建立溶液阴极辉光放电-原子发射光谱系统, 实现了富锶矿泉水中锶元素的浓度测量。 实验考察了溶液阴极辉光放电装置中放电电流、 溶液流速和pH值等参数对锶的信背比的影响, 确定了定量分析元素锶的最佳实验条件: 溶液流速1.85 mL·min-1、 溶液阴极辉光放电装置的放电电流75 mA, pH 1.0的HNO3作为电解质。 选取波长为460.77 nm的光谱线作为锶元素的分析谱线。 在上述最佳工作条件下对锶的溶液进行测定, 锶元素的发射光谱稳定性为0.52% ( n=21)。 锶的质量浓度在0.1~20 mg·L-1范围内与其发射强度呈线性关系, 线性相关系数为0.999 6。 所建立的溶液阴极辉光放电-原子发射光谱法测得锶的检出限为29 μg·L-1。 采用搭建的溶液阴极辉光放电-原子发射光谱检测系统测量了市场上常见的三种富锶矿泉水, 测量结果与电感耦合等离子体发射光谱法一致。 此外, 该方法对富锶矿泉水的加标回收率为98.8%~107.6%。 结果表明: 溶液阴极辉光放电-原子发射光谱法是测定富锶矿泉水中锶的一种有效方法。
Strontium element is an indispensable trace element in the human body, and strontium rich mineral water is an important means of supplementing strontium in the human body. At present, the conventional analytical methods used to detect strontium elements in strontium-rich mineral water, such as AAS, AFS, IC, ICP-AES/MS, etc., have the advantages of high detection sensitivity and good detection stability. However, these instruments are bulky, expensive, and energy-intensive, moreover some require inert/special gases, which are not suitable for field, real-time and online continuous monitoring. Therefore, it is of great significance to develop a miniaturized, low-cost and rapid spectral detection technology for the effective measurement of strontium. In recent years, Solution cathode glow discharge-atomic emission spectrometry (SCGD-AES) is a rapidly developing for detecting metal elements in an aqueous solution. Here, the SCGD-AES system was established to measure the concentration of strontium in strontium-rich mineral water. The experimental parameters such as discharge current, sample flow rate and pH on the SBR of strontium were investigated, and the optimal experimental parameters for quantitative analysis of strontium were as follows: 1.85 mL·min-1 for the sample flow rate, 75 mA for the discharge current, and the electrolyte acidified to pH 1.0 by HNO3. 460.77 nm was selected as the strontium analytical spectrum line, and the strontium solution was determined under the above optimal working conditions. The emission spectral stability of strontium was 0.52% ( n=21). The strontium concentration shows a linear relationship with its emission intensity in the range of 0.1~20 mg·L-1, and the linear correlation coefficient is 0.999 6. The detection limits of strontium were 29 μg·L-1 for the homemade SCGD-AES. The established SCGD-AES detection system measured three types of strontium-rich mineral water in the market, and the results were agreed with the results of inductively coupled plasma-atomic emission spectrometry. In addition, the recoveries of bottled mineral water are 98.8%~107.6%. The results show that SCGD-AES is an effective method for the determination of strontium in strontium-rich mineral water.
人体微量元素是人类生存和健康的基本需要[1]。 锶(strontium, Sr)元素作为一种必需的微量元素, 在一些疾病的防治中起着重要的作用[2]。 人体中锶含量的不平衡可能会引起许多疾病, 如骨质疏松、 牙齿松软、 认知障碍等[3]。 对于孕妇、 儿童和老年人这几类群体, 可能存在锶缺乏症, 这使他们更容易感染心血管等疾病[4]。 人体从食物和水中提取微量元素, 所以除了每天多餐摄入锶外, 适当饮用富含锶的水, 也可以在一定程度上预防一些疾病[5]。 监测锶元素含量对水质评价, 特别是矿泉水的质量评价具有重要意义。 中国饮用天然矿泉水的锶极限指数为5 mg· L-1, 为保证目前市面上富锶矿泉水质量可靠, 需要对水中的锶测定[6]。
溶液阴极辉光放电-原子发射光谱法(solution cathode glow discharge-atomic emission spectrometry, SCGD-AES)是近年来发展迅速的一种原子光谱技术[7], 具有消耗功耗小(< 75 W), 大气压下空气工作、 多元素同时测量等显著特点[8], 已广泛应用于各种实际样品的检测。 Yu等利用小型化液体阴极辉光放电发射光谱分析系统对盐矿中的K, Ca, Na和Mg等元素进行测定, 得到的结果与ICP所测结果基本一致[9]。 Liu等建立的溶液阴极辉光放电系统来测量锂, 其检出限(detection limits, DLs)为0.2 mg· L-1, 可以有效的测定医疗检验领域实际血清样品中微量元素锂的含量[10]。 Peng等测定了自来水和海水中的Cd, Hg和Pb, 检测灵敏度良好[11]。 而对于检测矿泉水中的元素, SCGD-AES也有着良好的检测性能。 Zhou等向矿泉水中添加一定量的镉、 铜、 铅、 锌, 测量并计算获得了良好的回收率[12]。 在之前的工作中, 我们使用SCGD-AES对中国市场瓶装矿泉水样品中的金属元素(包括Na, K, Ca和Mg)进行了检测。 根据瓶装水SCGD发射光谱的组成和强度的差异, 采用SCGD-AES结合化学计量学方法对中国市场上的7种瓶装水进行了分类[13]。
本文采用SCGD-AES对富锶矿泉水进行锶的检测, 考察了SCGD-AES中溶液流速、 放电电流、 pH值和空间分布等操作参数对锶的光谱信号的影响规律。 在优化的实验条件下, 对系统进行了锶的稳定性测试, 获得了锶的DLs和相对标准偏差(relative standard deviation, RSD)。 最后, 对矿泉水中锶元素做定量检测, 并使用电感耦合等离子体原子发射光谱法(inductively coupled plasma-atomic emission spectrometry, ICP-AES)来验证SCGD-AES对水样的测量结果。
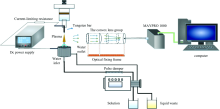
实验装置原理图如图1所示, 其结构与我们之前的实验系统类似[14]。 待测溶液样品在蠕动泵(BT100-2J, Longer, 中国)的带动下通入竖直放置的玻璃毛细管(内径0.38 mm、 外径1.1 mm), 并从毛细管顶部连续溢出, 落在接地石墨电极上。 玻璃毛细管上方竖直放置一根钨棒(底部磨尖)。 直流电源 (额定电流 150 mA, Glassman, 美国) 的正极接入一个阻值为2.7 kΩ 的镇流电阻后连接金属钨棒, 作为放电阳极, 直流电源的负极端连接石墨管作为放电阴极。 在阴阳极之间施加的高电压, 击穿两极间的空气后产生放电等离子体。
等离子体发出的光由光学系统收集后聚焦于光纤的入口处。 光纤的另一端连接到便携式光谱仪(Ocean Optics Maya 2000 Pro)。 光谱仪输出的光谱信号由计算机软件进行分析和处理。 光谱仪的工作软件参数为积分时间300 ms, 平均次数10次, 去除暗噪声和杂散光校正。
实验用锶标准溶液采用SrCl2· 6H2O (≥ 99.5%) 药品按照《化学试剂 杂质测定用标准溶液的制备》(GB/T 602—2002) 进行配置得到1 000 mg· L-1 Sr的标准溶液, 实验中不同浓度的标准溶液采用逐级稀释获得。 所有样品均用硝酸(分析纯)调至pH 1.0。 所用SrCl2· 6H2O由重庆川东化工股份有限公司提供。 所用去离子水(电阻率: 18.25 MΩ · cm)通过超纯水机(Ulupure UIPR-II-10T, 中国)获得。 用pH计(PHS-3E, INESA, 上海, 中国) 测定溶液的pH值。 实际矿泉水从当地超市采购, 所有瓶装水样品用HNO3酸化至pH 1.0, 然后用SCGD-AES进行分析。 “ 岳龙泉” 标注Ylq, “ 圣培露” 标注Spl, “ 巴马活泉” 标注为Bmhq。
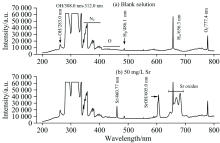
通过测量空白溶液(pH 1, HNO3) 和含锶的标准溶液, 得到200~800 nm波长范围内的光谱信息, 如图2所示。 在图2(a)中, 283.00~312.00 nm属于OH带, 486.10 nm为Hβ 的原子线, 656.30 nm为Hα 的原子线, 777.40 nm为O的原子线。 从图2(b)可以看出, 在空白溶液的基础上生成了两条新的谱线, 其中460.77 nm为锶的原子线。 此外, 在605 nm左右和640~690 nm之间可见分子带, 属于锶的氧化物[15]。 在SrOH (605.00 mm)的情况下, 实验结果存在较大误差, 因为在实际水样中一般是存在许多元素, 而在605.00 nm附近存在较强的背景信号, 影响实际测量结果, 所以后续实验选择460.77 nm进行分析。
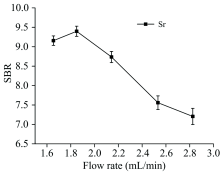
溶液流速对放电等离子体有重要的影响。 本实验中, 当溶液流速低于1.65 mL· min-1时, 进样通道中的水量不足以维持正常放电。 等离子体不稳定, 且间歇猝灭。 这时, 高电压直接作用在玻璃管上, 造成击穿放电的现象, 易对玻璃管造成损伤。 当流速大于2.85 mL· min-1时, 由于流速过快, 等离子体出现不稳定的情况。 因此, 设定流速在1.65~2.85 mL· min-1范围内, 溶液流速对锶信号强度与背景比值(signal-to-background ratio, SBR) 的影响, 如图3所示。 随着流速的增加, SBR呈现先上升后下降的趋势。 当流速为1.85 mL· min-1时, 误差棒较低, SBR值最高, 综合考虑后的最佳流速为1.85 mL· min-1。
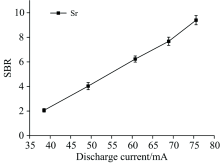
放电电流在等离子体的产生过程中起重要的作用。 当放电电流小于35 mA时, 激发等离子体能量不足, 易造成放电不稳定的现象。 但当放电电流大于80 mA时, 由于溶液的消耗速率超过溶液注入速率, 等离子体产生过程容易中断, 放电阳极金属表面迅速变红, 影响测试结果。 在此, 在流量为1.85 mL· min-1的实验条件下, 研究了35~80 mA范围内的放电电流对SBR的影响。 如图4所示, 随着放电电流的增大, 锶的SBR逐渐增大。 因此, 选择75 mA作为放电电流的实验值。
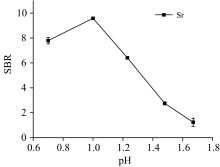
在放电过程中, 溶液的pH值会影响其电导率。 pH< 0.8时, 溶液阴极表面明显抖动, 放电激发过程非常不稳定, 等离子体稳定性下降。 当pH> 1.6时, 溶液的电导率减弱, 放电过程的能量不足以使待测元素被激发出来。 因此, 在溶液流速为1.85 mL· min-1和放电电流为75 mA的实验条件下, 测量0.8~1.6范围内的pH对SBR的影响。 如图5所示, 当pH 1时, 误差棒最小, SBR适中。 因此, 选择pH 1作为实验酸化条件。
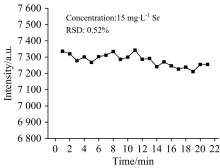
在固定锶的激发波长(460.77 nm) 下, 通过发射强度与时间的关系作图来检测放电的稳定性, 实验检测的稳定性用RSD表示, 如图6所示。 15 mg· L-1 Sr溶液的RSD值为0.52%。 结果表明, 所建立的SCGD-AES检测系统具有较好的检测稳定性。
在最佳实验条件下(放电电流为75 mA, 溶液流速为1.85 mL· min-1, 酸化条件pH 1.0), 测量锶的标准溶液浓度为0.1, 1, 5, 10和20 mg· L-1。 强度以锶的浓度为横坐标, 信号强度为纵坐标测量, 以特征波长(460.77 nm)的峰值量化目标元素。 采用检出限公式“ DLs=n* SD/k” , 其中n为置信系数[16]。 在我们的实验中取n=3, SD为空白溶液的标准差, k为标准拟合曲线的斜率。 由检出限公式得到锶的DLs为29 μg· L-1。 SCGD-AES的分析性能如表1所示, 光谱强度与锶的浓度呈良好的线性相关关系(r=0.999 6)。 结果表明, SCGD-AES方法具有较高的检测精度。
| 表1 SCGD-AES系统下锶的分析响应特性 Table 1 Analytical response characteristics of SCGD-AES system for Sr |
表2比较了所提出的SCGD-AES与采用小型化等离子体检测元素锶的ICP-AES的性能。 由表2可以看出, SCGD-AES和ICP-AES测量的结果基本一致。 因此, 选择锶 (460.77 nm)谱线作为水样SCDD-AES检测的实验结果是可靠的。 为了验证SCGD-AES检测结果的准确度, 对“ 岳龙泉” 、 “ 圣培露” 、 “ 巴马活泉” 等富锶矿泉水定量分析, 并进行了回收率实验。 由表3可以看出, 选用锶(460.77 nm)作为检测标准时, 回收率在98.8%~107.6%之间, 测定回收率与ICP-AES所测得的结果接近。 表明SCGD-AES具有较好的准确度性能。
| 表2 SCGD-AES和ICP-AES测定矿泉水中锶浓度的比较 Table 2 Comparison of Sr concentrations in mineral water determined by SCGD-AES and ICP-AES |
| 表3 矿泉水中锶的回收率 Table 3 Sr recoveries in mineral water |
采用自制的SCGD激发源结合便携式光纤光谱仪测定了矿泉水中的锶元素, 建立了测定水样中锶含量的新方法。 实验获得了SCGD-AES检测锶元素的最佳操作条件, 分别为1.85 mL· min-1溶液流速、 75 mA放电电流和pH 1.0 的HNO3作为电解质。 用SCGD-AES测定锶的检出限为29 μg· L-1。 15 mg· L-1 Sr的相对标准偏差为0.52% (n=21), 采用SCGD-AES定量检测矿泉水中的锶, 结果与ICP-AES结果吻合较好。 结果表明: 溶液阴极辉光放电原子发射光谱法是测定富锶矿泉水中锶的一种有效方法。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|