作者简介: 刘燕梅, 女, 1994年生, 华北理工大学药学院硕士研究生 e-mail: 1799735882@qq.com
表面增强拉曼光谱技术对分子具有特异性识别以及快速无损检测的能力, 使其在药物检测方面具有重大的潜力。 通过贵金属和氮化钛之间协同作用, 使复合基底具有较高的SERS性能, 提供了一种基于SERS技术的药物检测方法。 采用电化学沉积及自组装法, 制备出贵金属/氮化钛复合薄膜。 研究表明, 在复合薄膜中存在面心立方晶型TiN、 金属单质Au和Ag三种物相; 电子显微镜显示平均粒径分别为90和50 nm的金属Au和Ag颗粒均匀分布在TiN薄膜表面; 基底的紫外-可见吸收图谱中出现了贵金属金与银纳米颗粒及TiN薄膜三者的特征等离子体共振吸收峰。 以该复合薄膜为SERS基底, 对烟酸溶液进行拉曼检测。 结果显示, 贵金属/氮化钛复合薄膜对烟酸具有显著的SERS效应, 最低检测浓度为10-5 mol·L-1, 对1 033 cm-1处烟酸拉曼信号强度及浓度取对数, 发现两者间呈一定线性关系, 其 R2为0.969, 得益于TiN, Au和Ag之间可发生表面等离子体共振引起电磁场增强, 以及电荷转移效应。 研究还发现, 烟酸通过COO-基团垂直吸附在贵金属/氮化钛基底表面; 在酸性环境下, 烟酸N原子质子化主要以阳离子N+H(Ⅰ)形式存在; 在碱性环境时, 主要以阴离子COO-(Ⅲ)形式存在。 绞股蓝总甙溶液中模拟烟酸非法添加, 该复合基底对其最低的拉曼检测浓度是10-5 mol·L-1, 为现场快速检测非法添加药物提供了新途径。
The surface-enhanced Raman spectroscopy technology has specific recognition of molecules and rapid non-destructive detection capabilities, making it great potential in drug detection. In this study, drug detection research based on novel metal/titanium nitride composite substrate as SERS active substrate was carried out. Due to the synergy between the novel metal and titanium nitride, the composite substrate has high SERS performance, providing a drug detection method based on SERS technology. Electrochemical deposition and self-assembly methods were used to prepare novel metal/titanium nitride composite film. There are three kinds of phases: face-centered cubic crystal TiN, metal Au and Ag in the composite film. The electron microscopy showed that metal Au and Ag particles with a mean particle size of 90 and 50 nm were evenly distributed on TIN film's surface. For this reason, the characteristic plasmon resonance absorption peaks of the novel metal gold and silver nanoparticles and TiN thin film appeared in the ultraviolet-visible absorption spectra of the thin film. Using the composite film as the SERS substrate, Raman detection was performed on the nicotinic acid solution. The results show that the novel metal/titanium nitride composite film has a significant SERS effect. The logarithm of the Raman signal intensity and nicotinic acid concentration at 1 033 cm-1 indicated a certain linear relationship between the two, the linear correlation coefficient was 0.969, and the minimum detection concentration of nicotinic acid was 10-5 mol·L-1. This is due to the effect of charge transfer and the enhancement of the electromagnetic field caused by the surface plasmon resonance between the particles of TiN, Au and Ag. It was also found that nicotinic acid was vertically adsorbed on the novel metal/titanium nitride substrate's surface through the COO- group. When in an acidic environment, the protonation of nicotinic acid N atom mainly existed in cation N+H(Ⅰ). In an alkaline environment, it mainly existed in the form of anion COO-(Ⅲ). In addition, for the illegal addition of nicotinic acid in the gypenoside solution, the lowest Raman detection concentration of the composite substrate is 10-5 mol·L-1, which provides a new way for the rapid detection of illegally added drugs on site.
烟酸(Nicotinic acid)又称维生素B3, 是一种水溶性维生素, 与核糖、 磷酸、 腺嘌呤组成辅酶, 参与体内的氧化还原反应。 具有治疗皮肤性疾病、 高血脂症、 心血管病以及促进人体正常生长发育等作用。 据Lopez[1]报道烟酸缺乏症患者未经治疗可在4~5年内死于严重腹泻、 外周循环或全身衰竭, 死亡率高达15%~50%。 然而, 烟酸也被非法添加到保健食品中, 孙亮利用高效液相色谱法测定了保健食品中非法添加烟酸等药物[2]。 目前检测分析烟酸的主要方法有分光光度法、 气相色谱法、 高效液相色谱法、 近红外光谱法等[3]。 但这些方法前处理步骤复杂、 检测过程繁杂, 且分析时间较长。
表面增强拉曼光谱(surface-enhanced Raman spectroscopy, SERS)指由于物理和化学作用, 将分子吸附到纳米尺寸的金属(如金、 银、 铜等)或半导体等特殊结构的粗糙表面上, 分子的拉曼信号强度被异常放大的光谱现象。 表面拉曼增强机理包括由表面等离子体共振效应引起的电磁场增强机制, 以及吸附分子与基底之间电荷转移的化学增强机制。 SERS技术因其可表征分子结构信息, 检测灵敏度高, 不破坏样品等优点被用于生物医学检测和药物分析等领域。 例如, 韩礼刚[4]通过Gaussian 03软件理论上计算了烟酸分子的简正振动光谱, 对拉曼特征峰归属进行了指认, 为含烟酸的药物检测和痕量检测提供依据。 Barthelmes[5]利用银电极为SERS基底, 实现了对烟酸分子结构的拉曼分析, 但未模拟烟酸的非法添加检测。
最新研究发现, 氮化钛具有表面等离子体共振(surface plasmon resonance, SPR)效应, 且兼具熔点高、 热稳定和化学稳定性良好及生物相容性较好等优势, 具有作为SERS基底的应用潜力[6]。 Wei等[7]采用氨气还原氮化法制备了TiN薄膜, 发现其在500 nm附近出现表面等离子体共振吸收峰, TiN薄膜对罗丹明6G增强因子为1.06×104, 检出限达10-6 mol·L-1。 氮化钛与贵金属金、 银复合后因耦合增强作用而具有显著的SERS效应。 其中, Guler等[8]发现TiN具有与Au相似的光学性能, 将纳米针尖TiN薄膜和Au薄膜复合后具有较强的拉曼增强效果。 Ban等[9]研究TiN与Ag纳米球之间存在多种表面等离子体共振模式, 并利用该SERS基底强大的局部电磁场效应, 通过物理和化学机制协同作用提升了SERS活性, 实现了对分子高灵敏度和高稳定性的检测。
本工作将氮化钛薄膜与贵金属金、 银纳米颗粒复合, 利用电化学沉积方法在TiN薄膜表面沉积金纳米颗粒, 得到TiN-Au薄膜, 再通过银溶胶自组装制备出TiN-Au-Ag复合SERS活性基底, 深入地探究其对烟酸的拉曼增强效应。
四氯化钛(TiCl4)为钛源, 购自上海阿拉丁试剂网; N, N-二甲基甲酰胺(DMF)助溶剂, 购自上海阿拉丁试剂网; 聚乙烯吡咯烷酮(PVP, 分子量为130×104)成膜助剂, 唐山博亚树脂有限公司提供; 无水乙醇为分析纯, 购自天津市兴复精细化工研究所; 硝酸银(AgNO3)、 柠檬酸三钠(Na3C6H5O7·2H2O)、 氯金酸四水合物(HAuCl4·4H2O)和磷酸二氢钾(KH2PO4)为分析纯, 购自国药集团化学试剂有限公司; 氨气(99.99%)和氮气(99.99%)购自唐山市路北区万嘉气体经销处; 烟酸(C6H5NO2)为生化试剂, 购自上海宇涵生物科技有限公司; 绞股蓝总甙片购自某网。
1.2.1 SERS基底制备
TiN薄膜的制备: 取6 mL四氯化钛乙醇溶液, 加入无水乙醇10 mL, PVP 1 g, DMF 2.5 mL于烧杯中搅拌溶解, 得到TiO2前驱体溶液。 采用匀胶仪在1 cm×1 cm的石英基片上镀膜, 转速设置为3 500 r·min-1, 时间为20 s。 然后将膜于80 ℃下加热24 h, 置于600 ℃下预烧30 min, 得到TiO2膜。 将TiO2膜放入1 000 ℃管式炉中保温2 h, 升温速率为5 ℃·min-1, 通入800 mL·min-1的NH3, 得到TiN薄膜[7]。
Au和TiN-Au薄膜的制备: 在20 mL蒸馏水中加入0.007 1 g氯金酸, 0.195 6 g磷酸二氢钾, 搅拌溶解。 利用直流稳压电源提供电流, 将ITO玻璃和所制备的TiN薄膜为工作电极, Pt片为对电极, 沉积电压为10 V, 时间为5 min, 分别得到Au薄膜和TiN-Au薄膜。
银溶胶制备: 称取硝酸银0.018 g, 溶于100 mL去离子水中, 置于油浴锅中搅拌加热, 待溶液沸腾后, 逐滴加入0.03 mol·L-1 10 mL的柠檬酸钠, 反应1 h后, 制备得到黄绿色的银溶胶, 遮光保存。
1.2.2 检测溶液配制
烟酸溶液配制: 取烟酸0.0123 g于10 mL去离子水中, 超声5 min溶解, 得到10-2 mol·L-1的溶液。 采用10倍稀释的方法制备浓度范围从10-2~10-6 mol·L-1的烟酸溶液。
绞股蓝总甙溶液配制: 取一粒绞股蓝总甙片研磨, 加入甲醇10 mL, 超声20 min后, 在5 000 r·min-1条件下离心5 min取上清液。
绞股蓝总甙混合溶液配制: 取10 mL绞股蓝总甙上清液加入0.012 3 g烟酸, 得到烟酸浓度为10-2 mol·L-1的绞股蓝总甙混合溶液。 用绞股蓝总甙上清液依次稀释成梯度标准液: 10-2, 10-3, 10-4和10-5 mol·L-1。
1.2.3 SERS信号检测
将制备好的样品溶液与银溶胶按1:1体积比混合, 直接滴加于石英基底、 TiN及TiN-Au基底上, 晾干。 在激发波长为633 nm, 激发功率为5 mW, 采集时间为10 s, 物镜为10×, 进行SERS检测。
采用日本理学株式会社D/MAX 2500PC型X射线衍射仪分析所制样品的晶相组成; 采用日本日立公司S-4800型场发射扫描电子显微镜观测样品形貌并进行微区成分分析; 采用日本电子株式会社JEM-2800F型透射电子显微镜观测样品微观形貌; 采用美国PerkinElmer公司Lambda 750S型分光光度计测定样品的透射率(T)和反射率(R), 利用吸收率(A)=1-T-R, 得到其吸收率; 采用美国热电公司DXR型拉曼光谱仪检测样品拉曼信号, 激发波长为633 nm。
图1为TiN薄膜、 TiN-Ag、 TiN-Au和TiN-Au-Ag基底的XRD图谱。 图1(a)中分别出现了对应有NaCl型面心立方结构的TiN晶体(111)和(200)晶面的特征衍射峰。 当银溶胶自组装在TiN-Au基底上时, 样品XRD图谱中金属金和银的(111)及(200)晶面衍射峰发生了重合[10]。 为此, 对该衍射峰进行分峰拟合, 如图1(b), 可以看到在拟合图中分别出现了Ag晶体(200)以及Au晶体(200)的特征衍射峰, 表明复合基底中单质Au, Ag及TiN三种物相共存, 金纳米颗粒和银纳米颗粒同时存在于TiN薄膜上。 利用紫外-可见光谱对上述基底进行光学性能分析, 测试结果如图1(c)所示。 当金纳米颗粒沉积在纯TiN薄膜上时, TiN-Au基底吸收光谱中在490 nm附近出现了明显的等离子共振吸收峰。 另外, 银胶溶液吸收光谱中在420 nm处出现一共振吸收峰, 与文献[11]报道一致。 同时发现银溶胶颗粒自组装在TiN-Au薄膜后, TiN-Au-Ag基底在490 nm附近处出现TiN和Au的特征吸收峰, 另外在310 nm附近处也可观察到银纳米粒子的特征吸收峰, 表明这可能是由于金纳米颗粒与银纳米颗粒及TiN薄膜间产生了等离子共振效应, 据此推测该薄膜的SERS活性较高。
分别采用扫描电子显微镜与透射电子显微镜对上述样品的微观形貌进行分析, 结果如图2所示。 由图2(a)观察到TiN薄膜表面有直径约为50 nm不规则的球状TiN颗粒。 图2(b)表明, 当在TiN薄膜表面自组装银溶胶颗粒后, 氮化钛薄膜表面出现银纳米颗粒, 银颗粒分布不连续, 发生团聚现象。 当利用电化学沉积方法在TiN薄膜沉积金后, 如图2(c)所示, 薄膜表面上覆盖了致密且均匀的近似于球形的金纳米颗粒, 尺寸达到90 nm。 进一步在TiN-Au表面自组装银溶胶颗粒后, 发现复合薄膜表面呈现出更为均匀致密的纳米颗粒层, 厚度约为120 nm, 如图2(d)所示。 从图2(e)和图2(f)中发现, 所制备的银胶纳米颗粒呈近似球形, 粒径约为50 nm, 选区电子衍射表明单质银为多晶结构, 其高分辨电子图像中晶格条纹间距为1.22 nm, 与单质银晶体(311)晶面相对应。 从该样品的EDS(能谱)面扫描中可以看到复合薄膜表面分布着Ti, Au和Ag元素, 如图2(g—i)所示, 进一步印证了XRD的检测结果, 并证明了复合薄膜中存在氮化钛、 单质金和银纳米颗粒。
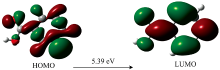
通过GaussView16.0软件计算了烟酸的轨道能级差为5.39 eV, 如图3所示。 文献[9]报道Au纳米粒子的禁带宽度为5.55 eV, Ag纳米粒子的禁带宽度为5.49 eV, TiN材料的禁带宽度为4.87 eV。 相比之下, 氮化钛、 金、 银与烟酸分子之间轨道能级差相近, 它们之间容易发生电荷转移, 因此, 预测该复合基底对烟酸具有SERS检测能力。
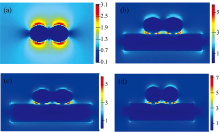
为了探究银胶、 TiN-Ag、 TiN-Au及TiN-Au-Ag基底薄膜的电场分布情况, 选择波长为400~700 nm的光沿y轴入射, 利用时域有限分差法对基底进行模拟, 结果如图4所示。 图4(a)与图4(b)相比较发现, 银溶胶颗粒与TiN薄膜进行组装后, 提高了局域电场强度。 这是由于在氮化钛薄膜与银纳米颗粒的结合处, 表面产生了强烈的等离子体耦合效应, 出现明显的“ 热点” 。 图4(b)和图4(c)显示基底的局域电场强度近乎相同。 从图4(d)可以看到, 在TiN-Au薄膜上组装银粒子后, 使得基底的局域电场强度明显增强, 这可能是因为Ag纳米颗粒会在聚集的Au纳米颗粒之间形成纳米带隙, 导致提供的“ 热点” 增多, “ 热点” 处的局域表面等离子体共振引起电场增强, 对于辐照电场E0和由此产生的局部电场E, 拉曼信号增强因子可以近似为(|E|/|E0|)的104 [12], 这将赋予该复合基底良好的SERS性能。
2.3.1 不同基底对SERS强度影响
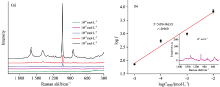
将浓度为10-2 mol·L-1的烟酸吸附在不同SERS基底上, 其拉曼检测结果如图5所示。 可以看到, 样品的拉曼图谱在847, 1 033, 1 154, 1 195, 1 390和1 590 cm-1处出现特征拉曼峰, 这些峰是烟酸的特征峰。 其中847 cm-1的特征峰是平面内环变形振动峰, 1 033和1 590 cm-1位移对应于烟酸结构中的吡啶环呼吸振动, 位移1 154 cm-1则归属于环呼吸和C—H的剪切振动, 1 195 cm-1处拉曼峰归属于环振动和C—H的伸缩振动, 1 390 cm-1对应—COOH基团对称拉伸模式[5, 13]。 以1 033 cm-1处拉曼峰作柱状图, 如图5(b)所示。 发现以银溶胶和TiN-Au复合薄膜作为基底时, 烟酸分子的信号强度较弱, 而在TiN表面自组装银溶胶粒子后, 样品的拉曼信号也得到了增强。 当TiN-Au基底上组装银溶胶粒子后, 对烟酸的拉曼检测信号强度达最大值, 为6 832 cps。 这表明了TiN-Au-Ag复合基底对烟酸有明显的SERS增强作用。 这是因为在TiN, Au与Ag具有等离子体共振协同效应, 而且三者之间形成了更多的SERS“ 热点” , 引起基底的局域电磁场强度增强, 同时它们与烟酸之间容易发生电荷转移, 从而证实了上述推测。
 | 图5 (a)烟酸在不同基底上的SERS图; (b)烟酸在不同基底上的柱状图Fig.5 (a) SERS spectra of nicotinic acid on different substrate; (b) Histogram of nicotinic acid on different substrate |
2.3.2 pH值对SERS强度影响
利用HCl和NaOH将10-2 mol·L-1烟酸的pH值分别调节为1, 3, 5, 7, 9, 11及13。 取不同pH值的烟酸与银溶胶按照体积比为1:1混合, 滴加至TiN-Au基底上, 测试不同pH值体系下烟酸的拉曼信号, 如图6所示。 从图中可以看到在酸性条件下, 当pH值逐渐增加, 在1 642 cm-1位移处的环振动拉曼峰消失, 这是由于吡啶衍生物中N质子化产生的影响; 随pH值进一步增大, 当达到碱性环境时, 观察到位于1 390 cm-1位移处COO—基团的拉曼信号峰强度逐渐增强, 因此, 通过增加pH可以发现烟酸溶液中由阳离子(Ⅰ)形式到两性离子(Ⅱ )及阴离子(Ⅲ)形式的结构变化。 在碱性环境中, 烟酸的拉曼信号会增强。 这是由于烟酸分子吸附在金属表面时有三种排列方式, 一是是分子平面取向排列, 二是氮原子垂直排列在金属表面, 三是羧基在金属表面垂直排列。 根据SERS选择规则, 只有垂直于SERS基底表面的分量振动模式才能被很大程度的增强, 而平行于基底表面的振动模式增强效果非常小或接近零, 故平行排列的烟酸分子拉曼信号强度弱。 另外, 当溶液在酸性环境下时, N原子质子化主要以阳离子N+H(Ⅰ)形式存在; 而在碱性环境时, 溶液主要以阴离子COO-(Ⅲ)形式存在, 由于金属表面与氢原子之间的排斥作用[14], 导致烟酸在碱性环境中的拉曼信号强度会进一步提高。 此时, 烟酸通过COO-基团垂直吸附在TiN-Au-Ag表面。
2.3.3 烟酸标准溶液的SERS定量分析
为测试TiN-Au-Ag基底对烟酸的最低检测浓度, 分别取1 mL浓度为10-2, 10-3, 10-4, 10-5和10-6 mol·L-1的烟酸与1 mL银溶胶混合, 然后滴加在TiN-Au基底上进行拉曼光谱测试, 结果如图7所示。 随着溶液浓度的降低, SERS基底上的烟酸分子信号强度也逐渐降低, 当浓度为10-6 mol·L-1, 已检测不到烟酸特征拉曼峰[见图7(a)]。 在烟酸浓度为10-2~10-5 mol·L-1范围内时, 对1 033 cm-1处拉曼信号强度及烟酸浓度求对数, 分别作为纵坐标和横坐标, 如图7(b)所示, 可以看到两者间呈一定线性关系, 其线性方程为Y=5.08+0.63X, 其R2=0.969。 当烟酸溶液浓度为10-5 mol·L-1时, 发现位于1 033 cm-1位移处的特征拉曼信号强度为72 cps, 说明在TiN-Au基底上添加银胶后, 烟酸的最低检测浓度可达到10-5 mol·L-1。
2.3.4 绞股蓝总甙溶液中烟酸的定性定量分析
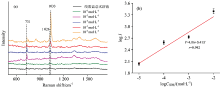
利用表面增强拉曼光谱技术在中成药绞股蓝总甙片中模拟非法添加烟酸, 将1 mL绞股蓝总甙溶液与1 mL银胶溶液混和均匀后, 滴加至TiN-Au复合基底上, 进行SERS检测。 如图8(a)所示, 在731及1 026 cm-1处出现了归属于绞股蓝总甙溶液的特征峰。 将不同浓度的烟酸掺杂到绞股蓝总甙溶液中, 烟酸的掺杂量为10-2~10-6 mol·L-1, 烟酸在1 033 cm-1处的特征峰可以被清楚指认。 表明利用表面增强拉曼光谱技术可以对药物的掺杂进行快速检测。 另外, 从图8(a)中发现, 随着烟酸浓度的降低, 其拉曼信号强度逐渐降低, 当浓度为10-6 mol·L-1时, 1 033 cm-1的特征拉曼信号峰检测不到, 而在1 026 cm-1位移处出现了属于绞股蓝总甙溶液的峰, 表明对烟酸的最低检测浓度为10-5 mol·L-1。 在10-2~10-5 mol·L-1浓度范围内, 对1 033 cm-1处的特征峰强度求对数, 作为纵坐标; 对掺杂的烟酸浓度求对数, 作为横坐标, 建立两者的定量关系发现烟酸浓度的对数与其拉曼信号强度的对数间呈一定的线性关系, 标准曲线方程为Y=4.06+0.41X, 相关系数r为0.942, 如图8(b)所示。
采用电化学沉积法和自组装相结合的方法, 制备了贵金属/氮化钛复合基底。 使用XRD、 SEM及TEM对复合基底表征发现, TiN, Au和Ag三种物相共存, 且Au和Ag颗粒均匀分布在TiN薄膜表面。 利用贵金属/氮化钛复合薄膜为SERS基底, 对烟酸溶液进行拉曼检测。 由于TiN, Au和Ag三者粒子间的表面等离子体共振引起电磁场增强, 以及电荷转移效应, 使得TiN-Au薄膜上组装银胶后, 在1 033 cm-1处对烟酸的拉曼检测信号强度值达到6 832 cps, 明显高于TiN-Ag, TiN-Au和银胶基底, 烟酸的最低检测浓度为10-5 mol·L-1。 另外发现烟酸在不同pH值环境下有不同的存在形式, 且于碱性环境下提高了烟酸的拉曼信号强度。 绞股蓝总甙溶液模拟烟酸非法添加, 最低检测浓度是10-5 mol·L-1, 模拟实现了对非法添加物的检出。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|