作者简介: 杨传孝, 1970年生, 华侨大学材料科学与工程学院副教授 e-mail: cxyang@hqu.edu.cn
在微波辅助条件下, 合成了甲醛功能化的聚乙烯亚胺(FPEI), 在激发波长为340 nm时, FPEI的荧光发射波长470 nm, 紫外灯下发蓝色荧光。 在此激发条件下, 曙红Y(Y eosin Y, EY)的荧光发射波长为540 nm, 发绿色荧光。 在酸性介质中, FPEI和 EY 通过静电作用形成FPEI/EY复合物, 导致EY 在540 nm 的荧光显著猝灭, 而FPEI本身的荧光只有微弱的降低。 当加入六偏磷酸钠(SHMP)时, SHMP、 EY与FPEI发生竞争结合, 由于SHMP与FPEI表面质子化氨基的静电作用强于EY, EY从FPEI/EY复合物中释放导致540 nm荧光强度逐渐恢复。 当SHMP与FPEI/EY 混合时, EY 540 nm荧光强度与FPEI 470 nm 荧光强度的比值( F540/ F470)与SHMP浓度呈较好的线性关系, 在紫外灯照射下体系的荧光由蓝色逐渐变为绿色, 由此建立了FPEI/EY比率荧光快速测定SHMP的新方法。 在最优条件下, 线性范围为0.1~4.2 μmol·L-1, 检出限(3 σ)为38 nmol·L-1。 该方法选择性好、 简单、 快速, 已成功应用于茶饮料中SHMP的分析检测。
Under the condition of microwave assisted, formaldehyde functionalized polyethyleneimine (FPEI) was synthesized. The maximum emission of FPEI at 470 nm was obtained when the excitation wavelength was set at 340 nm, and the blue fluorescence was easily observed under an ultraviolet lamp. Under this excitation condition, the fluorescence emission peak of the Eosin Y (EY) was located at 540 nm, and the green fluorescence was observed. In acidic medium, the EY and FPEI form a complex through electrostatic interaction. The formation of the FPEI/EY complex resulted in the quenching of EY fluorescence at 540 nm, while the fluorescence intensity of FPEI was only slightly reduced. In the presence of sodium hexametaphosphate (SHMP), competitive binding occurred between SHMP, EY and FPEI. Because the electrostatic interaction between SHMP and protonated amino groups on FPEI surface is stronger than that of EY, EY was gradually released from the PEI/EY complex, resulting in the recovery of EY fluorescence at 540 nm. The fluorescence change ratio between the fluorescence intensity of Ey at 540 nm and the fluorescence intensity of FPEI at 470 ( F540 /F470) has a good linear correlated with the concentration of SHMP, and a noticeable blue to green changed under an ultraviolet lamp if SHMP solution was mixed with the FPEI/EY. Based on the phenomena, a novel rapid ratiometric fluorescence method for determination of SHMP was developed. Under the optimized conditions, the linear range is 0.1~4.2 μmol·L-1, and the limit of detection (3 σ) was 38 nmol·L-1. The proposed method is of high selectivity, simple and rapid, and is successfully applied to determine the concentration of SHMP in tea drink samples.
多聚磷酸根、 偏磷酸根、 正磷酸根及核苷酸等均含磷酸根阴离子, 其中核苷酸是生命体组成的重要成分并参与生命过程, 多聚磷酸根、 偏磷酸根、 正磷酸根等是重要的化工原料, 六偏磷酸钠是常用的食品添加剂。 因此, 含磷酸根阴离子的检测具有十分重要的现实意义[1, 2]。 食品级六偏磷酸钠(sodium hexametaphosphate, SHMP)是一种多聚磷酸盐, 是一种具有环状和链状结构的混合物, 对二价金属离子 (如Ca2+) 具有较好的结合能力, 其链状结构能保持其pH在一个稳定的范围。 在食品、 乳品、 饮料及牙膏产品中加入SHMP, 可以提高产品的持水性、 结着性、 防止脂肪氧化, 提高果汁饮料的出汁率和黏度, 抑制维生素C的分解、 稳定食品中的天然色素及色泽、 保护牙齿免遭酸性饮料的侵蚀等[3, 4]; 在纳米材料的制备过程中加入多聚磷酸盐可以提高纳米粒子的稳定性及发光性能[5, 6]。 然而即使是食品级的SHMP, 其中也含有微量的重金属及氟化物, 过量添加会破坏营养元素, 严重危害人体的健康, 我国对各类食品中六偏磷酸钠的允许用量做了明确的规定[7](茶饮料中SHMP的最大使用量为0.5 g· kg-1), 因此建立一种快速检测食品、 饮料中SHMP含量的方法具有重要意义。 目前, 测定食品中磷酸盐添加剂的方法有重量法、 原子吸收光度法、 离子色谱法及分光光度法等。 其中重量法、 原子吸收光度法、 离子色谱法存在使用试剂种类多、 操作繁琐费时等缺点。 而荧光[8, 9]检测六偏磷酸钠具有较高灵敏度和选择性。
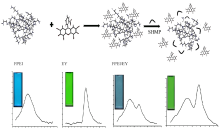
聚乙烯亚胺(polyethyleneimine, PEI)是一种水溶性阳离子聚合物, 具有线状和支链状两种结构形式。 其结构中富含大量胺基, 可通过氢键、 配位、 静电作用等与其他物质结合。 Wen[10]等研究表明PEI能与曙红(eosin Y, EY)通过静电作用结合, 导致EY的荧光显著猝灭, 当十二烷基硫酸钠存在时EY的荧光又得到恢复。 在微波辅助条件下甲醛与PEI快速作用, 生成物在紫外光照射下发蓝色荧光。 本研究表明该甲醛功能化的聚乙烯亚胺(formaldehyde functionalized polyethyleneimine, FPEI)保留了PEI的一些性质, 其表面残留的胺基仍能与EY通过静电作用结合形成基态复合物, 导致EY的荧光显著猝灭。 在酸性介质中, SHMP可以阻碍EY与 FPEI的结合, 从而抑制EY荧光强度的降低, 而FPEI本身的荧光强度变化不大, 可以作为内标物质。 由此构筑比率荧光体系(图1), 构建EY/FPEI比率荧光探针, 并成功用于饮料中 SHMP 的检测。 该方法选择性好、 操作简单、 快速, 测定结果令人满意。
Cary Edipse型荧光分光光度计, 安捷伦科技(中国)有限公司; Nicolet Magna IR560型傅里叶变换红外光谱仪(美国Nicolet公司), H-7650型透射电镜(日本Hitachi公司), UV-2800H紫外可见分光光度计(日本Shimadzu公司), Milli-Q超纯水(美国Millipore公司), WX-4000微波消解仪(上海屹尧仪器科技发展有限公司), WFH手提式紫外分析仪(杭州齐威仪器有限公司)。
聚乙烯亚胺(Polyethyleneimine, PEI, 分子量为10 000), 阿拉丁试剂有限公司; 甲醛溶液(37.0%~40.0%, 西陇化工股份有限公司); 曙红(Eosin Y, EY), 西陇化工股份有限公司, 溶液浓度为1.0× 10-4 mol· L-1; 六偏磷酸钠(sodium hexametaphoshate, SHMP), 广东光华化学厂有限公司, 溶液浓度为1.0× 10-5 mol· L-1。 试剂均为AR级, 实验使用超纯水, 电阻为18.2 MΩ 。
准确移取聚乙烯亚胺溶液 (8.539× 10-3 g· mL-1)10 mL, 甲醛溶液1.0 mL, 乙酸溶液0.4 mL加去离子水至15 mL。 在温度120 ℃, 压力10 atm, 功率600 W的条件下, 微波消解30 s获得FPEI备用。
将FPEI原液稀释200倍制备操作溶液。 在10 mL比色试管中依次加入0.5 mL醋酸-醋酸钠缓冲溶液(pH 3.93), 1.0 mL FPEI操作溶液, 适量的SHMP标准溶液和样品溶液, 0.2 mL浓度为 1.0× 10-4 mol· L-1的EY, 用超纯水定容至5.0 mL。 于Cary Edipse荧光分光光度计上, 340 nm光激发, 扫描360~650 nm 波长范围的荧光发射光谱, 并记录位于470和540 nm处的荧光强度。 直接把样品置于365 nm紫外灯下, 用数码相机拍摄荧光成像。
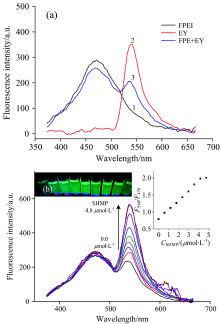
如图2所示, 在微波辅助条件下, 甲醛功能化的PEI在350 nm处出现新的紫外吸收峰, 其电镜图表明FPEI具有明显的网状结构(图2, 插图)。 激发波长在320~420 nm范围内, 随着激发波长的增加FPEI荧光发射峰的峰位逐渐红移, 在激发波长为340 nm时, FPEI的荧光激发峰位于470 nm处, 紫外灯下发蓝色荧光, 在FPEI相同激发条件下, EY的荧光发射峰位于540 nm处[图3(a, 线2)]。 与FPEI和EY的荧光发射光谱相比, FPEI/EY比率荧光发射光谱[图3(a, 线3)]中540 nm处EY的荧光发射强度显著降低, 而470 nm处FPEI的荧光强度却变化不大, 此时荧光颜色以FPEI为主。
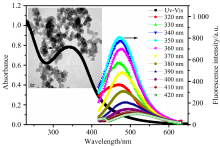 | 图2 FPEI的紫外-可见吸收光谱和在不同激光波长下的荧光发射光谱Fig.2 UV-Vis absorption and Fluorescence emission spectra of FPEI under different excitation wavelengths |
如图3(b)所示, 随着SHMP的量增加, FPEI/EY比率荧光体系在540 nm处荧光强度逐渐增加, 而470 nm处的荧光强度却基本不变, 540和470 nm处荧光强度的比值(F540/F470)与SHMP的浓度呈较好的线性关系[图3(b, 内插图)]。 在紫外灯照射下, 可以明显看出, 随着SHMP的量增加体系荧光由蓝色逐渐变为绿色。
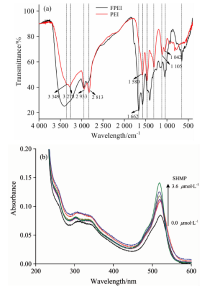
曙红 Y(H2L)在水溶液中的离解常数为pKa1=2.6和pKa2=3.6, 可以预测当pH> 3.6时EY主要存在形式是L2-。 而FPEI的红外吸收光谱[图4(a)]保留了N— H的伸缩振动(波数为3 349和3 278 cm-1)、 N— H的面内弯曲振动(波数为1 580 cm-1 )、 — CH2— 的伸缩振动(波数为2 933和2 813 cm-1)、 C— N的伸缩振动(波数为1 042和1 105 cm-1)等PEI的红外特征峰, 同时在1 662 cm-1产生了新峰, 表明甲醛的羰基基团与— NH2之间发生了Schiff碱反应, 进而形成具有网状结构的化合物。 在酸性条件下, FPEI表面残留的— NH2基和— NH基质子化, 通过静电引力与EY的生色团和荧光团上带负电荷的羟基氧原子作用, 形成了FPEI/EY基态复合物导致EY荧光猝灭, 遵从静态猝灭机理。 加入SHMP前后EY吸收光谱的变化可以证明FPEI/EY基态复合物的形成, 如图4(b)所示。 另一方面, 甲醛与PEI交联生成的FPEI具有网状结构且具有荧光特性, 这种网状结构结构可以有效减少EY 的稠环芳烃和 FPEI分子内烷基链的疏水作用, 使得EY只存在于FPEI分子的表面, 因此FPEI/EY基态复合物的形成对FPEI的荧光发射影响较小。 当有SHMP存在时, 由于SHMP与FPEI表面质子化氨基的静电作用强于EY, 因而SHMP可以阻止FPEI/EY基态复合物的形成, 致使EY吸光度[图4(b)]及荧光[图3(b)]逐渐恢复。
2.3.1 激发波长的选择
如图5所示, FPEI和EY的荧光发射强度与激发光波长有关, FPEI的最大激发峰位于350 nm处。 在激发波长位于320~340 nm时, 540 nm处EY的荧光强度基本不变。 当激发波长大于340 nm时, 540 nm处EY的荧光强度迅速降低。 考虑到FPEI/EY比率荧光体系荧光比色的需要, 本研究选择激发光波长为340 nm。
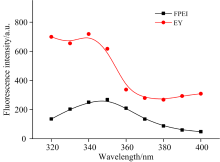 | 图5 激发光波长对荧光强度的影响 FPEI: 1.0 mL; EY: 4 μ mol· L-1; pH 3.93Fig.5 Effect of excitation wavelength on the fluorescence intensity FPEI: 1.0 mL; EY: 4 μ mol· L-1; pH 3.93 |
2.3.2 溶液pH的影响
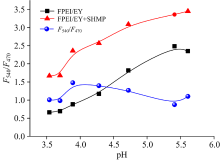
pH值对FPEI/EY复合物470 nm处的荧光强度基本没有影响, 但对于540 nm处的荧光强度影响较大, 随着pH值的不断增加, 荧光强度显著增强, 当pH值大于5.5后趋于稳定。 如图6所示, 加入SHMP前后, pH对于FPEI/EY复合物540和470 nm处的荧光强度的比值(F540/F470)的影响基本一致, 均随pH的增加逐渐增加。 但是, 加入SHMP前后F540/F470增加的程度(Δ F540/F470)却随pH的增加呈现先增加后降低的趋势, pH在3.9左右时体系F540/470增强的程度达到最大, 因此本研究用醋酸-醋酸钠缓冲溶液控制体系的pH为3.90左右。
2.3.3 甲醛加入量的影响
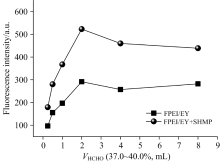
FPEI表面残留的氨基对FPEI/EY基态复合物的形成有较大的影响, 如图7所示。 随着甲醛(37.0%~40.0%)加入量的增加, FPEI/EY复合物位于540 nm处的荧光强度有逐渐增强的趋势, 当甲醛加量大于2.0 mL时荧光强度又缓慢降低。 研究表明540 nm处的荧光增强与SHMP间的线性范围及灵敏度均随着甲醛加入量的增加而增加, 当甲醛(37.0%~40.0%)加入量大于1.0 mL时其线性范围及灵敏度又逐渐减少。 这充分说明了甲醛越多FPEI的网状结构越多、 其表面的活性基团减少, FPEI与EY间的疏水作用和静电作用减弱, 有利于FPEI/EY复合物与SHMP作用。 但是甲醛加入量太多FPEI表面的质子化氨基太少, 又会导致FPEI表面结合的EY的量减少, 因而线性范围及灵敏度逐渐减少。 本研究用1.0 mL甲醛(37.0%~40.0%)合成FPEI。
2.3.4 EY加入量的影响
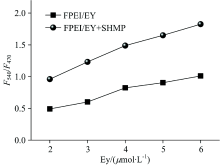
考察了一定量的FPEI与不同浓度的EY形成的FPEI/EY复合物与SHMP作用, 如图8和表1所示。 加SHMP前后FPEI/EY复合物F540/F470值随着EY浓度的变化趋势一致, 即F540/F470值随着EY浓度的增大而增加(图8)。 表1的实验结果表明随着EY浓度的增大FPEI/EY复合物的比率荧光与SHMP作用的线性范围有逐渐增大的趋势。 当EY浓度小于4.0 μ mol· L-1时, 随着EY浓度的增大FPEI/EY比率荧光测定SHMP的灵敏度(线性拟合曲线的斜率)增加较快, 而当EY浓度大于4.0 μ mol· L-1时FPEI/EY比率荧光测定SHMP的灵敏度增加变缓。 因此, 本研究选择浓度为4.0 μ mol· L-1的EY与FPEI作用形成FPEI/EY复合物。
| 表1 EY加入量对分析测定参数的影响 Table 1 Effect of EY on analytical parameters for determination |
本研究主要测定的是茶类饮料中的六偏磷酸钠的含量, 因此对于水中常见的金属离子、 阴离子和糖类进行了选择实验。 结果表明, 相对于SHMP浓度50倍的Fe3+, Mg2+, Li2+, Ni2+, Pb2+, Hg2+和Ba2+, 20倍的Ca2+和Zn2+, 5倍的Cu2+等金属离子对SHMP的测定没有影响; 100倍的柠檬酸根、 HP
在上述最优条件下, 考察了FPEI/EY复合物与不同浓度SHMP作用的线性关系, 如图9和表2所示。 与540 nm处的荧光增强与SHMP浓度的线性关系相比较, 可以看出比率荧光法(F540/F470)获得的线性相关系数(R2)、 线性范围和检出限均有明显提高, 这是因为比率荧光法可以有效避免光源不稳定等因素对荧光强度的影响, 可有效提高测定的准确度。 将三种饮料(茉莉清茶、 冰红茶、 冰绿茶)稀释10倍后用本方法进行测定, 结果如表3所示。 对样品进行了加标回收实验, 回收率在95.0%~108.3%之间, 说明运用比率荧光法测定饮料中六偏磷酸钠的结果满意。
 | 图9 540 nm荧光强度及F540/F470与不同浓度SHMP间的关系 FPEI: 1.0 mL; pH 3.93, λ ex=340 nmFig.9 Plots of fluorescence intensity at 540 nm and F540/F470via the concentrations of SHMP FPEI: 1.0 mL; pH 3.93, λ ex=340 nm |
| 表2 分析测定参数 Table 2 Analytical parameters for determination |
| 表3 饮料中SHMP的测定结果 Table 3 Results for the determination of SHMP in drink samples |
在微波辅助条件下, 成功合成了发蓝色荧光的 FPEI, 基于FPEI表面氨基与EY的生色基团和荧光基团作用形成FPEI/EY基态复合物, 发展了一种FPEI/EY双荧光体系比率荧光法测定SHMP的新方法, 该法具有灵敏度高、 反应快、 操作简便等优点, 可用于实际饮料中 SHMP的分析检测。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|