作者简介: 燕 芳, 1980年生, 内蒙古科技大学信息工程学院副教授 e-mail: 0472yanfang@163.com
传统鉴别法和现代鉴别法是目前我国中草药检测领域的主要方法。 传统鉴别方法虽因简便、 成本低廉等优势在研究中被广泛采用, 但鉴别准确度在一定程度上依赖于操作者是否具备丰富的药材知识和经验。 随着光谱分析技术的发展, 基于光谱分析技术的现代鉴别法逐渐走入人们的视野。 理论及大量实验研究表明, 中草药代谢物分子内振动模式及晶格的低频振动均发生在太赫兹波段, 据此可以鉴别中草药中所含成分。 甘草酸是甘草中的主要成分, 选择甘草酸为研究对象, 运用量子化学计算方法模拟甘草酸的太赫兹吸收谱, 为甘草酸的太赫兹吸收特征匹配分子振动模式, 此项工作对于深刻理解甘草酸分子内部各基团的相互作用与谱的形成机理十分必要。 为了确保模拟结果的可靠性, 需要建立甘草酸分子的初始构型, 选择合适的计算方法进行结构优化和频率计算, 最终获取甘草酸的太赫兹吸收谱数据。 利用Gaussian09半经验理论的PM3算法计算得到甘草酸太赫兹特征吸收峰分别位于0.87, 1.17, 1.56与2.76 THz处, 其中1.56 THz处的特征峰与参考文献中实验所测结果完全一致, 验证了计算结果的可靠性。 由于每个甘草酸分子中含有120个原子, 体系庞大, 在做振转模式分析时无法呈现其完整的结构, 故采用甘草酸分子的平面结构代替立体结构进行太赫兹特征吸收峰的振转分析。 分析表明, 甘草酸分子的太赫兹特征吸收峰产生与含氧官能团以及碳环的振转有关, 但主要是由甘草酸分子中的含氧官能团扭转形成的。
Traditional identification method and modern identification method are the main methods in the field of Chinese herbal medicine detection. Although the traditional identification method is widely used in research because of its advantages such as simplicity and low cost, the accuracy of identification depends to some extent on whether the operator has rich knowledge and experience in medicinal materials. With the development of spectral analysis technology, modern identification methods based on spectral analysis technology have gradually entered people’s field of vision. Theoretical and a large number of experimental studies have shown that the intramolecular vibration mode of the Chinese herbal metabolites and the low-frequency vibration of the lattice occur in the terahertz band, which can be used to identify the components contained in the Chinese herbal medicine. Glycyrrhizic acid is the main component in licorice. Glycyrrhizic acid was selected as the research object. The terahertz absorption spectrum of glycyrrhizic acid was simulated by a quantum chemical calculation method. The terahertz absorption characteristic of glycyrrhizic acid matched the molecular vibration mode. This work is deeply understood. The interaction of various groups within the glycyrrhizic acid molecule and the formation mechanism of the spectrum are necessary. In order to ensure the reliability of the simulation results, it is necessary to establish the initial configuration of the glycyrrhizic acid molecule, select the appropriate calculation method for structural optimization and frequency calculation, and finally obtain the terahertz absorption spectrum data of glycyrrhizic acid. Through the Gaussian09 semi-empirical theory PM3 algorithm, the characteristic absorption peaks of the glycyrrhizic acid terahertz are located at 0.87, 1.17, 1.56 and 2.76 THz, respectively. The characteristic peak at 1.56 THz is exactly the same as the experimental results in the reference literature, verifying the reliability of the calculation results. Since each glycyrrhizic acid molecule contains 120 atoms, the system is so large that it cannot exhibit its complete structure when it is analyzed by vibration mode. Therefore, the planar structure of glycyrrhizic acid molecules is used instead of the three-dimensional structure to carry out the vibration of the terahertz characteristic absorption peak. Turn analysis. The analysis shows that the terahertz characteristic absorption peak of glycyrrhizic acid molecule is related to the oxygen-containing functional group and the ring-like vibration of the carbon ring, but is mainly formed by twisting of the oxygen-containing functional group in the glycyrrhizic acid molecule.
太赫兹时域光谱技术(THz-TDS)已成为研究人员分析分子结构的重要手段。 研究发现, 许多生物大分子的振动都发生在0.1~10 THz内的太赫兹波段[1]。 王卫宁等应用THz-TDS技术, 测试了20种α -氨基酸的太赫兹光谱, 发现在0.2~3 THz频谱范围内上述氨基酸均存在各自的吸收峰[2]。 利用 THz-TDS技术获取样品太赫兹吸收光谱时, 去除基线可以消除样品散射对吸收光谱产生的影响。 大量的实验研究与理论计算均证明THz-TDS技术能够运用于有机分子分析。
有机分子构成了中草药中的主要成分, 故可以借鉴研究氨基酸分子所用到的太赫兹时域光谱技术对中草药进行鉴别与分析。 张活运用B3LYP泛函计算得到青蒿素的太赫兹吸收光谱, 与实验谱对比, 清晰的揭示了青蒿素特征峰的产生机理[3]。 刘俊秀等使用太赫兹光谱仪获取15种有机化合物的光谱数据, 利用差分-主成分分析-支持向量机有机物识别方法, 达到了很高的正确识别率[4]。 邹粮徽等利用太赫兹时域光谱技术检测水体重金属污染, 并指出药材中某一成分在太赫兹频率范围内的振动模式尚待研究[5]。 Liu等将THz光谱与ALAP-SVM相结合, 有效的鉴别不同转基因棉花种类[6]。
本文选取甘草中的主要成分甘草酸作为研究对象, 借助于Gaussian09软件对甘草酸分子进行量子化学计算分析。 Gaussian09软件在量子化学计算分析中被研究者广泛使用, 与之配套的GaussView5.0软件能够以动态的方式将分子的振动模式呈现出来。 不仅如此, Gaussian09软件还提供了密度泛函(DFT)、 半经验算法(Semi-Empirical)及从头算法(Ab Initio Method)等一系列计算方法, 这些计算方法的准确性已经在组氨酸、 L-, D-与DL-阿拉伯糖以及β -胡萝卜素等有机分子的计算中得到了证实[7, 8, 9]。
目前, 运用量子化学计算中草药单一成分的研究工作相对较少。 因此在后续研究中对分子构型的建立, 计算方法的选择要求更高。 另外甘草酸分子体系较大, 在保证计算结果准确的情况下, 还需考虑计算机时的长短。
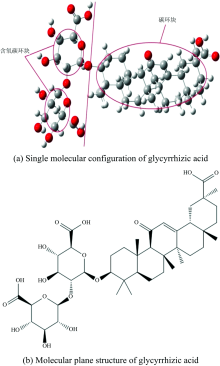
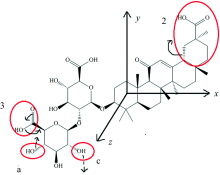
甘草酸分子式为C42H62O16, 含有120个原子, 归属于有机大分子。 故本文首先根据其分子结构特征, 对它进行结构分类, 以便于下一步计算结果的分析。 图1所示的甘草酸单分子构型是在ChemDraw中绘制完成的。
在图1(a)中, 根据甘草酸的结构特征, 以红色直线作为分界线, 把甘草酸分子“拆成”两部分。 由于甘草酸分子左半边碳环的构成含有氧原子(如图中红色圆圈), 故左半边可称为含氧碳环块。 甘草酸分子右半边碳环皆由碳原子构成, 而少有的氧原子均在碳环侧链, 可将右半边称为碳环块。
将ChemDraw中绘制的甘草酸分子坐标导入到Gaussian09软件中进行计算, 首先为甘草酸分子选择计算方法。 经过DFT和HF方法计算甘草酸这一有机大分子, 发现普通计算机的内存无法满足计算要求。 而半经验理论主要用于计算有机大分子体系, 且计算机时较短[10]。 因此, 本文采用半经验理论(Semi-Empirical)中的PM3算法进行结构优化。 在结构优化成功的基础上, 仍用PM3算法进行频率计算, 得到甘草酸分子的太赫兹吸收谱。 这里需要注意结构优化与频率计算要用相同的算法, 否则计算结果失去意义。 表1为实验计算机配置简介。
| 表1 计算机配置 Table 1 Computer configuration |
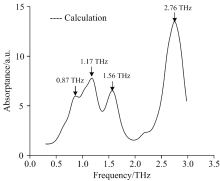
图2为利用量子化学方法计算得到的太赫兹吸收谱, 其频谱范围为0.3~3 THz。 由图2可见, 甘草酸分子在0.3~3 THz范围内有四个吸收峰, 分别位于0.87, 1.17, 1.56与2.76 THz处。 其中1.56 THz处的吸收峰与赵春喜[11]实验所测得的1.56 THz吸收峰位完全一致, 且与其运用密度泛函理论(DFT)方法计算得到的1.55 THz处吸收峰基本符合。 证明了本文中的甘草酸分子初始构型与PM3算法的选择是合理的, 也说明量子化学计算可以为实验获得的太赫兹光谱提供理论佐证。 其余三个吸收峰位与相关文献之间还存在一定的差异, 这与计算时选取了不同的计算方法和不同的分子构型有一定的关系。
支持向量机(SVM)、 量子化学计算与太赫兹时域光谱技术相结合的定性分析, 是建立在太赫兹吸收谱基础之上、 从不同角度进行分析的方法。 本文参考上述方法的思路, 从振转模式的视角出发, 在GaussView5.0的视频模块中, 观察分析特征吸收峰的振转动态模式, 进一步揭示特征吸收峰的产生机理。
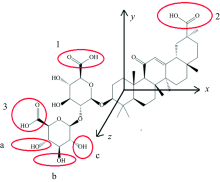
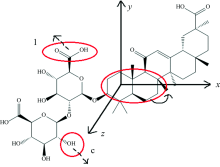
由于甘草酸分子的平面结构在Chemdraw中绘制, 且Gaussian09计算所用输入坐标是从Chemdraw中导入, 计算成功后产生的输出文件在GaussView5.0打开, 观察特征峰的振转模式, 所以甘草酸分子平面结构与立体结构坐标具有一致性。 因而可采用甘草酸分子平面结构图代替立体结构图分析振转模式。 根据甘草酸分子基团的结构特征, 对其分类标号, 分析四个吸收峰位的振转模式。 如图3所示, 三个羧基(—COOH)分别标号为1, 2和3; 三个羟基(—OH)依次标号为a, b和c。 图4—图7分别为甘草酸分子在四个吸收峰位的振转模式分析图。 甘草酸分子在0.87 THz处吸收峰, 主要是两个羧基(—COOH)分别近似以y轴为转轴(标号为1的羧基)、 x为转轴(标号为2的羧基)扭转, 共同作用形成的, 且2号羧基振动幅度大于1号。 在1.17 THz处的吸收峰是由于3号羧基近似以y轴方向扭转、 2号羧基振转模式与0.87 THz处相同, 其中3号羧基振动幅度明显大于2号而形成的; 除此之外, 碳环块也存在小幅度的集体振动。 1.56 THz处的吸收主要是由3号羧基绕x轴转动、 a与c两处的羟基伸缩振动(a处羟基向内伸缩、 c处羟基向外伸缩), 与2号羧基及其所在的碳环集体绕y轴转动造成的。 2.76 THz处的吸收峰主要由1号羧基的向内伸缩振动, c处的羟基向外伸缩振动, 和红圈内两个碳环绕x轴扭转形成。
通过分析发现, 甘草酸分子特征吸收峰振转模式的产生主要是由含氧官能团(—COOH、 —OH)的扭转和振动造成的, 另外还包括碳环的小幅振动, 且碳环的振动多是由侧链的甲基或氢原子引起的。
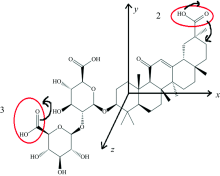
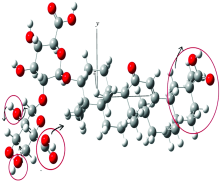
由于甘草酸分子平面结构来源于分子构象图, 在Gaussian09计算产生的输出文件中, 可以将甘草酸分子输出构象图提取出来。 在此仅列出1.56 THz处甘草酸分子输出构象, 标识出振转分子基团, 以便与平面结构下的振转模式图进行观察对比。
分析了甘草酸的分子结构, 利用半经验理论中的PM3算法, 对甘草酸分子进行了几何优化和频率计算, 通过计算得到了甘草酸分子的THz吸收谱。 理论计算表明, 甘草酸分子的四个特征吸收峰分别位于0.87, 1.17, 1.56以及2.76 THz处, 不同峰位的振转幅度与振转模式有差别, 但是主要与甘草酸分子中的羧基、 羟基(—COOH、 —OH)振转有关。 这说明了含氧官能团对甘草酸分子的太赫兹吸收峰产生有着重要影响。 本文不仅可以为甘草中的其他成分研究提供重要参考, 而且在研究中草药成分的过程中, 具有一定的借鉴性。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|