作者简介: 薛长国, 1978年生, 安徽理工大学材料科学与工程学院副教授 e-mail: chgxue@foxmail.com
工业的发展导致大量染料被排放到水体中, 对水环境造成严重污染, 危害整个生态系统, 因此开发便携快速的检测技术至关重要。 表面增强拉曼光谱技术具有单分子水平检测灵敏度高、 检测周期短、 分子指纹特异性等优点, 在水体有机染料检测领域的应用受到广泛关注, 但是该技术依赖于高增强能力和高信号重现性的可靠底物, 而底物的合成大多使用有毒有害原料, 会带来潜在的环境风险。 无毒化学品、 对环境无污染的溶剂和可再生材料的利用是绿色合成策略中值得重点考虑的因素。 采用水热法绿色合成纳米银并用于表面增强拉曼技术, 检测水体中的有机染料。 首先采用了一种简单、 快速、 绿色合成的方法, 以海藻酸钠为还原剂和稳定剂, 水为反应介质, 通过水热还原硝酸银实现了纳米银水溶胶的制备, 得到本实验的可靠底物。 用紫外-可见分光光度法和透射电子显微镜分析了纳米银的结构和表面形貌, 结果表明, 制得的纳米银水溶胶粒径较大, 分布较宽, 分散良好且呈球形, 颗粒平均直径为46 nm。 将三种染料(亚甲基蓝、 罗丹明B和碱性品红)配置成不同浓度梯度的溶液, 然后与制备好的银胶混合用于表面增强拉曼检测。 检测染料溶液的拉曼光谱, 查阅文献分配指认特征峰; 染料纯溶液在1×10-3 mol·L-1浓度时能检测出拉曼特征峰, 但在1×10-4 mol·L-1及更低浓度时已无特征峰; 检测银胶的拉曼光谱, 其并没有拉曼光谱峰, 表明银胶对混合液的拉曼光谱并没有背景影响; 银胶混合液的拉曼光谱特征峰位在低浓度梯度仍比较明显。 结果表明, 通过该方法绿色合成的纳米银对三种染料均有较好的拉曼增强作用, 灵敏度能达到10-6 mol·L-1。 随着人们对环境保护的重视, 以绿色方法合成的纳米银作为可靠基底的表面增强拉曼技术将在染料废水检测领域具有更广阔的应用前景。
The development of industry has caused a large number of dyes to be discharged into water bodies, causing serious pollution to the water environment and harming the entire ecosystem. Therefore, it is important to develop portable and rapid detection technology. Surface-enhanced Raman spectroscopy has the advantages of high single-molecule level detection sensitivity, short detection cycle, and molecular fingerprint specificity. Its application in the field of water organic dye detection has received widespread attention, but this technology relies on reliable substrates with high enhancement and high signal reproducibility, but the synthesis of substrates mostly uses toxic and hazardous materials, posing potential environmental risks. The use of non-toxic chemicals, non-polluting solvents and renewable materials are important considerations in green synthesis strategies. In summary, this paper adopts a hydrothermal method to green synthesize nano-silver and use it in surface-enhanced Raman technology to detect organic dyes in water. First, a simple, fast, and green synthesis method was adopted, using sodium alginate as the reducing agent and stabilizer, and water as the reaction medium. The nano-silver hydrosol was prepared by hydrothermal reduction of silver nitrate, and a reliable substrate for this experiment was obtained. The structure and surface morphology of nano-silver were analyzed by UV-visible spectrophotometry and transmission electron microscopy. The results showed that the prepared nano-silver hydrosol had a large particle size, a wide distribution, a good dispersion and a spherical shape, and an average particle diameter 46 nm. Three dyes (methylene blue, rhodamine B, and basic fuchsin) were formulated into solutions of different concentration gradients and then mixed with the prepared silver gum for surface-enhanced Raman detection. The Raman spectrum of the dye solution was detected, and the characteristic peaks were identified by reference to the literature. Raman characteristic peak can be detected when the concentration of the pure solution is 1×10-3 mol·L-1. However, there was no characteristic peak at 1×10-4 mol·L-1 concentration or lower. The detection of the Raman spectra of the silver gum showed that there was no Raman peak, indicating that the silver gum had no background effect on the Raman spectra of the mixture. The Raman spectral characteristic peak position of the silver gum mixture is still relatively obvious at low concentration gradients. These results show that the Nano-silver synthesized by this method has a good Raman enhancement effect on the three dyes, and the sensitivity can reach 10-6 mol·L-1. With the emphasis on environmental protection, the surface-enhanced Raman technology using Nano-silver synthesized by green method as a reliable substrate will have a broader application prospect in the field of dye wastewater detection.
染料的大规模生产和广泛应用给地球生态带来了相当大的影响, 对水环境污染非常严重。 然而, 对染料组分痕迹的检测和鉴定极具挑战性。 传统色谱和光谱工具难以检测到微弱的光谱和化学信息[1]。
近年来, 表面增强拉曼光谱(SERS)在水体检测领域表现了巨大潜力。 自1974年被人们发现以来, 该技术显示出极高的灵敏度和特异性[2, 3], 因此SERS是研究水溶液中化合物和生物样品的理想工具[4]。 SERS是一种基于金属纳米颗粒表面分子吸附的痕量物质的定量分析技术, 在金属纳米粒子中, 纳米银(AgNPs)因有优良的光学、 电子特性, 出色的抗菌活性和催化性等性能而得到广泛应用。 如今, 制备纳米银的方法有很多, 如机械球磨法、 电化学还原法、 液相化学还原法、 微波处理等。 在这些方法中, 化学还原法由于其制备简单、 成本低、 易于对银纳米粒子的尺寸和形状进行控制而得到广泛的应用。 柠檬酸钠、 硼氢化钠、 水合肼、 苯胺是合成纳米银的常用还原剂。 但是, 由于它们的毒性和生物相容性, 会造成严重的环境污染。 因此使用无毒化学品、 环境友好溶剂和可再生材料是未来材料合成发展的趋势。
海藻酸钠(sodium alginate, SA)是一种从海藻中分离出来的天然碳水化合物聚合物[5], 由于其生物相容性, 低毒性, 相对低的成本以及通过添加二价阳离子如Ca2+而温和凝胶化而广泛用于食品和饮料, 制药和生物工程工业。 藻酸盐的羧基可以与Ag+静电相互作用形成络合物, 羟基将Ag+还原为Ag0, 随后原子聚结, 形成金属团簇; 由于静电斥力和空间效应, 含有羧基的藻酸盐碎片产生的表面负电荷稳定了纳米颗粒, 使其不与下一个颗粒聚集, 从而制得AgNPs。
本工作采用一种简单, 快速和完全绿色的方法合成AgNPs, 使用海藻酸钠作为还原剂和稳定剂, 水作为反应介质, 通过水热法进行合成, 并将其用于有毒染料的表面增强拉曼光谱检测中。 使用紫外-可见分光光度计和透射电子显微镜进行纳米银的表征与分析。 进一步, 对低浓度的染料(亚甲基蓝、 罗丹明B、 碱性品红)溶液进行SERS的检测, 为后续绿色化学制备AgNPs及水体检测提供研究基础。
鼓风干燥箱, 型号DHG-9247A; 紫外-可见分光光度计, 型号UV1901PC; 透射电子显微镜, 型号Tecnai G2 20; 785 nm激光器, 型号Laser785-5HS; 光纤探头, 型号RPB-785-1.5-SS; 光栅光谱仪, 型号Omini-λ 5008i; Andor CCD, 型号iVac-316-CCD。
海藻酸钠(SA), 化学纯; 硝酸银(AgNO3), 分析纯; 亚甲基蓝(MB), 分析纯; 罗丹明B(RhB), 分析纯; 碱性品红(BF), 分析纯; 去离子水。
通过在水溶液中用海藻酸钠水热还原AgNO3实现了AgNPs的制备。 将30 mL去离子水、 1 mL 0.04 mol· L-1 AgNO3和1.6 mL 0.5%海藻酸钠溶液在室温下混合, 得到混合均匀的溶液, 混合物转移到50 mL不锈钢反应釜中, 将反应釜放置在鼓风干燥箱内, 加热至120 ℃, 6 h后取出反应釜, 冷却至室温, 产物离心, 沉淀物分散到40 mL 0.05%海藻酸钠水溶液形成纳米银水溶胶[6]。
使用紫外-可见分光光度计来进行UV-Vis光谱测量。 具体表征方法为: 取2 mL纳米银水溶胶于石英比色皿中, 将比色皿置于分光光度计样品槽中测量, 参比溶液为去离子水。 紫外扫描波长范围为300~800 nm。
利用透射电子显微镜(TEM)观察和表征纳米银颗粒的形态和尺寸。
调制不同浓度梯度的亚甲基蓝、 罗丹明B、 碱性品红, 将其与纳米银水溶胶混合后进行表面增强拉曼检测, 设置不同的光谱参数, 采集拉曼光谱, 分析图谱。
本实验使用天然生物聚合物藻酸盐以“ 绿色” 方法合成AgNPs。 藻酸盐起到还原剂和稳定剂的双重作用。 所制备的纳米银水溶胶呈黄棕色。
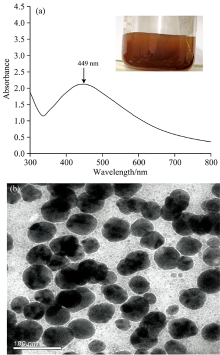
通过紫外-可见分光光度计和透射电子显微镜对AgNPs进行表征。 图1(a)为室温下所制备的纳米银水溶胶的UV-Vis光谱图, 图中显示样品的表面等离子吸收峰波长449 nm, 表明溶液中存在纳米银[7]; 峰形较宽, 表明制得的纳米银水溶胶粒径较大, 分布较宽。 放置半个月后, 其UV-Vis光谱图并未发生明显变化, 可以证明所制备的纳米银水溶胶是稳定的。 图1(b)为纳米银水溶胶的TEM图像。 TEM分析表明AgNPs分散良好且呈球形, 颗粒平均直径为46 nm。
亚甲基蓝(methylene blue, MB)是一种阳离子染料, 可使棉花、 丝绸和木材染色。 吸入MB会导致呼吸困难, 而通过口摄入MB会引起恶心, 呕吐和精神错乱[8]。
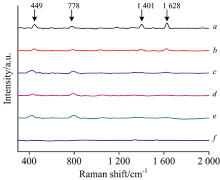
配置不同浓度的MB水溶液并用保鲜膜封好。 检测不同浓度的MB纯溶液的拉曼光谱, 拉曼光谱检测参数设置均相同, 样品功率为100 mW, 积分时间15 s, 累计次数2次。 图2中从谱线f中可知银胶并没有拉曼光谱峰, 说明银胶对混合液的拉曼光谱并没有背景影响; a— e为MB纯溶液的拉曼光谱, MB溶液浓度在5× 10-4 mol· L-1时449, 778, 1 401和1 628 cm-1附近能检测到特征峰, 查阅文献知在449, 1 401和1 628 cm-1附近的MB特征峰归属于C— C, C— H伸缩和C— N— C骨架弯曲振动[9]。 随着MB溶液浓度的降低, 特征峰基本消失, 普通拉曼已检测不出。
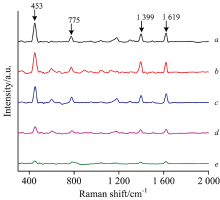
取1 mL纳米银水溶胶与1 mL不同浓度的亚甲基蓝溶液混合后, 将其置于超声波仪器中超声5 min后, 静置2 h。 将不同浓度的MB银胶混合液置于石英比色皿中进行拉曼检测, 参数设置如2.2节。 图3(a— e)为不同浓度的MB银胶混合液SERS光谱, 图中MB浓度在5× 10-4, 5× 10-5, 2.5× 10-5和2.5× 10-6 mol· L-1时均能检测到四个特征峰, 而且特征峰明显; MB浓度在2.5× 10-7 mol· L-1时特征峰不显著, 但仍能观察到峰位。
图2与图3相比较, 可以得出结论: 通过水热法绿色合成的纳米银对低浓度的MB溶液有明显的SERS效应, 检测浓度能达到2.5× 10-7 mol· L-1。
罗丹明B(Rhodamine B, RhB)是一种合成的有机红色染料, 具有高溶解度, 广泛用作食品中的着色剂和水示踪剂荧光, 但对人和动物具有致癌、 生殖和神经毒性等[10]。
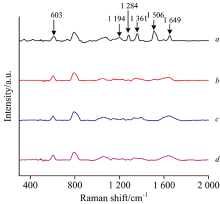
配置不同浓度的RhB水溶液并用保鲜膜封好。 检测不同浓度的RhB纯溶液的拉曼光谱, 拉曼光谱参数设置均相同, 样品功率为350 mW, 积分时间20 s, 累计次数4次。 图4中a— d为RhB纯溶液的拉曼光谱, RhB溶液浓度在1× 10-3 mol· L-1时603, 1 194, 1 284, 1 361, 1 506和1 649 cm-1附近能检测到特征峰, 查阅文献知这些特征峰分别归属于环变形振动、 C— H面内弯曲振动、 C— C桥梁伸缩振动、 芳香族C— C伸缩振动、 芳香族C— C伸缩振动和芳香族C— C伸缩振动[11]。 随着RhB纯溶液浓度的降低特征峰逐渐消失, 普通拉曼已检测不出。
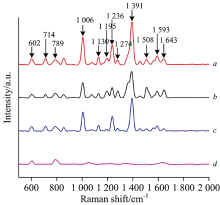
取1 mL纳米银水溶胶与1 mL不同浓度的RhB溶液混合后, 将其置于超声波仪中超声5 min后, 静置2 h。 将不同浓度的RhB银胶混合液置于石英比色皿中进行拉曼检测, 参数设置保持不变。 图5(a— d)为不同浓度的RhB银胶混合液SERS光谱, 图中RhB浓度在1× 10-3, 1× 10-4, 1× 10-5和1× 10-6 mol· L-1均能检测到上述四个特征峰, 而且特征峰明显, 在714, 1 006, 1 130, 1 236, 1 391和1 593 cm-1处出现了新的特征峰, 这是RhB纯溶液所不具有的。
图4与图5相比较, 可以得出结论: 通过水热法绿色合成的纳米银溶胶对低浓度的RhB溶液有明显的SERS效应, 检测浓度能达到1× 10-5 mol· L-1。
碱性品红(basic fuchsin, BF)是三苯甲烷染料, 广泛用于纺织、 化学分析和微生物染色。 但其生物降解性差, 有毒性和致癌性[12]。
配置不同浓度的BF水溶液并用保鲜膜封好。 检测不同浓度的BF纯溶液的拉曼光谱, 拉曼光谱参数设置均相同, 样品功率为100 mW, 积分时间5 s, 累计次数1次。 图6中a— d为BF纯溶液的拉曼光谱, BF溶液浓度在1× 10-3 mol· L-1时419, 1 176, 1 374和1 590 cm-1附近能检测到特征峰, 根据文献这些振动带分别被指定为平面外苯环变形, C— H弯曲, N-苯基拉伸和平面内环拉伸弯曲振动[12]。 随着BF纯溶液浓度的降低特征峰基本消失, 普通拉曼光谱已检测不出。
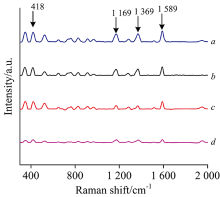
取1 mL纳米银水溶胶与1 mL不同浓度的BF溶液混合后, 将其置于超声波清洗仪中超声5 min后, 静置2 h。 将不同浓度的BF银胶混合液置于石英比色皿中进行拉曼检测, 参数设置保持不变。 图7为不同浓度的BF银胶混合液SERS光谱, 图中BF浓度在1× 10-3~1× 10-6 mol· L-1均能检测到上述四个特征峰, 而且特征峰明显, 在418, 1 169, 1 369和1 589 cm-1处出现了新的特征峰, 这是BF纯溶液所不具有的。
图6与图7相比较, 可以得出结论: 通过水热法绿色合成的纳米银对低浓度的BF溶液有明显的SERS效应, 检测浓度能达到1× 10-6 mol· L-1。
针对传统工具对水中有毒染料的检测存在费用高昂、 灵敏度低等缺点, 提出利用表面增强拉曼光谱技术对有毒染料进行检测, 该方法具有制样简单、 检出限高、 重现性好等优点。 同时, 为了遵循“ 绿色化学” 的主旨, 使用海藻酸钠作为还原剂和稳定剂, 在水热条件下合成了纳米银溶胶, 作为表面增强拉曼光谱的可靠基底, 能够有效增强拉曼信号。 利用TEM和UV-Vis对所合成的纳米银进行了表征, 表明制得的纳米银溶胶粒径较大, 分布较宽。 配置不同浓度梯度的染料(MB, RhB和BF)溶液, 并与纳米银溶胶混合进行SERS研究。 结果表明, 该纳米银溶胶作为表面增强拉曼光谱基底, 能够检测出10-6 mol· L-1的染料溶液, 且能猝灭染料的荧光, 使其特征峰均能很好地显示, 表明该纳米银粒子具有非常高的表面增强拉曼光谱活性。 纳米银水溶胶SERS具有高灵敏度和检测速度, 用作水中染料的痕量检测表现优异, 有着巨大的应用前景。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|