作者简介: 沙文, 1982年生, 安徽大学电气工程与自动化学院副教授 e-mail: ahu001@163.com
复混肥成分的快速、 原位检测对化肥的生产过程、 产品质量控制具有重要的意义。 在化肥企业生产中, 实验室进行分析, 检测时间长, 无法实现线上检测。 与复混肥成分现有检测方法相比, 激光诱导击穿光谱(LIBS)检测时间只需几分钟、 一次测量可完成复混肥成分检测、 几乎无需样品预处理, 将该技术用于复混肥成分快速、 现场检测非常合适。 搭建LIBS系统, 激光器(100 mJ, 1 064 nm, 1 Hz)输出的激光束经45°反射镜由水平转为垂直方向, 经焦距为40 mm的透镜聚焦至旋转台上的复混肥样品表面, 产生激光等离子体。 激光器的调Q信号控制光纤光谱仪(Avantes, 195~500 nm)采集信号, 设置光谱延迟时间为1.28 μs, 采集时间为1.05 ms, 最终获取复混肥样品LIBS光谱。 20个复混肥样品由安徽徽隆集团提供, 磷元素的参考值由企业采用国家标准方法测量。 将复混肥样品粉碎过筛取3 g, 采用压片机在8 MPa下压制成形。 实验中, 使用小型风扇吹扫复混肥样品表面, 形成稳定气流, 每个样品重复测量10次, 每次测量平均20个脉冲, 以减小样品不均匀性。 其中, 15个样品用于定标回归模型的建立, 五个样品用于检验定标模型的适用性。 复混肥是一种成分复杂的混合物, 其中氮、 磷、 钾均以化合物存在。 传统的LIBS定量方法是基于待测元素单条谱线强度, 未考虑其他元素影响, 降低了定量结果的准确性。 将LIBS技术和多元线性回归法结合用于分析复混肥中磷元素浓度。 选取磷元素的三条特征谱线即213.6, 214.9和215.4 nm。 磷矿中硅元素含量基本不变, 且硅元素在磷的谱线附近存在多条谱线, 如212.4, 220.8, 221.1和221.7 nm。 分别采用一元、 二元、 三元和四元线性回归法建立校准曲线。 结果表明, 采用P Ⅰ: 214.9 nm谱线强度作自变量建立一元线性回归, LIBS预测值与参考浓度的相关系数仅为0.083, 无法满足磷元素的定量分析要求。 当采用P Ⅰ: 214.9 nm谱线强度和三条特征谱线之和(P Ⅰ: 213.6, 214.9和215.4 nm)作自变量建立二元线性回归拟合时, 相关系数提高到0.856, 平均绝对误差由1.32%减小到0.16%。 在二元线性回归中引入Si Ⅰ: 212.4 nm谱线强度, 建立三元线性回归, 相关系数为0.869。 为进一步提高磷元素浓度测量的准确性, 建立四元线性回归方程, 将Si Ⅰ: 212.4, 220.8, 221.1和221.7 nm谱线强度之和作为自变量加入三元线性回归, 相关系数提高到0.980, 且15个定标样品的相对误差范围为0.06%~1.31%, 而验证样品为0.13%~1.26%, 这说明采用四元线性回归定标法可提高复混肥中磷元素浓度测量的准确性。
The rapid and in-situ detection of compound fertilizer components was of great significance to the production process control and product quality control of chemical fertilizer production enterprises. In the production of fertilizer companies, compound fertilizer samples were collected on the production line and sent to the laboratory for analysis. The time required for detecting was long, which can’t meet the compound fertilizer company’s production line for testing. Compared with the existing detection methods of compound fertilizer components, the detection time of laser-induced breakdown spectroscopy (LIBS) was several minutes. And the measurement of compound fertilizer components can be completed in one measurement, with almost no need for compound fertilizer samples. LIBS technique was very suitable for the rapid and on situ detection of compound fertilizer components. In the LIBS detection system, the laser beam output from the solid-state pulse laser (100 mJ, 1 064 nm, 1 Hz) was converted from horizontal to vertical by a 45°-mirror. The laser beam was focused onto the target using a lens (focal length=40 mm). The sample was placed at a rotating platform. The light emitted by the plasma was collected by an optical fiber spectrometer (Avantes, 195~500 nm) with a delay time of 1.28 μs and an integration time of 1.05 ms. The spectrometer was triggered by the signal of laser’s Q-switched. The LIBS spectrum of the compound fertilizer sample was finally obtained. In the experiment, 20 compound fertilizer samples were provided by Anhui Huilong Group. The reference concentration of phosphorus element was measured by the enterprise using the national standard method. The samples were ground into powder and sieved. Three grams of every sample was pressed pellets under a pressure of 8 MPa. During the experiment, a small fan was used to continuously purge the surface of sample to form a stable airflow environment. Each sample was repeatedly measured 10 times, and each spectrum was formed by 20 shot average to reduce the heterogeneity of the sample. 15 samples were selected as calibration set to train regression model, and 5 samples were chosen to test the model. The compound fertilizer was a complex mixture of components, in which the nitrogen, phosphorus, and potassium were all present as compounds. The traditional quantitative analysis method of LIBS was based on the intensity of a single characteristic line of the measured element. The influence of other elements was not considered, which greatly reduced the accuracy of the analysis results. In this paper, LIBS technology and multiple linear regression calibration were used in combination to determine the phosphorus concentration in compound fertilizer. Three feature spectral lines of P element detected by LIBS were 213.6, 214.9 and 215.4 nm. As the concentration of silicon in the phosphate rock was relatively stable. And near the spectral feature line of P element, there were many characteristic lines of Si element, such as 212.4, 220.8, 221.1 and 221.7 nm. The analysis was carried out based on unary, binary, ternary, and quaternary linear regression calibration curves, respectively. It turned out that the unary linear regression method hardly served the quantitative analysis for compound fertilizer sample only using the intensity of P Ⅰ 214.9 nm as variable, and the correlation coefficient between the LIBS prediction value and the reference concentration was only 0.083. When using the intensity of P Ⅰ: 214.9 nm and the sum of three characteristic lines (P Ⅰ: 213.6, 214.9 and 215.4 nm) as input variables to establish the binary linear regression, the correlation coefficient increased to 0.856 and the average absolute error decreased from 1.32% to 0.16%. When introducing the line intensity of Si Ⅰ: 212.4 nm into the binary linear regression equation, the ternary linear regression was established, and the correlation coefficient was only increased to 0.869. In order to further improve the accuracy of phosphorus concentration measurement in compound fertilizers, the quaternary linear regression equation was established. The sum of the Si Ⅰ: Si 2.4: 222.4, 220.8, 221.1 and 221.7 nm line intensities was used as an independent variable to add into ternary linear regression equation. The correlation coefficient was increased to 0.980. The relative error ranges were 0.06%~1.31% and 0.13%~1.26% for 15 calibration samples 5 validation samples, respectively. The results demonstrated that using the quaternary liner regression calibration method can improve the accuracy of phosphorus concentration measurement in compound fertilizers.
复混肥是以矿物、 空气和水为原料, 经化学反应及机械加工而成的肥料。 农作物生长过程中必须吸收一定的营养元素, 通过合理施用复混肥, 可促进农作物快速生长。 我国农业上每年消耗大量的肥料, 肥料产品的质量检验非常重要。 (1)复混肥在贮存、 运输和使用过程中, 应避免包装混淆, 因此必须了解复混肥的品种和成分; (2)假冒伪劣复混肥对农业的危害极大, 施用该种复混肥会耽误农作物的生长发育, 甚至导致农作物的死亡; (3)复混肥的正确施用能够促进作物的生长, 相反, 如果不正当的施用则会造成不良的后果, 甚至作物不生长并且对土质的营养含量起到破坏的作用。 现阶段, 复混肥生产企业主要采用在生产线上采集样品, 送至化验室进行分析, 检测方法包括: 国家标准方法、 原子吸收光谱法(AAS)、 激光拉曼光谱仪(LRS)、 紫外分光光度计法(UV)、 火焰原子吸收光谱法(FAAS)、 电感耦合等离子体发射光谱法(ICP-AES)、 近红外漫反射法(NIR)光谱等方法[1, 2, 3]。 上述方法中除近红外漫反射光谱技术无需对复混肥样品进行预处理外, 其他方法需对复混肥样品进行预处理, 检测时间长, 无法实现在线检测。 而近红外漫反射光谱技术对于复混肥中五氧化二磷、 氧化钾、 微量元素和重金属元素等无机成分无法精确测定。 为了实现复混肥生产过程中在线监测控制, 急需发展新的检测技术。
与现有的检测技术相比, 激光诱导击穿光谱(laser-induced breakdown spectroscopy, LIBS)是一种新的光谱检测方法。 它是将高能量的激光脉冲聚焦到待测样品表面, 样品汽化产生等离子体光谱信号, 再采用光谱仪完成信号的采集。 理论上可根据发射光谱谱线对应的波长和强度就分析得到所测样品的组成及浓度。 由于该技术最小测量周期为毫秒量级、 所需样品量少、 多元素同时检测、 分析不同形态样品、 可用光纤传输实现原位测量等特点, 已在很多领域得到广泛应用[4, 5, 6, 7]。
近年来已有研究者开展采用LIBS技术分析化肥成分。 Farooq等[8]对化肥中的P, Mg和Mn等元素进行了测量分析, 但是文中并没有具体给出每个元素的检测限。 Daniel Fernandes Andrade等[9]将液态化肥变成固态并采用LIBS进行测量, 对化肥中的Cu, K, Mg, Mn, Zn, As, Cd, Cr和Pb进行了分析, 检测误差为0.02%~0.06%。 Bruno S Marangoni等[10]采用LIBS对26个不同的有机肥和无机肥料中磷元素进行了分析, 对光谱进行基线校正和峰值强度归一化, 提高了LIBS测量值与真实值间的相关性, 但对2个验证样品的测量绝对误差接近5%。 Yao[11]等对复合肥中的磷和钾元素进行分析, 采用Unscrambler软件中的PLS方法建立了定量模型, 得到的结果优于传统分析方法。 Daniel F Andrade[12]采用LIBS技术直接分析了固体复合肥料中的Cd, Cr, Pb, B, Cu, Mn, Na, Zn, Ca和Mg等元素, 通过优化检测系统参数, 并将定量分析结果与ICP-OES进行对比, 相关性较好, 并确定上述元素检测限为2 mg· kg-1~1%。 Senesi等[13]采用单脉冲、 双脉冲LIBS对磷矿石和有机矿物磷肥进行了测量, 并采用PCA和PLSR两种方法对样品进行识别, 识别结果可达到95%的置信水平, 说明LIBS技术可用于原位快速分类磷肥。 上述研究工作的开展证明LIBS技术可以用于化肥成分检测和种类识别, 但实现在线检测, 尚有很多问题需要解决。
由于复混肥中磷元素的原材料为矿石, 基体效应较严重, 导致待测元素的发射谱线强度和浓度之间往往偏离简单的线性关系。 同时, 复混肥中氮、 磷、 钾元素以化合物形式存在, 而传统的单变量方法是基于元素谱线强度和元素浓度建立的, 没有考虑其他元素的影响, 使得分析结果准确性大大降低。 近几年来, 很多研究者在LIBS测量过程中采用多变量分析, 利用多元素的多条特征谱线信息, 可一定程度上消除元素间相互干扰和谱线波动, 从而提高分析结果的准确性。 Chen等[14]采用多元线性定标法对马铃薯中的Cr元素进行分析, LIBS测量结果与AAS间的相关性为0.987, 验证样品的预测浓度相对偏差小于5.5%。 本文采用安徽徽隆集团提供的复混肥样品为测量对象, 复混肥中五氧化二磷元素含量由生产企业采用国家标准方法检测确定。 用LIBS完成复混肥中磷元素的测量, 并采用多元线性回归定标法对磷元素浓度进行定量分析。
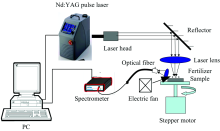
已有的LIBS检测系统包括: 固体脉冲激光器(BigSky, ICE450, 100 mJ, 1 064 nm, 1 Hz)、 光纤光谱仪(Avantes, 195~500 nm)、 样品台、 激光聚焦装置、 光谱收集装置和数据处理系统。 激光聚焦装置主要包括反射镜片和聚焦镜, 样品池包括载物台和旋转电机, 光谱收集装置包括透镜组和光纤, 数据处理系统为计算机。 如图1所示, 脉冲激光器输出的激光束经45° 反射镜由水平方向变为垂直方向, 再经透镜聚焦到复混肥样品表面, 产生激光等离子体, 到达复混肥样品表面的峰值功率密度为2.2 GW· cm-2。 复混肥样品被激发产生等离子体, 经过1.28 μ s的延迟时间等离子体信号经聚焦透镜收集并会聚到光纤上, 传输至光谱仪进行分光和探测, 由计算机获取LIBS光谱。 调节样品台上步进电机的转速, 保证电机转一圈时间为20 s, 每次测量平均20个激光脉冲照射到样品, 并进行10次重复测量, 对每次测量得到的特征谱线采用Matlab进行洛伦兹线型拟合得到光谱强度。 采用小型风扇对复混肥样品表面进行持续吹扫, 形成稳定的气流环境。
将20个不同磷元素的复混肥样品粉碎, 每个样品取3 g, 放进直径为25 mm的模具内, 在压强为8 MPa的压力下压制成形, 厚度约为2 mm。 表1给出的是20个复混肥样品中磷元素浓度值, 多元线性定标回归模型采用前15个复混肥样品, 16— 20号样品为验证样品, 用于检验定标模型的适用性。
| 表1 20个复混肥样品中磷元素含量 Table 1 Phosphorus concentrations of 20 compound fertilizer samples |
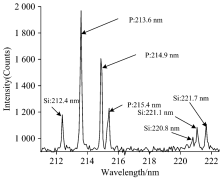
波长范围211~221 nm的复混肥样品LIBS光谱如图2所示。 复混肥生产企业一般采用磷矿石作为原材料, 从图2中可以看出复混肥样品中含有丰富的Si和P元素特征谱线。 表2给出磷元素和硅元素特征谱线的相关参数[15]。 在212~216 nm范围内的LIBS光谱中, 磷元素的213.6, 214.9和215.4 nm三条特征谱线可以被清晰的观测到, 其中, 213.6 nm特征谱线的强度最大。 磷元素的三条特征谱线均不受其他元素干扰。 硅元素的特征谱线主要有212.4, 220.8, 221.1和221.7 nm, 其中, 212.4 nm这条特征谱线的强度最大。
| 表2 Si和P元素特征谱线的特征参数 Table 2 Characteristic parameters of lines of Si and P elements |
目前, 激光诱导击穿光谱技术采用最传统的定标曲线是假设等离子体处于局部热平衡状态下, 可采用式(1)表达:
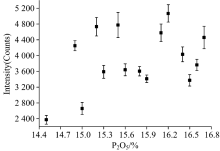
其中b称为自吸收系数, 自吸收现象一般是待测元素浓度较高时, 元素特征谱线出现饱和。 复混肥中磷元素属于非金属元素, 从表2中给出的磷元素的跃迁能级可以看出, 激发电位较高, 同时, 图2中给出的LIBS光谱中可以看出, 磷元素的3条特征谱线强度都较低, 没有出现饱和现象, 可认为自吸收系数b=1, 即I=aC。 国内复混肥成分中采用P2O5表示磷元素含量, 对表1中的1— 15号复混肥样品进行定量分析, 以磷元素的P Ⅰ : 214.9 nm特征谱线的拟合强度为纵坐标, 样品中P2O5浓度为横坐标, 建立定标曲线如图3所示, 相关系数r仅为0.082; 对磷元素的其他谱线也建立了定标曲线, 线性回归效果都不好, 说明一元线性回归无法满足复混肥中磷元素浓度定量分析精度。
由于LIBS受到基体元素的干扰较为严重, 复混肥中磷的原材料为磷矿, 含有众多金属元素。 多元线性校正方法可以利用LIBS光谱中多条相应特征谱线信息建立定量分析模型, 一定程度上可减少其他元素的影响, 从而提高测量准确性。 对于具有多种组分的复合肥样品, 待测元素浓度值往往与多种因素有关。 假设待分析元素浓度为c, 所选取的多元素特征谱线强度为I1, I2, …, In。 依据待测元素浓度与LIBS光谱数据的测量值可表示为
其中ei是拟合残差, i是测量次数, m是变量数。
定义
其中, 系数a0, a1, …, am是当Q值最小时计算得到的, 它表示的是影响待测元素浓度的特征谱线强度权重。
磷元素的特征谱线存在的211~221 nm波长范围内, Si元素的特征线较丰富且与磷元素谱线相接近, 如图2所示。 此外, 由于硅元素含量在磷矿中相对稳定, 故考虑Si元素基体效应对复混肥中P元素浓度的影响是合适的。 完成复混肥样品的测量后, 对选取的特征光谱进行处理, 选取P元素的单条谱线强度(P Ⅰ : 214.9 nm), 和P元素的多条谱线强度的总和(P Ⅰ : 213.6, 214.9和215.4 nm), 分别作为自变量, 建立复混肥中磷元素的多元线性回归模型。 即,
然后, 将所选取的复混肥中Si元素特征谱线代入多元线性回归模型,
其中,
采用表1中1— 15号复混肥样品建立定标回归模型, 分别选取一元、 二元、 三元和四元线性回归进行定量分析。 然后建立LIBS预测浓度与参考浓度之间的关系。 基于建立的定量模型, 计算表1中16— 20号验证样品中P元素含量, 用于检验定标模型的适用性。 表3给出了采用不同变量的线性回归法定量分析复混肥中磷元素浓度的结果。 由一元线性回归可看出, 采用P Ⅰ : 214.9 nm谱线作为自变量时, LIBS预测值与参考浓度的线性关系较差, 相关系数仅为0.083, 这说明传统的单变量曲线拟合方法无法满足样品成分复杂的定量分析要求。 当采用P Ⅰ : 214.9 nm谱线强度和P元素的三条特征谱线之和(P Ⅰ : 213.6, 214.9和215.4 nm)作为自变量建立二元线性回归拟合时, 相关系数提高到0.856。 在采用P元素的二元变量基础上, 加入Si Ⅰ : 212.4 nm谱线强度建立三元线性回归拟合, 得到LIBS预测浓度与参考浓度的关系较好, 相关系数增加到0.869。 为了进一步提高LIBS预测浓度与参考浓度的线性关系, 建立四元线性回归分析, 将Si元素的四条特征谱线强度线(Si Ⅰ : 212.4, 220.8, 221.1和221.7 nm)之和作为自变量加入三元线性回归分析。 结果表明, LIBS测量浓度与参考浓度间的线性相关较好, 相关系数提高到0.980。
| 表3 采用不同线性回归方法定量分析复混肥中磷元素 Table 3 Quantitative analysis of P in compound fertilizer by different linear regression methods |
通过比较定量线性回归分析方法的结果(表3), 四元线性多元回归模型最佳, LIBS预测值与参考值间的R2提高到0.980, 20个复混肥样品的平均绝对误差最小, 仅为0.11%。 采用四元线性回归模型确定复混肥中P元素浓度, 依据实验数据所建立的回归方程可以表示为
采用回归方程(7)对20个复混肥样品中P元素浓度进行预测, 1— 15号用于建立回归模型的复混肥样品的LIBS预测值与参考值间的线性关系如图4(a)所示, R2为0.980。 将获取的16— 20号验证样品的LIBS光谱数据代入建立的四元回归方程, 得到磷元素浓度的预测值。 图4(b)给出的是LIBS预测值与参考值间的线性关系, 相关系数R2为0.985, 这表明LIBS测量的准确度得到有效改进。 从方程(7)中可以看出, 硅元素的谱线强度对磷元素浓度影响较大, 这是由于复混肥生产中采用磷矿作为磷元素的原材料。 磷矿中含量有大量的基体元素硅, 其特征谱线位于磷元素特征谱线附近,由于LIBS技术受待测样品的基体效应影响严重, 使得所建立的多元线性回归方程中硅元素谱线强度贡献较大。
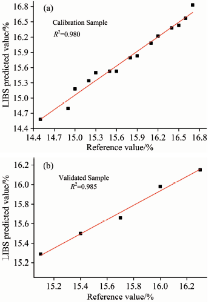 | 图4 LIBS预测值与参考值间线性关系 (a): 15个定标样品; (b): 5个验证样品Fig.4 Comparison between predicted value and reference value (a): Fifteen calibration samples; (b): Five validated samples |
在测量中可采用绝对误差(absolute error)来衡量LIBS测量结果的准确性, 它的计算公式为LIBS测量值与参考值间差值的绝对值。 相对误差为绝对误差除参考值, 它可以表示每个待测样品测量结果的准确性。 20个复混肥样品LIBS测量结果的绝对误差和相对误差如表4所示。 其中, 1— 15号定标样品的绝对误差和相对误差范围为0.01%~0.20%和0.06%~1.31%; 16— 20号验证样品的绝对误差范围为0.02%~0.19%, 相对误差范围为0.13%~1.26%。 本实验过程中采用小型风扇一直对复混肥样品产生的等离子体进行吹扫, 形成稳定的气体环境, 从而LIBS测量信号的稳定性得到提高。 同时, 由于复混肥企业提供的是质量合格的样品, 20个复混肥样品的浓度范围变化不是很大, 考虑了基体元素硅的影响, 建立多元线性回归方程, 使复混肥中磷元素的LIBS测量准确性得到提高。
| 表4 定标与验证样品的定量分析结果 (四元线性回归模型) Table 4 Quantitative analysis of P for calibration and validated samples (the quaternary linear regression model) |
将LIBS技术和多元线性回归方法结合用于复混肥中磷元素浓度测定。 20个复混肥样品由安徽徽隆集团提供, 分别采用一元、 二元、 三元和四元线性回归校准曲线对15个复混肥样品建立定量分析模型, 并对5个未知浓度复混肥样品进行分析。 结果表明, 对于氮磷钾含量各为15%的复混肥样品, 采用IP作为自变量的一元线性回归法几乎无法对成分复杂的复混肥样品进行定量分析。 二元线性回归采用
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|