作者简介: 王华宇, 女, 1990年生, 长春理工大学化学与环境工程学院化学硕士研究生 e-mail: 824356039@qq.com
采用柠檬酸钠为表面活性剂的水热法制备了NaGd(MoO4)2: xEu3+( x=10%, 20%, 30%, 40%)和NaGd(MoO4)2:7%Eu3+, yS
NaGd(MoO4)2: xEu3+( x=10%, 20%, 30%, 40%) and NaGd(MoO4)2:7%Eu3+, yS
由于white light emitting diode(WLED)具有亮度高、 功耗低、 耐久性、 效率高、 环保等优点, 及其符合全球节能减排与保护环境的需求, 因此极大加快了白光LED取代传统的荧光灯和白炽灯的步伐[1]。 目前实现WLED的形式主要有三种[2], 其中最理想的方式是将近紫外LED芯片与可被近紫外有效激发而发射红、 绿、 蓝三基色发光体有机结合[3]。 传统的WLED是由蓝光InGaN芯片和黄色的YAG荧光粉结合而成的, 因为缺少红光成分, 使得产品的显色指数较低(Ra< 80), 而且色温较高(Tc> 7 000 K)[4]。
双钼酸盐ALn(MoO4)2(A是碱金属离子, Ln是三价稀土离子)是典型的白钨矿化合物, 四面体对称, NaLn(MoO4)2化合物每个单元晶胞中有两个Ln3+, 两个Na+, 四个Mo
本工作通过水热法制备了不同Eu3+掺杂量的NaGd(MoO4)2, 由于低浓度Eu3+掺杂的NaGd(MoO4)2的发光强度不理想, 所以引入S
氧化铕, 氧化钆(纯度: > 99.99%, 长春海普瑞稀土材料技术有限公司), 硝酸(纯度: 65%~68%, 北京化工厂), 钼酸钠(分析纯, 北京化工厂), 柠檬酸钠(分析纯, 北京化工厂), 硫酸钠(分析纯, 北京化工厂), 硼酸钠(分析纯, 北京化工厂), 无水乙醇(纯度: ≥ 99.7%, 北京化工厂), 去离子水为实验室自制。
以制备NaGd(MoO4)2:7%Eu3+, yS
样品结构用Rigaku D/max-IIB型X射线衍射仪(Cu Kα 1射线, λ =1.540 5 Å )进行表征, 工作电压30 kV, 扫描速度为4° (2θ )/min, 工作电流30 mA, 步长为0.02° , 扫描范围10° ~90° ; 采用日本Hitachi F-7000荧光光谱仪测量荧光粉的激发及发射光谱, 氙灯作激发光源, 扫描速度1 200 nm· min-1; 用Shimadzu-8400s红外光谱仪(FTIR)确定样品中官能团; 粒子形貌和尺寸采用PhilipsXL-30型扫描电子显微镜(SEM)进行表征。 所有测试都在室温下进行。
如图1所示样品在(101), (112), (004), (200), (204), (220), (116), (312), (224), (208), (316)处有明显的衍射峰, 通过与标准卡片PDF#25-0828匹配, 仍然为纯的四方相, 属于I41/a(88)空间群, a=b=0.524 4 nm, c=1.148 7 nm, 过量的Eu3+掺杂不会改变NaGd(MoO4)2晶相, 当S
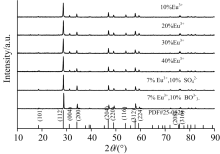 | 图1 NaGd(MoO4)2:xEu3+(x=10%, 20%, 30%, 40%)与NaGd(MoO4)2:7%Eu3+, 10%S |
图3是样品的红外光谱, a, b, c分别表示NaGd(MoO4)2:7%Eu3+, NaGd(MoO4)2:7%Eu3+, 10%S
图4为NaGd(MoO4)2:7%Eu3+的SEM图, 图中可以看出样品为均匀的梭状结构, 平均直径约为0.47 μ m, 平均长度约为1.35 μ m。 图5为样品中掺杂S
 | 图4 不同分辨率下的NaGd(MoO4)2:7%Eu3+的扫描电镜图 内插图为粒径分布图Fig.4 SEM images of NaGd(MoO4)2:7%Eu3+under different magnification The inset picture is the particle size distribution histogram |
图6为NaGd(MoO4)2:xEu3+的荧光光谱, 图6(a)是发射光谱, 在616 nm处有强的发射峰对应于Eu3+的5D0→ 7F2电偶极跃迁, 在593 nm是由5D0→ 7F1磁偶极跃迁产生的, 而且位于616 nm处的电偶极跃迁强度远大于磁偶极跃迁, 因为Eu3+对所处环境敏感, 当电偶极跃迁最强时, Eu3+所处环境的对称性下降, 由此也可知在NaGd(MoO4)2:xEu3+的荧光粉中, Eu3+占据低对称性位置, 由图6(a)也可以看出随着Eu3+浓度的增加Eu3+的特征发射峰先增强后下降, 在Eu3+浓度为30%时达到最强。 图6(b)是激发光谱, 其主要由两大部分构成, 一部分是O— Mo电荷迁移带, 另一部分是由Eu3+的特征激发带构成, 362 nm处对应于7F0→ 5D4, 383 nm对应于7F0→ 5L7, 395 nm处对应于7F0→ 5L6, 417 nm处对应于7F0→ 5D3, 465nm处是7F0→ 5D2。
图7是NaGd(MoO4)2:xEu3+(x=10%, 20%, 25%, 30%, 35%, 40%)的发射光谱, 从图中可以明显看出Eu3+掺杂量为30%时发光最强, 进一步证明NaGd(MoO4)2:30%Eu3+发光最强。 由以上实验确定了NaGd(MoO4)2基质中掺杂大量的Eu3+时发光一直增强, 且掺杂量为30%时发光强度达到最高, 而少量的Eu3+掺杂发光强度不是很强, 所以在基质中引入S
 | 图7 NaGd(MoO4)2:xEu3+(x=10%, 20%, 25%, 30%, 35%, 40%)的发射光谱图Fig.7 Emission spectra of NaGd(MoO4)2:xEu3+(x=10%, 20%, 25%, 30%, 35%, 40%) |
图8是NaGd(MoO4)2:7%Eu3+, yS
图9是NaGd(MoO4)2:7%Eu3+, yB
S和Mo的电负性分别为2.59和2.16, 适当量S
图10是NaGd(MoO4)2:7%Eu3+, 10%S
样品的CIE坐标值列于表1, R表示标准红光的色坐标。 图11是CIE图, 1~4对应于NaGd(MoO4)2:xEu3+(x=10%, 20%, 30%, 40%), 样品色坐标向红光区移动; 5~7分别对应于NaGd(MoO4)2:7%Eu3+, NaGd(MoO4)2:7%Eu3+, 10%S
| 表1 NaGd(MoO4)2:xEu3+(x=10%, 20%, 30%, 40%)和NaGd(MoO4)2:7%Eu3+, y%S |
水热法制备了NaGd(MoO4)2:xEu3+和NaGd(MoO4)2:7%Eu3+, yS
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|










