作者简介: 程方贝贝, 女, 1994年生, 合肥学院生物食品与环境学院硕士研究生 e-mail: c15156040783@163.com
水体重金属铅(Pb)污染对人类健康及水生态环境具有重要影响。 为实现水体重金属Pb的现场快速检测, 以蛋白核小球藻为吸附剂, 开展了基于蛋白核小球藻富集-X射线荧光(XRF)光谱的水体重金属Pb快速检测研究。 结果表明: 蛋白核小球藻与重金属Pb反应液的pH值为7且反应温度为25 ℃时, 蛋白核小球藻对重金属Pb具有快速高效吸附特性, 在反应时间为5 min时对0.012 8~0.353 5 mg·L-1这一较宽浓度范围内重金属Pb的吸附效率高达92%以上, 但对类金属As的吸附效率却低于5%, 因此基于蛋白核小球藻的富集作用可以有效避免重金属Pb与类金属As共存时As的Kα最优特征谱峰对XRF光谱测量过程中Pb的Lα最优特征谱峰的干扰与影响; 在蛋白核小球藻对重金属Pb的最佳吸附反应条件下, 当反应液样品富集量为10 mL时, 建立了基于蛋白核小球藻富集-XRF光谱的水体重金属Pb定量检测方法, 水体重金属Pb浓度与XRF光谱中Pb的Lα特征谱峰净积分荧光强度间具有良好的线性关系, 相关系数 r为0.990, 检测限为7.2 μg·L-1, 低于我国《地表水环境质量标准(GB 3838—2002)》中Ⅰ类水质标准中重金属Pb的标准限值; 采用该方法对合肥市市内派河、 匡河、 南淝河、 四里河及十五里河实际水体水样中重金属Pb进行检测, 回收率均在87.84%~115.66%范围内, 表明所建立的藻富集与XRF光谱法相结合的水体重金属Pb快速检测方法能够很好地应用于实际水体中重金属Pb的快速分析与检测。 该研究为发展水体重金属现场快速监测技术与仪器奠定了方法基础。
The heavy metal lead (Pb) pollution in water impacts human health and the water ecological environment. In order to realize the on-site and rapid detection of heavy metal Pb in water, in this paper, Chlorella pyrenoidosa was used as the adsorbent, and the rapid detection of heavy metal Pb in water based on enrichment by Chlorella pyrenoidosa combined with X-ray fluorescence (XRF) spectroscopy was carried out. The results show that when the pH value of the reaction solution of Chlorella pyrenoidosa and heavy metal Pb was 7. The reaction temperature was 25 ℃, Chlorella pyrenoidosa had the fast and high-efficient adsorption characteristics to heavy metal Pb, when the reaction time was 5 min, the adsorption efficiency of heavymetal Pb in the wide concentration range of 0.012 8~0.353 5 mg·L-1 was as high as 92%, but the adsorption efficiency of metalloid As was lower than 5%. Therefore, the enrichment based on Chlorella pyrenoidosa could effectively avoid the interference and influence of the optimal Kα characteristic peak of As on the optimal Lα characteristic peak of Pb in the XRF measurement process when the heavy metal Pb and metalloid As coexist; Under the optimal adsorption reaction conditions of Chlorella pyrenoidosa for heavy metal Pb, when the enrichment volume of the reaction solution was 10 mL, a quantitative detection method of heavy metal Pb in water based on the combination of Chlorella pyrenoidosa enrichment and XRF spectroscopy was established. There was a good linear relationship between the concentration of heavy metal Pb in water and the net integrated fluorescence intensity of the Lα characteristic peak of Pb in the XRF spectrum with a correlation coefficient r of 0.990. The detection limit of the method was 7.2 μg·L-1, which was lower than the standard limit of heavy metal Pb in the Class Ⅰ water quality standard in “Environmental Quality Standard for Surface Water (GB 3838—2002)” of China. This method was adopted to detect the heavy metal Pb in the actual water samples of Paihe, Kuanghe, Nanfeihe, Silihe and Shiwulihe in Hefei City, and the recoveries were all within the range of 87.84% to 115.66%, indicating that the established rapid detection method of heavy metal Pb in water which combined with enrichment by algal cells and XRF spectroscopy could be well applied to the rapid analysis and detection of heavy metal Pb in actual water. This research will provide a method basis for developing on-site and rapid monitoring techniques and instruments for heavy metals in water.
随着我国采矿、 冶炼、 化工、 电镀、 制革等行业的快速发展[1], 农业化肥与农药的大量施用, 以及人们日常垃圾的不合理堆放, 致使大量的重金属污染物进入水体, 造成了严重的水体重金属污染。 铅(Pb)作为一种典型的重金属污染物, 因具有难以降解性[2]和生物累积性[3], 且对人体神经系统、 肾脏、 心血管系统、 造血系统都有重要影响[4], 对人体健康及水生态环境构成严重威胁。 实现水体重金属Pb的现场快速检测对防治水体重金属污染、 保障生态系统安全和人类健康具有十分重要的现实意义。
紫外-可见分光光度法(UV)[5]、 原子吸收光谱法(AAS)[6]、 原子荧光光谱法(AFS)[7]、 电感耦合等离子-质谱法(ICP-MS)[8]等传统水体重金属检测方法虽然能够实现水体重金属的准确与高灵敏检测[9], 但是通常需要现场采样再进行实验室分析, 并且需要复杂的前处理过程, 难以实现水体重金属污染的现场快速检测。 X射线荧光(XRF)光谱法具有对待测样品无破坏性[10]、 检测速度快[11]、 仪器简单[12]、 操作方便[13]等特点, 已成为重金属现场快速检测的重要手段。 XRF光谱法直接对水体重金属检测时, 高能X射线直接照射液体样品会使样品因局部受热而产生气泡、 沉淀等现象, 易产生较高的X射线散射背景, 从而影响XRF光谱法的灵敏性及测量精度[14]。 且在XRF光谱分析过程中, 当重金属Pb与类金属As同时存在时, Pb元素的最优选特征峰Lα 特征峰与As的最优选特征峰Kα 特征峰因能量极为接近而会相互重叠, 因此水体中As的共存会对Pb的XRF光谱测量与分析产生干扰与影响。
由于微藻具有容易获取与培养、 体积小、 比表面积大、 绿色环保等特点, 且对重金属具有良好的吸附特性[15], 在水体重金属污染治理与修复方面具有良好的应用[16, 17]。 因此针对上述问题, 本研究选取蛋白核小球藻为吸附剂, 探究其对水体重金属Pb的最佳吸附条件, 对比其对重金属Pb与As的吸附性能, 并建立了基于蛋白核小球藻富集-XRF光谱的水体重金属Pb快速检测方法, 将该方法应用于实际水样中重金属Pb的检测研究。 为发展水体重金属现场快速监测技术与仪器奠定了方法基础。
实验用藻为我国淡水中常见的微藻— — 蛋白核小球藻, 该藻种购于中国科学院水生生物研究所淡水藻种库, 实验前使用BG11培养基(青岛高科技工业园海博生物技术有限公司)对该藻种进行实验室扩大培养。 接种与培养所用培养基及相关器皿均需经过YM50A型立式压力蒸汽灭菌锅(上海三申)(121 ℃、 20 min)的高压灭菌处理, 接种过程于SW-CJ-1D型无菌工作台(苏州净化)中进行。 接种完成后将藻培养液置于HP00G型智能光照培养箱(武汉瑞华仪器)中进行培养, 培养条件为: 光暗时间比设置为12 h:12 h, 光照强度设置为6 600 lux, 温度设置为25 ℃。
采用抽滤方法去除蛋白核小球藻培养液中的培养基, 将抽滤后的藻细胞转移至去离子水中, 获取蛋白核小球藻悬浮液, 通过称量抽滤后滤膜上藻细胞的质量确定蛋白核小球藻悬浮液中藻细胞的质量浓度。
以分析纯硝酸铅[Pb(NO3)2](天津市津北精细化工有限公司)及分析纯亚砷酸钠(NaAsO2)(成都艾科达化学试剂有限公司)分别配制浓度为100 mg· L-1的重金属Pb与As的标准溶液。
取一定量蛋白核小球藻悬浮液于50 mL容量瓶中, 再加入一定体积浓度为100 mg· L-1的重金属Pb标准溶液, 用去离子水定容至50 mL, 将反应液转移至100 mL锥形瓶中, 并置于转速为100 r· min-1、 温度为25 ℃的MQD-B3G型叠加式光照振荡培养箱(上海旻泉)中进行吸附反应。 在反应时间为5 min时, 取10 mL反应液采用抽滤方式对重金属Pb进行富集, 所用的富集滤膜为混合纤维素脂膜(上海兴亚净化材料厂, 孔径0.22 μ m), 富集重金属区域直径为1.56 cm。
将抽滤后滤液转移至离心管中, 并以同样操作方式但不加入蛋白核小球藻悬浮液所配置的重金属Pb溶液为空白对照样。 采用iCAPRQ型电感耦合等离子体-质谱仪(Thermo Fisher Scientific, 美国)测量经蛋白核小球藻吸附后滤液中剩余的Pb2+浓度及未经藻细胞吸附的空白样品中Pb2+浓度, 并根据式(1)计算藻细胞对重金属Pb2+的吸附效率P(%)
$P(\%)=\frac{c_{0}-c}{c_{0}} \times 100$(1)
式(1)中: c0为反应液中未经藻细胞吸附的初始Pb浓度(即空白样品中Pb浓度), 单位为mg· L-1; c为经过藻细胞吸附后滤液中剩余的Pb浓度, 单位为mg· L-1; P为藻细胞对重金属Pb的吸附效率, 单位为%。
将富集后获得的薄膜样品自然风干后, 采用能量色散XRF光谱分析仪进行XRF光谱测量, 能量色散XRF光谱分析仪的激发源为Amptek公司Mini-X射线管, 靶材为Ag靶, X射线管前端安装有黄铜准直器和20 mil的Al原级滤波片, 探测器为Amptek公司的硅漂移探测器(SDD)。 XRF光谱测量时相关仪器参数设置为: X射线管激发电压为40 kV, 激发电流为20 μ A; 探测器信号累积时间(Accumulation Time)为120 s, 脉冲整形峰值时间为6.4 μ s, 脉冲整形宽度为0.8 μ s, 增益为47.47; 采用含有Fe元素和Mn元素的316不锈钢金属板块对仪器的通道数和能量值进行校准, 所测的XRF光谱通道范围为1~4 096, 对应能量范围为0~27.20 keV; 测量过程中通过改变富集样品激发点位, 对每个富集样品重复测量四次, 取能量值为10.3~10.8 keV之间Pb元素的Lα 特征谱峰进行分析。
为了实现水体重金属Pb的快速高效富集, 分别研究了反应液pH值、 反应温度对蛋白核小球藻吸附重金属Pb性能的影响, 以此筛选出水体重金属Pb高效富集的最佳吸附条件, 在此基础上验证水体重金属Pb高效富集的最佳浓度范围。
2.1.1 pH值对蛋白核小球藻吸附Pb性能的影响
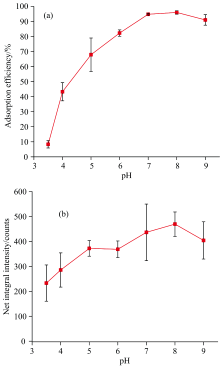
pH值是影响物质间结合性能的重要影响因素, 为获取蛋白核小球藻对水体重金属Pb高效富集的最佳pH值, 以0.1 mol· L-1硝酸溶液和0.1 mol· L-1氢氧化钠溶液对蛋白核小球藻与重金属Pb反应液的pH值进行调节, 以研究反应液pH值对蛋白核小球藻吸附重金属Pb性能的影响。 当反应液pH值分别为3.5、 4、 5、 6、 7、 8、 9, 且在转速为100 r· min-1、 温度为25 ℃的培养箱中进行吸附反应5 min后, 100 mg· L-1蛋白核小球藻对5 mg· L-1重金属Pb的吸附效率如图1(a)所示, 相应富集样品经XRF光谱测量后在10.3~10.8 keV能量范围内Pb元素Lα 特征谱峰的净积分荧光强度如图1(b)所示。
由图1(a)可以看出, 当反应液的pH值为3.5时, 蛋白核小球藻对重金属Pb的吸附效果较差, 平均吸附效率仅为8.34%; 当反应液的pH值由3.5增加到8时, 蛋白核小球藻对重金属Pb的吸附效率逐渐增大, 在pH值增加到7~8时, 吸附效率已高达95%及以上, 此时蛋白核小球藻对重金属Pb的吸附效果最好; 当反应液的pH值由8继续增加到9时, 蛋白核小球藻对重金属Pb的吸附效率反而有所降低。 由图1(b)可以看出, 富集有重金属Pb的薄膜样品Pb元素Lα 特征谱峰的净积分荧光强度随pH的变化规律与图1(a)中Pb吸附效率随pH的变化规律近似一致, 即当pH值为7~8时, Pb元素Lα 特征谱峰净积分荧光强度达到较高值。
由此可见, pH值对蛋白核小球藻吸附重金属Pb的性能有重要影响。 当反应液的pH值为7~8时, 蛋白核小球藻对重金属Pb具有最好的吸附效果且获得的富集薄膜样品中重金属Pb同样具有较高的特征谱峰强度。 因此为了避免水体重金属Pb因碱性环境易形成沉淀析出而影响实验结果的稳定性, 本研究确定蛋白核小球藻与重金属Pb反应液的最佳pH值为7。
2.1.2 反应温度对蛋白核小球藻吸附Pb性能的影响
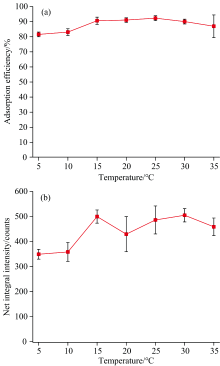
温度是影响物质间吸附性能的关键环境因子。 为了明确当反应环境的温度发生变化时, 蛋白核小球藻对重金属Pb的吸附性能是否会受到影响, 本研究将pH值为7的100 mg· L-1蛋白核小球藻与5 mg· L-1重金属Pb的反应液分别置于转速为100 r· min-1、 温度分别为5、 10、 15、 20、 25、 30、 35 ℃的培养箱中进行吸附反应, 在反应时间为5 min时, 不同反应温度下蛋白核小球藻对重金属Pb的吸附效率如图2(a)所示, 相应的富集样品XRF光谱中在10.3~10.8 keV能量范围内的谱峰净积分荧光强度如图2(b)所示。
由图2(a)可以看出, 当反应体系的温度为5 ℃时, 蛋白核小球藻对重金属Pb的吸附效果相对较差, 平均吸附效率为81.54%; 当温度由5 ℃增加到15 ℃时, 蛋白核小球藻对重金属Pb的吸附效率有所增加, 且当温度达到15 ℃时, 吸附效率已达到90%以上; 当反应温度在15~25 ℃范围内时, 蛋白核小球藻对重金属Pb的吸附效率在较高值的情况下保持稳定; 当反应温度由25 ℃继续上升到35 ℃时, 蛋白核小球藻对重金属Pb的吸附效率则呈下降趋势。 由图2(b)可以看出, 富集有重金属Pb的薄膜样品Pb元素Lα 特征谱峰的积分荧光强度随温度的变化规律与Pb吸附效率随温度的变化规律较为接近, 即当温度为25~30 ℃时, Pb元素Lα 特征谱峰积分荧光强度达到较高值。
反应体系的温度对蛋白核小球藻对重金属Pb的吸附性能有一定影响, 当反应溶液的温度为15~25 ℃时, 蛋白核小球藻对重金属Pb具有最好的吸附效果且富集样品的XRF光谱中具有较高的Pb元素特征谱峰强度, 但由于蛋白核小球藻最佳的生长温度为25 ℃, 且根据之前研究结果[18]可知蛋白核小球藻活藻细胞对重金属Pb的吸附性能要优于灭活藻细胞, 因此为了避免温度变化对蛋白核小球藻细胞活性的影响, 确定25℃为蛋白核小球藻吸附重金属Pb的最佳反应温度。
2.1.3 最佳吸附条件的适用性验证
为了验证在上述最佳吸附条件下, 蛋白核小球藻是否对不同浓度重金属Pb均具有高效吸附性能, 本研究分析了在最佳吸附条件下蛋白核小球藻对不同浓度重金属Pb的吸附效率。 当反应体系pH值为7、 反应温度为25 ℃、 反应时间为5 min时, 100 mg· L-1蛋白核小球藻对反应液中浓度分别为0.007 2、 0.012 8、 0.030 0、 0.068 0、 0.091 3、 0.143 5、 0.229 1和0.353 5 mg· L-1重金属Pb的吸附效率如图3所示。
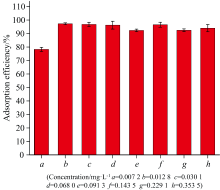 | 图3 蛋白核小球藻对不同浓度重金属Pb的吸附效率Fig.3 Adsorption efficiency of Chlorella pyrenoidosa to different concentrations of heavy metal Pb |
由图3可以看出, 当重金属Pb浓度为0.007 2 mg· L-1时, 蛋白核小球藻对其吸附效果相对较差, 平均吸附效率低于80%; 当重金属Pb浓度在0.012 8~0.353 5 mg· L-1时, 蛋白核小球藻对Pb都具有较好的吸附效果, 平均吸附效率均在92.33%~96.53%范围内。 由此可见, 蛋白核小球藻对水体中0.012 8~0.353 5 mg· L-1这一较宽浓度范围内的重金属Pb都具有极好的吸附效果, 而《地表水环境质量标准(GB3838— 2002)》中Ⅰ 类~Ⅴ 类水中重金属Pb的标准限值为0.01~0.1 mg· L-1, 因此蛋白核小球藻能够满足地表水中水体重金属Pb的高效富集要求。
在XRF光谱中, 重金属Pb的Lα 谱峰(能量值为10.55 keV)和As的Kα 谱峰(能量值为10.53 keV)分别是Pb元素和As元素特征谱峰中的最强峰, 因此在XRF光谱分析中, 重金属Pb的Lα 特征谱峰和As的Kα 特征谱峰均为Pb元素和As元素最为优选的特征峰, 但两者能量极为接近, 因此当水体中重金属Pb与As同时存在时, 则因两特征谱峰相互重叠从而影响重金属Pb元素定量分析的准确性。 为了探究当以蛋白核小球藻为吸附剂富集水体重金属Pb时, 蛋白核小球藻是否同样对类金属As也具有很好的吸附性能, 本研究在上述最佳反应条件下, 对比分析了蛋白核小球藻对重金属Pb与As的吸附性能。 当反应温度为25 ℃、 反应体系pH值为7、 反应时间为5 min时, 浓度为100 mg· L-1的蛋白核小球藻对不同浓度重金属Pb与As的吸附效率如图4(a)所示, 相应的富集样品XRF光谱中在10.3~10.8 keV能量范围内的谱峰净积分荧光强度如图4(b)所示。
由图4(a)可以看出, 当重金属Pb浓度与类金属As浓度较为接近时, 蛋白核小球藻对重金属Pb的吸附能力远远高于对类金属As的吸附能力, 例如当重金属Pb浓度在0.011 3~0.436 3 mg· L-1范围内时, 蛋白核小球藻对重金属Pb的吸附效率都高达92%以上, 而对于浓度相近的类金属As的吸附效率却均低于5%; 由图4(b)富集样品与空白滤膜在10.3~10.8 keV能量范围内XRF谱峰净积分荧光强度对比图可以看出, 经过蛋白核小球藻吸附后, 类金属As富集样品XRF谱峰净积分荧光强度与空白滤膜的XRF谱峰净积分荧光强度极为接近, 且并不随反应液中As初始浓度的增加而增大; 相比之下, 重金属Pb富集样品的XRF谱峰净积分荧光强度却明显大于相近浓度下类金属As富集样品的XRF谱峰净积分荧光强度, 并且随Pb初始浓度的增加而逐渐增大。 研究表明, 在蛋白核小球藻对重金属Pb的最佳吸附条件下, 其对类金属As的吸附能力较弱, 因此当水体中重金属Pb与As共存时, 通过蛋白核小球藻对重金属Pb的吸附作用, 可以实现水体中重金属Pb与As的有效分离及对重金属Pb的高效富集, 从而避免了在有As共存情况下, 其会对重金属Pb的XRF光谱定量分析产生干扰与影响。
在蛋白核小球藻富集重金属Pb的最佳吸附反应条件下, 当蛋白核小球藻与Pb反应液的富集量为10 mL、 富集区域直径为1.56 cm时, 分析了自然风干后富集样品在10.3~10.8 keV能量范围内XRF光谱的特征谱峰净积分荧光强度与反应液中重金属Pb初始浓度之间的定量关系, 结果的如图5所示。
 | 图5 Pb的Lα 特征谱峰净积分荧光强度与Pb浓度定量关系曲线Fig.5 Quantitative relationship curve between net integral fluorescence intensity of Lα characteristic peak of Pb and Pb concentration |
由图5可以看出, 当重金属Pb的初始浓度在0.012 8~0.353 5 mg· L-1范围内时, Pb的Lα 特征谱峰的净积分荧光强度与水体中Pb初始浓度之间具有非常好的线性关系, 线性方程为F=400.08+4 077.83c, (其中F为Pb的Lα 谱峰净积分荧光强度值, c为Pb浓度值, 单位为mg· L-1), 相关系数R2为0.990。 对初始浓度为0.012 8 mg· L-1的Pb标准溶液进行6次重复富集与XRF光谱测量, 富集样品中Pb元素Lα 特征谱峰净积分荧光强度的相对标准偏差为8.64%。 在相同条件下对未加入重金属Pb的混合纤维素脂滤膜所富集的藻细胞空白样品进行11次XRF光谱测量, 在Pb的Lα 特征谱峰处所对应的能量范围内11次测得的总积分荧光强度值的标准偏差为9.7617, 根据检测限(LOD)的计算公式LOD=3SD/k(SD为空白样品多次测量的标准偏差, k为校准曲线的斜率), 10 mL反应液富集量所对应的XRF光谱法的检测限为7.2 μ g· L-1, 低于《地表水环境质量标准(GB 3838— 2002)》中的I类水质标准限值0.01 mg· L-1, 因此该方法能够满足于各类地表水中重金属Pb的定量分析与检测。
为验证所建立的基于蛋白核小球藻富集-XRF光谱的水体重金属Pb这一快速检测方法是否适用于实际水样中重金属Pb的检测, 本研究采集了合肥市内派河、 匡河、 南淝河水、 四里河水及十五里河实际水样, 经过实验室前处理及ICP-MS检测, 测得水样中重金属Pb的浓度分别为0.005、 0.036、 0.027、 0.013和0.027 μ g· L-1。 采用标准加入法, 分别向实际水样中加入重金属Pb标准溶液, 使加入后实际水样中所加入的重金属Pb浓度为15、 25、 40和100 μ g· L-1。 通过标准加入后, 对实际水样在最佳反应条件下经5 min的蛋白核小球藻吸附后, 对富集样品进行XRF光谱测量, 并根据原水样中重金属Pb的浓度及所加入的重金属Pb的标准浓度值, 计算重金属Pb的回收率, 结果如表1所示。 研究表明采用所建立的检测方法, 对实际水样中重金属Pb测量的回收率均在87.84%~115.66%范围内, 说明本方法对实际水样重金属Pb的检测具有很好的适用性, 能够应用于实际水体重金属Pb的定量分析与检测。
| 表1 实际水样重金属Pb的XRF测量结果 Table 1 XRF measurement results of heavy metal Pb in actual water samples |
蛋白核小球藻作为一种环保型生物吸附材料, 对水体重金属Pb具有良好吸附效果, 在反应体系pH值为7且反应温度为25 ℃时, 5 min蛋白核小球藻对0.012 8~0.353 5 mg· L-1这一较宽浓度范围内重金属Pb的吸附效率就高达92%以上, 但对类金属As的吸附性能较差, 因此蛋白核小球藻对水体重金属Pb的富集有效避免了水体共存类金属As对Pb元素XRF光谱定量分析的干扰与影响。 在最佳吸附反应条件下, 建立了基于蛋白核小球藻富集-XRF光谱的水体重金属Pb定量检测方法, 当样品富集量为10 mL时, 该方法的检测限为7.2 μ g· L-1, 低于《地表水环境质量标准(GB 3838— 2002)》中的Ⅰ 类水质标准限值0.01 mg· L-1, 能够满足于各类地表水中重金属Pb的定量分析与检测。 将本方法采用标准加入法对合肥市不同河流的实际水样中重金属Pb进行检测, 回收率均在87.84%~115.66%范围内, 验证了所建立的基于藻富集-XRF光谱法的这一水体重金属Pb快速检测方法能很好地适用于实际水体中重金属Pb的现场快速检测。 为发展水体重金属污染物现场快速监测技术与仪器奠定了方法基础。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|