作者简介: 王一如, 女, 1983年生, 徐州工程学院物理与新能源学院实验师 e-mail: wangyiru2022@yeah.net
亲脂性偶氮染料苏丹红Ⅲ(Sudan Red Ⅲ)分子因染色后可使食品鲜艳、 不褪色, 常被放入食品添加剂中, 食用后对人体的肝肾器官有明显的毒性作用, 严重影响人类身体健康。 苏丹红分子的毒性与其分子几何和电子结构密切相关, 对其结构、 电子激发等研究具有重要的指导意义。 采用密度泛函理论(DFT)方法结合def2-TZVP基组对苏丹红Ⅲ分子结构、 红外与拉曼光谱和紫外光谱进行系统研究, 结果表明PBE0和B3LYP杂化泛函方法计算的红外和拉曼光谱与实验值吻合; 采用含时的B3LYP杂化泛函计算得到的苏丹红Ⅲ分子的紫外-可见吸收峰为228、 353和490 nm, 与实验符合较好, 它们是基态电子向第2激发态、 第6激发态、 第30激发态跃迁所致。 采用空穴—电子分析法考察电子激发可知, S0→ S2激发类型是氧、 氮原子到萘环和苯环上的 n—π*电荷转移激发, 同时伴随着萘环、 苯环环内间的π—π*局域激发。 S0→ S6激发类型是氮、 氧原子到萘环, 氮原子到苯环上的n—π*和萘环环内间π—π*电荷转移激发的叠加。 S0→ S2和 S0→ S6激发类型属于电荷转移激发为主的混合激发。 S0→ S30激发类型属于萘环环内的π—π*局域激发, 同时也伴随着氧、 氮原子到萘环上的 n—π*和苯环到萘环上的π—π*电荷转移激发, S0→ S30激发类型是以局域激发为主。 通过分子片段对空穴、 电子的贡献热图分析, 进一步证实了上述电子激发转移过程。 系统研究苏丹红Ⅲ分子的光谱及电子激发, 为实验检测食品苏丹红Ⅲ分子提供理论参考。
The lipophilic azo dye Sudan Red Ⅲ molecule enhances flavor or makes food bright and attractive. After eating, it has noticeable toxic effects on the liver and kidney organs of the human body and seriously affects human health. The toxicity of Sudan red molecule is closely related to its molecular geometry and electronic structure, which has important guiding significance for studying its structure and electronic excitation. In this work, we aimed to systematically investigate the molecular structure, infrared and Raman spectra, and ultraviolet spectra of Sudan Red Ⅲ by using the density functional theory (DFT) method in conjunction with the def2-TZVP basis set. The excitation properties of Sudan Red Ⅲ were also studied in detail by the hole-electron analysis method. The results show that the infrared and Raman spectra calculated for Sudan Red Ⅲ using the PBE0 and B3LYP exchange-correlation functional agree with the experimental data. Using the time-dependent B3LYP (TD-B3LYP) method with the def2-TZVP basis set, The UV-visible absorption peaks of Sudan Red Ⅲ show 228, 353, and 490 nm, which are in good agreement with the experiments. It can be found that they are through the transition of the ground state electrons to the second excited state, the sixth excited state, and the 30th excited state. The electron excitation characteristics are studied by using hole-electron analysis. It can be found that S0→ S2 is attributed to the superposition of the n—π* charge-transfer excitation in the direction from oxygen and nitrogen atoms to the naphthalene and benzene ring, and the π—π* local excitation between intra-ring naphthalene and benzene rings. The superposition of the n—π* charge-transfer excitation from oxygen and nitrogen atoms to naphthalene and benzene ring and the π—π* local excitation between intra-ring naphthalene and benzene rings are excited by S0→ S6. The electronic transition of S0→ S2 and S0→ S6 from the ground state to the excited state belongs charge transfer excitation, where the charge transfer excitation effect is dominant. S0→ S30 is attributed to the superposition of local excitation and charge-transfer excitation, where the local excitation effect is dominant. They contributed π—π* local excitation between intra-ring naphthalene rings, and the superposition of n—π* in the direction from oxygen and nitrogen atoms to naphthalene and benzene ring and π—π* charge-transfer excitation between intra-ring naphthalene rings. Furthermore, we draw heatmaps of the contribution of molecular fragments to holes and electrons. The electron mentioned above excitation transfer was further confirmed by heat map analysis. The spectrum and electron excitation of Sudan Red Ⅲ were investigated systematically, which can provide a theoretical reference for experimental detection of Sudan Red Ⅲ in food.
苏丹红(Sudan)分子作为化学工业染色剂, 广泛应用于油彩、 机油、 蜡和鞋油等产品的染色, 以促使鞋、 地板等增光, 受到人们的青睐。 苏丹红主要包括Ⅰ 、 Ⅱ 、 Ⅲ 和Ⅳ 四种类型, 属于亲脂性偶氮染料。 这种偶氮类化合物在人体内经历活化过程后, 通过生物转化形成芳香胺化合物, 对人体的肝肾器官有明显的毒性作用, 被国际癌症研究机构(International Agency for Researchon Cancer, IARC)确定为致癌物[1, 2, 3, 4, 5]。 另外, 亲脂性偶氮染料苏丹红也可直接被酶氧化[6, 7], 其产物可导致DNA损伤[8, 9]。 实验发现苏丹红分子的致癌活性与其分子几何和电子结构有关, 尤其是化学键分布、 电荷分布[10]等。
值得关注的是, 由于苏丹红Ⅲ 分子对食品染色后可使食品鲜艳、 不褪色, 从而增添人们的食欲、 提高其食用价值, 一些企业违规使用苏丹红Ⅲ 分子, 将其放入食品(如红色豆腐乳[11]、 辣椒粉[12]、 调味酱[13]、 辣条[14]、 辣椒油[15]、 红心家禽蛋[16]、 花椒粉[17]等)添加剂中, 严重影响人类身体健康。 因此, 世界各国开展对苏丹红进行检查。 目前有大量报道苏丹红Ⅲ 分子的检测方法, 例如高效液相色谱法[18]、 高效液相色谱-质谱法联用[19]、 紫外-可见分光光度法[20]、 电化学法[21]等。 显然, 这些检测方法均与分子结构及其物性有密切关系。 因此, 从原子分子层次上, 充分理解苏丹红Ⅲ 分子的几何结构及电子结构本质不仅具有物理意义, 而且更具有商业价值。
目前应用广泛、 效果较好且可靠的分析和检测物质结构及其物性的手段仍然是光谱学方法[22, 23]。 其中红外光谱常用于分子的立体构型鉴定和分子的化学组成进行分析[24]。 由于拉曼位移的大小与入射光的频率无关, 入射光与分子振动能级的能量交换, 可直接测量分子振动能级与转动能级结构, 拉曼光谱常作为红外光谱的重要补充[25]。 紫外光谱是分子中电子受激跃迁产生的, 因此, 紫外吸收谱用于分子的电子结构分析和鉴定[26]。 研究表明, 密度泛函理论(density functional theory, DFT)是一种研究多电子体系电子结构的量子力学方法, 能较好地预测、 分析分子的红外与拉曼光谱、 分子激发能等。 如计算分子的红外与拉曼光谱[27]、 紫外-可见吸收光谱[28]与实验值吻合较好。
以往的实验和理论研究报道了苏丹红Ⅲ 分子的红外与拉曼光谱、 紫外光谱[25, 29]。 例如, Kunov-Kruse等实验和理论分析了苏丹红Ⅲ 的分子结构、 红外与拉曼光谱[30]。 陈晨等利用拉曼光谱法研究了苏丹红Ⅲ 分子拉曼光谱[25]。 张金平[31]等研究了有机溶液中苏丹红Ⅲ 分子的紫外-可见光谱, 结果表明在极性溶剂中苏丹红Ⅲ 分子的可见区特征吸收峰比在非极性溶液中略有红移。 尽管以往对苏丹红Ⅲ 分子的性质探究已经取得了重大进展, 但有关苏丹红Ⅲ 分子的电子激发性质及电荷转移过程还未见相关报道, 基于苏丹红Ⅲ 分子的精确光谱仍有待完善。 本工作采用密度泛函理论(DFT)方法对苏丹红Ⅲ 分子结构、 分子轨道、 红外与拉曼光谱和紫外光谱进行系统研究, 并采用空穴-电子分析法详细研究苏丹红Ⅲ 分子的激发性质, 分析电子激发过程及其分子性质以阐明染料发光产生机理, 为苏丹红Ⅲ 分子研究提供分子层面的解析, 亦可丰富有机分子光谱数据库, 甚至为实验检测食品苏丹红Ⅲ 分子提供理论参考以保障食品安全。
当光与物质相互作用时, 物质中价电子吸收光子能量而发生能级跃迁, 价电子由基态跃迁到激发态。 因此, 分子发光机理的基本特征可认为是由电子激发引起, 它的吸收光谱
可反映出电子跃迁的难易程度和概率。 空穴-电子分析法可以较好地研究电子的激发特征[32, 33, 34]。 空穴-电子激发性质可以通过分析波函数, 计算出空穴和电子的质心距离D、 重叠程度Sr、 总体平均分布广度H、 分离程度t等参数来描述。 具体表达式如式(1)— 式(4)
式(1)中, Dx=|Xele-Xhole|, Dy=|Yele-Yhole|, Dz=|Zele-Zhole|, X, Y, Z为空穴和电子质心的笛卡尔坐标。 式(2)中, ρ 为空穴(电子)密度, Sr的值域为[0, 1], 表征空穴和电子重叠程度。 式(3)中, σ 为空穴(电子)在x, y, z方向上分布的方均根偏差。 式(4)中, HCT是衡量在电荷转移激发(charge transfer excitation, CT)方向上空穴和电子的平均延展程度, 式中t> 0表示空穴和电子分离程度大。
通过式(1)— 式(4)中的参数可以定性表征分子激发特征, 从而确定电子激发跃迁及其转移过程。 采用PBE纯泛函、 PBE0和B3LYP杂化泛函方法联合def2-TZVP基组, 计算优化苏丹红Ⅲ 分子的基态结构。 基于基态结构, 分析了其分子轨道、 红外与拉曼光谱、 紫外光谱性质。 此外, 采用B3LYP杂化泛函方法联合def2-TZVP基组研究电子光谱与激发、 电荷转移等性质。 所有计算收敛指标为默认值, 相邻两次迭代的均方根密度矩阵元差值小于10-8, 迭代次数为128, 最大的相邻两次迭代的密度矩阵元绝对差值小于10-6, 相邻两次迭代的体系能量绝对差值小于10-6 Hartree。 全部计算在Gaussian09, E.01软件包进行[35], 分子轨道、 紫外光谱、 激发态性质、 电荷转移等等分析均在Multiwfn软件[36]下完成。
优化后得到单重态苏丹红Ⅲ 基态分子振动无虚频, 其结构如图1所示。 它们的主要键长、 键角和二面角列入表1中。 从表1中的数据可知, PBE纯泛函、 PBE0杂化泛函和B3LYP
杂化泛函计算得到的键长、 键角各有差异, 这意味着计算的键长、 键角与交换关联函数中的Hartree-Fock交换(HFX)的组成密切相关。 尽管它们有一定的差异, 但不同泛函优化的结果同实验值基本符合[37]。
| 表1 不同方法联合def2-TZVP基组优化后苏丹红Ⅲ 分子主要键长、 键角 Table1 The partially optimized bond lengths and bond angles of Sudan Red Ⅲ by different methods with def2-TZVP basis set |
采用B3LYP/def2-TZVP方法和基组计算苏丹红Ⅲ 分子能级轨道、 能隙Eg和态密度。 结果表明, 最高占据轨道(HOMO)和最低未占据轨道(LUMO)能量分别为-6.058(记EH)和-2.974(记EL)eV, 能隙Eg(Eg=EL-EH)为3.084 eV。 计算的苏丹红Ⅲ 分子电子激发波长处于紫外波段。
体系的分子轨道能级可以通过态密度直观显现出来, 苏丹红Ⅲ 分子的态密度(density of states, DOS)和局部态密度(partial DOS, PDOS)如图2所示。 图2中下方竖线为分子轨道能级位置, DOS采用Gaussian函数展宽, 半高全宽(FWHM)值取0.02 a.u.。 从图2(a)中可清晰看出, 对于低能量区-0.8~-0.6 a.u.附近的轨道, 它们主要由苯环、 萘环上H的s轨道和C的px、 py轨道杂化为σ 成键轨道。 图2(b)轨道等值面图(能级为-0.668 a.u.)证实了H的s轨道和C的p轨道杂化形成的σ 成键轨道。 能量为-0.4 a.u.附近的轨道, H、 C和N的PDOS几乎相当, 主要由H的s轨道, C和N的p轨道混合产生, 同时伴随着O的p轨道(孤对电子占据)贡献。 这意味着H与C的轨道相互作用形成了σ 成键轨道; C和N的px、 py轨道相互作用形成σ 成键轨道; C和N的pz轨道相互作用形成π 成键轨道。 图2(c)中σ 成键轨道(能量为-0.403 a.u.)和图2(d)中π 成键轨道验证了这一结论。 特别地, 能量在-0.248 a.u.附近的轨道, 即HOMO+1轨道, N的PDOS在整个PDOS峰中最高, 与C片段的PDOS接近, 说明HOMO+1轨道主要由N的孤对p电子, 及C和N的px、 py轨道共同构成σ 成键轨道共同贡献。 图2(e)明显看出是N的孤对p电子轨道以及σ 成键轨道。 在HOMO轨道位置, 能级为-0.223 a.u., 主要由C的PDOS构成, 伴随着微弱的N的PDOS, O的轨道几乎不参与。 图2(f)看出, HOMO轨道明显为是由C环pz轨道构成的π 成键轨道。 对于非占据轨道区域, 能量为-0.109 a.u.的LUMO轨道, N的PDOS与C的PDOS非常接近, 表明C和N的pz轨道共同构成了π 反键轨道[图2(g)]。
在def2-TZVP基组下, 采用PBE纯泛函、 PBE0杂化泛函和B3LYP杂化泛函方法, 计算了苏丹红Ⅲ 分子的红外光谱和拉曼光谱, 结果如图3、 图4所示。 红外光谱和拉曼光谱吸收峰列于表2中。 图3、 图4可清晰的看到, 相同的基组下, PBE0和B3LYP杂化泛函方法计算的吸收峰非常相似, PBE纯泛函与它们略有差异。 从表2和图3可知, 两种杂化泛函计算的红外和拉曼光谱均与实验值[37]符合较好。 这意味着PBE0和B3LYP杂化泛函方法能更准确、 更合理的描述苏丹红Ⅲ 分子的红外光谱和拉曼光谱。 如B3LYP杂化泛函计算得到的苏丹红Ⅲ 分子吸收峰位于1 308 cm-1处, 实验观察到的红外吸收峰为1 304 cm-1, 拉曼散射峰为1 307 cm-1 [37]。
| 表2 苏丹红Ⅲ 分子实验与理论计算红外与拉曼谱峰 Table 2 The experimental vs. theoretical calculated FTIR and Raman peaks of Sudan Red Ⅲ |
采用含时密度泛函理论方法(TD-DFT, PBE、 PBE0、 B3LYP)计算了苏丹红Ⅲ 分子的紫外-可见吸收光谱, 如图5所示。 图中可知, 纯泛函PBE计算结果与PBE0、 B3LYP杂化泛函计算结果差异明显, 这是由于纯泛函没有HF部分, 激发能明显偏低, 导致波谱向长波方向移动, 杂化泛函考虑了电子相关, PBE0和B3LYP中HF成份分别为25%和20%, 它们的紫外-可见吸收光谱特征非常相似。
实验发现苏丹红Ⅲ 分子的紫外-可见吸收谱在223 nm(紫外光区)、 351 nm(紫外光区)、 500 nm(可见光区)附近有明显吸收峰[29, 38]。 采用PBE0和B3LYP杂化泛函计算得到的苏丹红Ⅲ 分子紫外-可见吸收峰为220/228、 338/353和470/490 nm(图5)。 杂化泛函计算的紫外可见光谱与实验符合较好(B3LYP杂化泛函同实验符合程度更高)。 计算结果再次表明PBE0和B3LYP杂化泛函能准确的描述苏丹红Ⅲ 分子的性质。
计算得到与实验观察相符的吸收峰列于表3中, 它们对应的激发态、 跃迁波长、 振子强度、 跃迁轨道贡献率、 激发能也分别列于表3中。 从表3可知, 实验观察到的吸收峰为基态电子向第2激发态、 第6激发态、 第30激发态跃迁所致。 由于基态电子向第5激发态、 第46激发态跃迁波长与实验值相近, 也将它们列入表3。 从表中可知基态到第2激发态, 是电子从第92号分子轨道(HOMO)向第93号分子轨道(LUMO)激发跃迁起主导, 其跃迁贡献率为99.25%。 基态电子向第5、 6、 30、 46激发态跃迁中均由多条分子轨道共同完成, 并无某单一的分子轨道主导。 例如, 基态电子向第5激发态跃迁中, 第88号轨道向第93号轨道跃迁的贡献率为63.74%, 第92号轨道向第94号轨道的贡献率为22.61%。 第90号轨道向第93号轨道跃迁的贡献率仅为1.68%。 这表明除基态向第2激发态中的电子跃迁可认为几乎由HOMO分子轨道向LUMO分子轨道跃迁之外, 其他基态向激发态电子激发性质并不能用单一的分子轨道跃迁进行描述, 这意味着采用分子轨道跃迁分析电子跃迁不能更好的诠释电子激发特性。
| 表3 苏丹红Ⅲ 分子的电子激发分析表 Table 3 The analysis chart of electron excitation of Sudan Red Ⅲ |
空穴-电子分析法[36, 39]可以全面考察电子激发特征, 通过式(1)— 式(4)式计算出基态向第2、 5、 6、 30、 46激发态的D, Sr, H, t参数数值列于表4。 还绘制了空穴-电子图(hole-electron)、 空穴-电子质心分布图(Chole-Cele图)[17]以及Sr函数图(图6), 绘制均采用0.001等值面。 空穴-电子图和空穴-电子质心分布图中绿色和蓝色分别表示电子和空穴分布。 为了方便分析, 将表3中的轨道能级图绘制于图7中。
| 表4 苏丹红Ⅲ 分子的激发态参数 Table 4 Excited state parameters of Sudan Red Ⅲ |
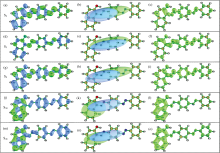 | 图6 苏丹红Ⅲ 分子的空穴-电子、 Chole-Cele、 Sr示意图Fig.6 Electron-hole, Chole-Cele, and Sr distributions of Sudan Red Ⅲ |
从表4可知, S0→ S2、 S0→ S6、 S0→ S30、 S0→ S46激发中, 它们的空穴和电子的质心距离D值均大于C— C键、 N— N键、 C— N键等的核间距, 说明空穴和电子质心距离较远。 Sr数值高, 空穴和电子分布特征超过一半的重合[图6(b)、 (h)、 (k)、 (n)]。 t的数值均小于0, 空穴和电子分布有没有显著分离。 电子与空穴的总体平均分布广度较大, 电荷转移激发(CT)方向上空穴和电子的平均延展程度广。 结合表4中各参数、 分子轨道图[图6(a)— (h)]、 Chole-Cele图[图6(h)、 (k)、 (n)]可知, S0→ S2、 S0→ S6激发类型归属于电荷转移激发, 同时伴随着局域激发。 而S0→ S30、 S0→ S46激发类型归属于局域激发, 同时伴随着电荷转移激发。
根据空穴-电子图[图6(a)]和分子轨道图[图7(a)— (h)]可知, S0→ S2激发中, 空穴主要由萘环、 a苯环(图1)上的π * 轨道和氮(N3、 N5)原子、 氧原子的孤对电子轨道构成[图7(c)]。 电子分布主要由氮(N2、 N3、 N4、 N5)原子的孤对电子轨道构成[(图7(c)], 同时有少量氧原子的孤对电子轨道和萘环以及a苯环上π 轨道构成[图6(a)]。 空穴和电子分布在萘环、 a苯环上, 环内空穴和电子在空间上既有重叠也有分离[图6(a), (c)], 暗示着环内间存在电荷转移。 由上述可知S0→ S2是氧、 氮原子到萘环和a苯环上的n— π * 电荷转移激发为主的激发类型, 同时伴随着萘环、 a苯环环内间的π — π * 局域激发。
S0→ S6激发中, 空穴主要由萘环、 少量a苯环和b苯环上的π 轨道、 氮(N3、 N5)原子以及氧原子的孤对电子轨道构成[图7(d), (e)]。 电子分布主要由氮(N2、 N3、 N4、 N5)原子以及氧原子上少量的孤对电子轨道和萘环、 a苯环、 b苯环(图1)上少量的π * 轨道构成[图7(a), (b), (c)]。 所以, S0→ S6激发类型是氮、 氧原子到萘环, 氮原子到a苯环上的n— π * 和萘环环内间π — π * 电荷转移激发的叠加, 该激发态应该属于电荷转移激发为主的类型。
S0→ S30和S0→ S46激发中, 空穴主要由萘环、 a苯环、 b苯环上的π 轨道和氮(N2、 N3、 N4、 N5)原子以及氧原子上少量的孤对电子轨道构成[图7(a), (b), (c)]。 电子分布主要由萘环上π * 轨道构成[图7(f), (g), (h)、 图6(j, m)]。 空穴和电子同时分布在萘环上, 环内空穴和电子在空间上既有重叠也有分离[图6(j, m)], 暗示着环内间存在电荷转移。 因此, S0→ S30和S0→ S46激发属于萘环环内的π — π * 局域激发。 另外, 空穴在苯环、 氮、 氧原子空间上也有分布, 所以S0→ S30和S0→ S46激发同时也伴随着氧、 氮原子到萘环上的n— π * 和a苯环、 b苯环到萘环上的π — π * 的电荷转移激发。
特别地, S0→ S5激发中, D为0.65 Å , 小于C— C键、 N— N键、 C— N键等的核间距, 说明空穴和电子质心距离较近。 Sr数值为0.78[图6(f)], 意味着空穴和电子的分布特征重合度高。 t的数值小于0(-1.85 Å ), 意味着空穴和电子分布无明显分离。 H和HCT指数分别为5.06和2.50 Å , 表明电子与空穴的总体平均分布广度较大, 电荷转移激发方向上空穴和电子的平均延展程度相比与S0→ S2激发中的小, 但延展度也较广。 由图6(b)和图7(c)可知S0→ S5激发类型为电荷转移激发为主。 根据空穴-电子图[图6(d)]可得, 空穴分布在萘环、 a苯环、 b苯环的π 轨道和氮(N2、 N3、 N4、 N5)原子、 氧原子的孤对电子轨道上。 电子分布也主要由萘环、 a苯环的π * 轨道、 氮(N2、 N3、 N4、 N5)原子、 氧原子的孤对电子轨道构成。 由上述可知S0→ S5激发类型是氧、 氮原子到萘环、 a苯环、 b苯环上的n— π * 和萘环π — π * 电荷转移激发的叠加。
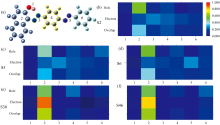
为了更进一步直观查看萘环、 苯环、 氮原子、 氧原子对空穴和电子激发的贡献, 本文将苏丹红Ⅲ 分子划分为6个片段, 如图8(a)所示。 羟基(O— H)为第1片段, 萘环为第2片段, N2、 N3原子连接部分为第3片段, 中间苯环(图1中a苯环)为第4片段, N4、 N5原子连接部分为第5片段, 最右边苯环(图1中b苯环)为第6片段。 并把基态向第2、 5、 6、 30、 46激发态对应片段对空穴、 电子和二者重叠的贡献的热图绘制于图8(b)— (f), 相应的片段对空穴和电子的贡献值列入表5中。 为了便于横向对比, 所有激发态的热图色彩刻度统一设为0.0~1.0。
| 表5 苏丹红Ⅲ 分子片段对空穴和电子的贡献 Table 5 Contribution of each fragment to hole and electron of Sudan Red Ⅲ |
如图8(b)所示, S0→ S2中被激发的电子主要来自片段2, 其空穴和电子重叠区域比较分散, 片段2处重叠程度相对其他片段最高。 从表5可知, 空穴主要集中于片段2(占比58.13%), 电子则分散在2、 3、 4、 5片段, 分别占比为20.10%、 25.44%、 22.18%、 19.02%。 比较空穴和电子的贡献, 激发前后片段2的电子贡献减小说明有失去电子的倾向, 由于片段2中的Diff.为-38.03%, 当前考察的是单电子激发, 因此片段2的电子在电子激发过程中减少了0.38个。 而片段3、 5电子的贡献变大则说明具有接受电子的倾向, 由片段3、 5的Diff.数据可知, 片段2这部分电子转移到片段3、 5的氮原子上。 另外, 在片段2空穴与电子重叠有34.18%的程度, 暗示着片段2中内存在电荷转移。 证实了上述S0→ S2激发过程不仅有片段间电荷转移过程, 还存在局域激发。
如图8(c)、 (d)所示, S0→ S5和S0→ S6被激发的电子同S0→ S2类似, 主要来自片段2, 其空穴和电子重叠区域比较分散, 从表5可知, 空穴主要集中在片段2, 电子则分散在2、 3、 4、 5片段。 S0→ S5中, 片段2空穴与电子重叠有31.57%。 由于片段2中的Diff.为-21.61%, 片段2的电子在电子激发过程中减少了0.22个, 由片段3的Diff.数据可知这些电子转移到片段3、 5的氮原子。 片段6的电子被激发转移到片段5中氮原子。 片段2处重叠程度相对其他片段最高, S0→ S5和S0→ S6重叠程度分别为31.57%, 35.14%。 从而验证了S0→ S5和S0→ S6激发过程是电荷转移为主, 同时存在局域激发混合激发类型。
对比图8(e)、 (f)可知, S0→ S30和S0→ S46激发状态类似。 它们被激发的电子是片段2的, 激发后电子大部分还是留在片段2, 而空穴和电子的重叠在片段2显著高于其他部分。 表明S0→ S30和S0→ S46激发过程以局域激发为主的激发类型。 此外, 从表5可知, S0→ S30中空穴主要集中在片段2、 4, 电子则集中在片段2, 片段2空穴与电子重叠有66.39%。 由于片段2中的Diff.为39.06%, 片段2的电子在电子激发过程中增加了0.390 6个, 主要由来自于片段4和片段6中电子激发转移得到。 S0→ S46空穴主要集中在片段2、 6, 电子则集中在片段2。 被激发的电子同样来自于片段4和片段6中。 这意味着S0→ S30和S0→ S46激发过程也存在明显的电荷转移激发。 进一步证实S0→ S30和S0→ S46过程以局域激发为主, 同时存在明显的电荷转移, 属于混合激发类型。
采用密度泛函理论(DFT)计算了苏丹红Ⅲ 分子的基态性质, 前线分子轨道、 红外和拉曼光谱、 紫外光谱与电子激发。 采用PBE纯泛函、 PBE0杂化泛函和B3LYP杂化泛函方法, 结合def2-TZVP基组计算了苏丹红Ⅲ 分子的红外光谱与拉曼光谱。 结果表明PBE0和B3LYP杂化泛函方法计算的红外和拉曼光谱与实验值符合较好; HOMO轨道主要由C原子片段的局部态密度(partial density of states, PDOS)构成, 伴随着微弱的N原子片段的PDOS, C原子环pz轨道间构成的π 成键轨道。 LUMO轨道中N片段的PDOS与C片段的PDOS非常接近, C原子和N原子的pz轨道共同构成的π 反键轨道。
采用含时的B3LYP杂化泛函计算得到的苏丹红Ⅲ 分子的紫外-可见吸收峰为228、 353、 490 nm, 与实验符合较好, 它们源于基态电子向第2激发态、 第6激发态、 第30激发态跃迁。 采用空穴-电子分析法考察电子激发可知, S0→ S2激发中, 空穴主要由萘环、 苯环中的π * 轨道和氮原子、 氧原子的孤对电子轨道构成。 电子分布主要由氮原子的孤对电子轨道构成, 同时有少量氧原子的孤对电子轨道和萘环以及a苯环上π 轨道构成。 S0→ S2是氧、 氮原子到萘环和苯环上的n— π * 电荷转移激发为主的激发类型, 同时伴随着萘环、 苯环环内间的π — π * 局域激发。 S0→ S6激发类型是氮、 氧原子到萘环, 氮原子到苯环中的n— π * 和萘环环内间π — π * 电荷转移激发的叠加。 该激发态应该属于电荷转移激发为主的类型。 S0→ S30和S0→ S46激发中, 空穴和电子同时分布在萘环上, 环内空穴和电子在空间上既有重叠也有分离, S0→ S30和S0→ S46激发属于萘环环内的π — π * 局域激发, 同时也伴随着氧、 氮原子到萘环中的n— π * 和a苯环、 b苯环到萘环中的π — π * 的电荷转移激发。 S0→ S5激发类型是氧、 氮原子到萘环、 苯环中的n— π * 和萘环π — π * 电荷转移激发的叠加。 通过分子片段对空穴、 电子的贡献热图分析, 进一步证实了上述电子激发转移过程。 本工作对苏丹红Ⅲ 分子的光谱及染料发光机理做了系统的研究, 可为苏丹红Ⅲ 分子研究提供分子层面的解析, 为实验检测食品苏丹红Ⅲ 分子提供理论参考以保障食品安全。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|