作者简介: 刘玉莹,女, 1997年生,新疆大学资源与环境科学学院硕士研究生 e-mail: 610473420@qq.com
向日葵作为我国主要的油料作物之一, 其秸秆是天然的纤维素材料, 具有绿色无毒, 成本低廉的优势, 是制备生物质碳量子点的理想材料之一。 近年来, 由于含铜农药和化学肥料的不规范使用, 大量含铜污染物被排放导致农田土壤和水环境中的铜含量远高于环境背景值。 因此, 迫切需要开发出一种选择性好、 灵敏性强且对环境友好的Cu2+检测方法。 碳量子点(CDs)是一种粒径小于10 nm的准球形荧光碳纳米材料, 因其表面含有丰富的极性官能团, 具有良好的水溶性而被广泛研究。 与传统的半导体量子点(CdSe, CdTe)相比, CDs具有合成原料广泛、 生物相容性好等优点。 主要应用于生物成像、 光催化、 光电转化以及传感检测等领域。 然而目前用于碳化合成CDs的前驱体大多为昂贵的化学品, 且合成过程复杂污染环境, 限制了CDs的大规模生产与应用。 开发出一种生态友好, 简单、 廉价的CDs合成方法是很有意义的。 本研究以废弃的向日葵秸秆为碳源, 采用简便的水热法合成生物质碳量子点(S-CDs)作为荧光探针, 用于检测识别Cu2+。 通过对S-CDs的一系列光学性质分析与表征, 鉴定出其表面官能团主要包括O—H, N—H以及等, 其中丰富的O—H可以提供胶体稳定性, 有效地控制纳米颗粒的形态和粒径分布, 从而提高S-CDs的量子产率(QYs)。 ex=317 nm, em=456 nm, S-CDs在pH为2.0~12.0的范围内具有优异的光学性能和良好的光稳定性, 受高盐度环境的影响较小, QYs约为8.42%, 在365 nm的紫外分析仪照射下发射出蓝色荧光。 此外, 以合成的S-CDs作为荧光探针, 进一步研究了基于Cu2+诱导S-CDs的荧光猝灭效应。 结果表明, 制备的S-CDs在0~10 μmol·L-1浓度范围内对Cu2+反应灵敏, 呈良好的线性关系( R2=0.971 4), 检出限(LOD)低至167 nmol·L-1。 在实际应用中, 湖水中的Cu2+检测回收率在96.18%~109.22%。 该研究在资源化利用秸秆废弃物的基础上, 介绍了一种基于荧光碳量子点的Cu2+检测方法。
Sunflower is one of the main oil crops in China. Its straw is a natural cellulose material, which has the advantages of being green, non-toxic and low cost, and it is an ideal material for synthesising biomass carbon quantum dots. In recent years, due to the abuse of copper-containing pesticides and chemical fertilizers, many copper-containing pollutants have been discharged, resulting in the copper content in farmland soil and water environment being much higher than the environmental background value. Therefore, it is urgent to develop a Cu2+ detection method with good selectivity, high sensitivity and environmental friendly. Carbon quantum dots (CDs) are quasi-spherical fluorescent carbon nanomaterials with particle sizes less than 10 nm. Its surface contains abundant polar functional groups and has been widely studied for its good water solubility. Compared with traditional semiconductor quantum dots (CdSe, CdTe), CDs have extensive synthetic materials and good biocompatibility advantages. They are mainly used in biological imaging, photo catalysis, photoelectric conversion, sensor detection and other fields. However, most of the precursors of carbonized CDs synthesis are expensive chemicals, which have the disadvantages of a complex synthesis processes and environmental pollution, limiting the large-scale production and application of CDs. Therefore, developing an eco-friendly, simple and inexpensive CDs synthesis method is of great significance. In this study, waste sunflower straw was used as a carbon source, and a simple hydrothermal method was used to synthesize biomass carbon quantum dots (S-CDs) as fluorescent probes to detect Cu2+. Through a series of optical properties analysis and characterization of S-CDs, the surface functional groups of S-CDs mainly include O—H, N—H and among which abundant O—H can provide colloid stability, effectively control the morphology and particle size distribution of nanoparticles, thus improving the quantum yield (QYs) of S-CDs. ex=317 nm, em=456 nm, S-CDs have excellent optical performance and good optical stability in the pH range of 2.0~12.0, less affected by high salinity environment, QYs is about 8.42%, emitting blue fluorescence under UV analyzer irradiation at 365 nm. In addition, the fluorescence quenching effect of S-CDs induced by Cu2+ was further studied using the synthesized S-CDs as a fluorescence probes. The results showed that the prepared S-CDs were sensitive to Cu2+ in the concentration range of 0~10 μmol·L-1 with a good linear relationship ( R2=0.971 4), and the detection limit (LOD) was as low as 167 nmol·L-1. In practice, the detection recoveries of Cu2+ in lake water are 96.18%~109.22%. In this study, a Cu2+ detection method based on fluorescent carbon quantum dots was introduced based on resource utilization of straw waste.
引 言
荧光碳量子点(CDs)因其独特的光学性质和化学性质, 在金属离子传感[1]、 生物成像[2]、 生物传感[3]、 光催化[4]和药物传递[5]等领域得到了广泛研究。 合成CDs可采用“ 自上而下” 的方法, 如电化学氧化和激光烧灼[6], 以及“ 自下而上” 的方法, 如超声[7]、 微波[8]和热解[9]。 这些方法存在仪器复杂, 程序繁琐等缺点, 限制了CDs大规模的合成[10]。 与其他合成方法相比, 水热法在高温高压条件下一步合成CDs, 不需后续的加工处理, 具有操作简单, 合成效果好的优势, 一步实现了前驱体的碳化与功能化[11]。
近年来, 一些利用生态友好、 廉价可再生的生物质材料为碳源合成CDs的方法引起了研究人员的广泛关注[12]。 Zhao等[13]以稻壳生物质为前驱体, 首先采用超声法, 加入适量H2SO4对样品进行5 h超声处理, 再加入适量HNO3, 进一步超声10 h; 随后将过滤后的样品重新分散至去离子水中, 在200 ℃, 10 h的水热条件下得到QYs为9.2%的CDs。 Xu等[14]以厨余垃圾葡萄皮为绿色前驱体, 通过简单的水热法(180 ℃, 6 h)合成了QYs为3.1%的CDs。 然而, 目前以生物质为前驱体合成CDs的制备方法存在合成步骤复杂或QYs较低的问题, 限制了生物质碳量子点的实际应用。 因此, 探究如何采用简便方法制备出光学稳定性好, 量子产率高的生物质碳量子点很有必要。
铜对于植物和动物而言是一种重要的微量元素。 异常水平的Cu2+含量可导致生物体出现氧化应激反应, 影响水生动物生长发育, 危害人体健康[15], 因此Cu2+的选择性检测对环境和健康具有重要意义。 传统的荧光传感材料如机染料、 半导体量子点以及贵金属纳米团簇等已被广泛研究应用Cu2+的微量检测。 但因其毒性大、 成本高在环境中光学稳定性差等缺点, 严重限制了其实际应用。 CDs是一种新型荧光碳纳米材料, 在金属离子传感机制中, CDs的荧光性能可能会受到一些金属离子(如Cu2+, Fe3+, Cr6+, Hg2+等)的影响, 这种影响往往伴随着荧光强度的增强或衰弱, 利用CDs这一特性, 可达到快速检测金属离子的目的。
向日葵作为我国重要的农作物之一, 其秸秆是天然的纤维素材料, 廉价易得, 是一种理想的生物质材料。 本研究以废弃的向日葵秸秆为前驱体, 不需要添加昂贵的有机化学品或繁琐的加工过程, 使用马弗炉在250 ℃, 2 h的条件下高温加热秸秆粉末, 使其充分碳化, 并在此基础上以180 ℃, 6 h的水热条件制备出QYs为8.42%的S-CDs(图1)。 通过高温碳化结合水热法有效地提高了生物质碳量子点的QYs, 并发现制备的S-CDs对Cu2+在0~10 μ mol· L-1范围内具有较强的响应能力, 通过开展稳定性实验、 选择性实验以及干扰实验等, 对基于S-CDs检测Cu2+的荧光传感系统进行了系统的评价, 并将其应用于湖水样品中Cu2+的选择性检测。
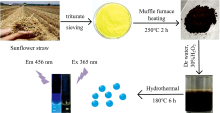 | 图1 向日葵秸秆水热法制备荧光碳量子点的流程示意图Fig.1 Schematic illustration of hydrothermal synthesis of fluorescent carbon quantum dots (S-CDs) from sunflower straw |
实验试剂: 向日葵秸秆(新疆阿勒泰地区)100 ℃烘干并研磨, 过100目筛, 30%H2O2, CoCl2· 6H2O, NaCl, CrO3, CuSO4· 5H2O, HgCl2, FeCl2· 4H2O, CrCl3· 6H2O, FeCl3· 6H2O, MnCl2, MgCl2, NiCl2· 6H2O, Li2CO3, CdCl2, K2CO3, KH2PO4, Na2CO3, K2SO4, NaHCO3, Na2SO3(AR)。
实验仪器: F-4500型荧光分光光度计, 电热恒温干燥箱202-007, UV-3600型紫外分光光度计, SX2-4-10 NP型马弗炉, Vertex 70傅里叶红外光谱仪(FTIR), Thermo Escalab 250Xi X射线光电子能谱仪(XPS), JEM-2100透射电子显微镜(TEM)。
称取适量向日葵秸秆样本, 在250 ℃马弗炉中加热2 h。 取1.0 g加热后的向日葵秸秆样本, 加入1 mL H2O2, 30 mL去离子水溶解搅拌, 密封在50 mL高压反应釜中, 设置加热温度为180 ℃, 加热时间为6 h, 加热结束后, 冷却至室温。 以10 000 r· min-1离心15 min, 分离S-CDs溶液, 然后用0.22 μ m微孔膜过滤器过滤, 得到的S-CDs溶液再转移至1 000 KD透析袋中透析24 h, 透析后的淡黄色S-CDs溶液在4 ℃下避光保存, 用于检测与表征。
根据文献[16]参比法计算S-CDs的荧光产率。 通过紫外-可见分光光度计将硫酸奎宁水溶液(0.1 mol· L-1 H2SO4溶液中, 360 nm激发下, Φ s=0. 54)的吸光度下调至0.05作为对照标准溶液。 同样, 将S-CDs的吸光度下调至0.05。 并在S-CDs的最佳激发波长下分别扫描硫酸奎宁标准参比物和S-CDs溶液的荧光光谱, 通过荧光光度计软件记录综合荧光强度(即荧光光谱的面积)。 分别测试去离子水和0.1 mol· L-1 H2SO4的折射率, 通过式(1)计算S-CDs的荧光QYs
式(1)中: Φ ST为参考物质的荧光QYs, KX和KST分别为线性拟合线的斜率, η X和η ST为折射率。
对Cu2+的检测: 向第1.2节中合成的S-CDs溶液加入计量的Cu2+标准液, 使体系的Cu2+浓度分别为0, 0.05, 0.1, 0.3, 1, 3, 5, 8, 10, 20, 30, 40和50 μ mol· L-1, 样品体系为1.0 mL。 为保证溶液混合均匀, 在317 nm激发波长下, 5 min后记录荧光发射图谱, 在456 nm处测定荧光强度。 为保证S-CDs对Cu2+检测的真实性和可靠性, 在每组实验浓度下测量9个重复样品。
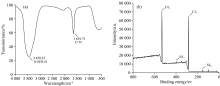
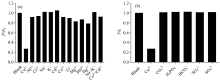
通过透射电子显微镜对向日葵秸秆中提取的S-CDs进行形貌的分析表征, 确定了S-CDs的形貌。 由图2(a)所示, S-CDs呈准球型, 分散性较好, 单个的S-CDs直径在5 nm左右[图2(b)]。 通过FTIR光谱对合成的S-CDs的化学键进行了表征, 如图3(a)所示。 图中3 450.22 cm-1处O— H/N— H的伸缩振动吸收峰, 说明其具有良好的水溶性[17]。 1 639.73 cm-1处的特征吸收带为芳香族CN杂环[14]。 S-CDs的XPS分析图谱如图3(b)所示。 图3(b)中531.09, 283.5, 398.1和152.08 eV处出现的四个峰分别为O(1s), C(1s), N(1s)和S(2p)的峰, 这表明所制备的S-CDs主要由C, O, N和S元素组成。
 | 图2 (a)S-CDs的TEM照片; (b)单个S-CDs的高分辨TEM照片Fig.2 (a)TEM image of S-CDs; (b) HR-TEM image of a single S-CDs |
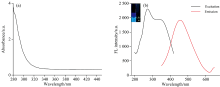
利用紫外-分光光度计和荧光分光光度计分别记录了生物质向日葵秸秆碳量子点(S-CDs)的紫外吸收和荧光光谱(图4)。 图4(a)为水热法合成S-CDs的紫外可见吸收光谱。 制备的S-CDs具有良好的水溶性, 在可见光下呈淡黄色, 在紫外灯照射下呈蓝色荧光。
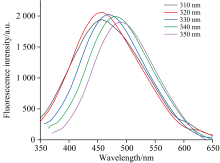
在280~450 nm范围内观察到一个明显的吸收带, 285 nm处存在一个明显的吸收带, 归因于C=C键的π — π * 跃迁[18]。 在最佳激发波长(317 nm)下, S-CDs在456 nm出现一个明显的荧光发射峰[图4(b)]。 为进一步研究S-CDs的荧光性能, 检测了不同激发波长下S-CDs的荧光发射光谱。 如图5所示, 在激发波长的改变下, 发射峰的位置向长波方向移动, 最终在约317 nm的激发波长下得到了最大的荧光发射强度。
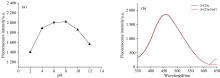
测定了S-CDs在不同pH缓冲绍液中的发光性能, 如图6(a)所示, pH值在2.0~8.0的范围内, 荧光强度呈上升趋势, pH值在8.0~12.0间荧光强度呈下降趋势, 实验结果表明S-CDs的荧光强度对pH值的依赖性较强。 实验结果与羟基修饰的CDs相似[18]。 为进一步证实S-CDs在高离子强度环境下的稳定性, 在1.0 mL体系中加入适量的S-CDs溶液, 加入1 mmol· L-1 NaCl溶液, 在最佳激发波长317 nm, 最大发射波长456 nm的条件下扫描荧光光谱, 图6(b)为加入1 mmol· L-1 NaCl前后S-CDs的荧光发射光谱图。 由图6(b)可知, 在1 mmol· L-1的NaCl溶液中, S-CDs的荧光强度没有发生变化, 说明S-CDs的抗盐能力较好。
为评估S-CDs对Cu2+灵敏度和选择性, 首先, 研究了Cu2+浓度与S-CDs荧光猝灭程度(F/F0)的关系。 实验采用0~50 μ mol· L-1的Cu2+浓度, 测定了S-CDs溶液对Cu2+的敏感性。 结果显示, Cu2+浓度与猝灭程度线性关系的p值为0.022, 小于0.05, 说明二者存在显著性差异。 由图7(a)所示, 随着Cu2+浓度的增加, S-CDs在456 nm左右的荧光强度逐渐降低, 表明该体系对Cu2+非常敏感。 由图7(b)所示, 在0~10 μ mol· L-1围内, 得到了良好的线性相关性(y=0.991 8-0.037x), 相关系数r为0.971 4, 计算出检出限(LOD)为167 nmo· L-1, 低于美国环境保护署规定中饮用水Cu2+含量的上限值(20 μ mol· L-1)[19]。 此外, 探讨了S-CDs对Cu2+的选择性。 分别配置200 μ mol· L-1不同种类金属离子、 金属离子混合物以及阴离子与S-CDs的混合溶液, 在317 nm的激发波长下检测其在456 nm处的荧光发射强度。 结果如图8(a)所示, Cu2+猝灭了72%的S-CDs初始荧光强度, 而在其他金属阳离子以及金属混合物中, 没有发现明显的荧光猝灭现象。 进一步考察了一系列阴离子作为干扰物质对S-CDs荧光的影响。 从图8(b)可以看出, S-CDs溶液中加入Cu2+时, 荧光猝灭明显, 而
为了进一步验证该传感器在水体环境中检测的适用性, 取适量湖水(新疆阿勒泰, 乌伦古湖)为实际样品, 在14 000 r· min-1的转速下离心10 min后, 提取上清液, 0.22 μ m微孔膜过滤器过滤, 采用ICP-MS检测湖水中Cu2+浓度背景值为0.004 mg· L-1。 处理后的水样与不同浓度的Cu2+混合, 采用标准曲线法测定水样中Cu2+的含量(表1) , 样品的回收率在96.18%~109. 22%之间。 加标回收率表明该实验方法的测定结果准确可靠, 验证了S-CDs在实际水体中具有检测Cu2+的潜力。
| 表1 水样中Cu2+的测定结果 Table 1 Results for the determination of Cu2+ in water samples |
研发了一种利用水热法将农业废弃物转化为绿色生物质碳量子点(S-CDs)的简便方法。 向日葵秸秆中木质素与纤维素的存在丰富了S-CDs表面的官能团, 从而增强了S-CDs的光致发光。 制备的S-CDs水溶性好, 表面有丰富的官能团, 有利于S-CDs与Cu2+键合, 形成有效的荧光猝灭。 S-CDs的荧光强度与Cu2+浓度在0~50 μ mol· L-1的动态响应范围内具有良好的线性关系, 在0~10 μ mol· L-1动态响应范围内, 对Cu2+的检出限低至167 nmol· L-1, 可以检测到实际水样中的Cu2+, 回收率较好。 结果表明, 向日葵秸秆作为一种农业废弃物有潜力成为一种生态友好的前驱体材料, 用于制备荧光碳量子点, 进行实际环境中Cu2+的检测。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|