作者简介: 郝 俊, 1981年生, 天津大学环境与工程学院博士研究生 e-mail: haojun588@126.com
钙元素含量直接影响牛奶的品质, 牛奶作为人体摄入钙营养素的一种重要食品来源, 其钙含量分析样品量巨大, 传统基于消解、 灰化等复杂前处理的实验室方法分析效率较低, 因此迫切需要建立牛奶中钙含量的快速及现场分析方法。 近年来, 液体阴极辉光放电-原子发射光谱(SCGD-AES)因无需真空条件和燃气、 载气等附加气体而受到关注。 自主开发了一套采用CCD检测器的便携式液体阴极辉光放电-原子发射光谱仪, 采用牛奶样品直接稀释进样, 考察了该仪器对牛奶中钙含量分析的适用性, 建立了稀酸稀释进样-大气压液体阴极辉光放电-原子发射光谱法快速测定牛奶中钙含量的分析方法。 对该法测定牛奶中钙含量的主要工作条件与参数进行了优化, 结果表明: 酸度对钙元素测定灵敏度的影响显著, 采用1%(V/V)硝酸介质, 该方法对钙元素测定具有最佳的灵敏度和稳定性。 该方法将1%(V/V)硝酸作为牛奶样品的稀释液。 系统考察了稀释倍数对牛奶样品中钙含量测定的影响, 结果表明: 采用100倍以上1%(V/V)稀硝酸稀释, 牛奶中钙含量的测定准确度良好, 未发现显著的基体干扰。 将该方法应用于实际牛奶样品中钙含量的测定, 稀释倍数选取100倍时, 方法检出限为35 mg·L-1, 牛奶样品中钙含量能够准确测定的同时, 无需进一步稀释; 加标回收率在89.0%~109.7%之间; 对同一牛奶样品中钙含量6次重复测试的相对标准偏差低于5%, 且单一样品测试时间小于1 min。 结果表明: 该方法可以满足牛奶中钙含量的实验室快速测定和现场快速分析或筛查要求。
The content of calcium is closely associated with the quality of milk. The traditional analytic methods based on tedious wet digestion or dry ashing preparation techniques are low efficiency. Meanwhile, the milk samples for determination are too much as milk is an important and common food origin for calcium nutrient income. Therefore, it’s in urgent demand for the establishment of the rapid and field analytic method of calcium in milk. Recently, significant attention has been drawn to solution cathode glow discharge-atomic emission spectrometry (SCGD-AES) due to the absence of vacuum conditions as well as the addition of airflow of the fuel and carrier gas, etc. Thus, a portable SCGD-AES instrument was developed with an inside CCD detector, through which practicability for calcium determination in milk was inspected based on direct dilution sampling. Furthermore, the rapid and convenient method was established to rapidly determine calcium in milk using a home-made solution cathode glow discharger coupled with a portable optical fiber spectrometer based on direct dilution sampling. The conditions and parameters influencing the analytical sensitivity of potassium were optimized comprehensively, including the emission wavelength, the acidity of the cathode solution, etc. The results showed that acidity was a key parameter influencing the analytical sensitivity, and when 1%(V/V)HNO3 was used as the medium, the best analytical performances could be acquired. Therefore, 1% (V/V) HNO3 was chosen as the dilution reagent. Furthermore, the selection of the dilution times of the real milk samples was investigated. The results showed that when the milk samples were diluted to 100 times or above, no significant matrix interference was observed and the accuracy could be assured. Under the optimized conditions, when the milk sample was diluted 100 times, the limit of determination for calcium in milk was 35 mg·L-1, which was just suitable for the direct determination, and the relative standard deviations based on 6 duplicate tests of the same milk sample were below 5%. The spiked recoveries were within the range of 89.0%~109.7%. The results showed that the method was simple and reliable and could satisfy the demands of rapid detection of calcium in milk for laboratory and field tests.
钙是保持生命健康不可或缺的营养素之一。 钙元素不仅是构成生命体骨骼组织的主要矿物质成分, 还直接参与机体的代谢活动。 钙是维持细胞生存代谢和机能的主要电解质元素, 其在神经、 肌肉的应激过程以及维持生命体酸碱平衡等方面具有重要作用。 缺钙可能会导致儿童佝偻病, 青少年发育迟缓, 孕妇高血压, 老年人骨质疏松症等诸多问题。 目前, 我国居民日常钙摄入量严重不足, 尤其是儿童、 青少年和老年人缺钙比例比较高[1]。 通过牛奶等高钙食品补钙已经成为一种大众认可的生活或食疗习惯。 牛奶中含有丰富的活性钙, 是奶业加工最重要的产品之一。 钙含量水平直接影响原料奶的质量, 钙元素对维持牛奶的盐类平衡, 保持牛奶体系的稳定性等发挥着至关重要的作用[2]。 通过测定牛奶钙含量可以在一定程度上反映牛奶的品质。
目前, 牛奶中钙含量测试主要采用滴定法[1]、 分光光度法[3]、 火焰原子吸收光谱法[2, 4, 5, 6, 7]、 电感耦合等离子体-原子发射光谱法[8, 9, 10, 11, 12]或离子选择电极法[13, 14]。 其中, 滴定法存在干扰严重、 终点显示不明确、 准确度不高等缺点; 分光光度法分析效率低, 干扰严重; 火焰原子吸收光谱法以及ICP-AES法对牛奶中钙含量分析均依赖于乙炔、 氩气等气体钢瓶, 故对实验室的分析条件要求较为苛刻; 离子选择性电极法电极处理过程较为繁琐耗时, 且需定期维护或更换。 此外, 上述方法均需要借助干灰化或者湿法消解等前处理手段进行样品制备[15], 很难在现场快速分析中应用。 激光诱导击穿光谱(LIBS)法曾有应用于奶粉中金属元素测定[16]的报道, 但该法更加适合固体样品分析, 很难应用于液态奶中钙元素的测定。 牛奶分析样品量巨大, 开发一种无需气体钢瓶, 分析成本低且高效、 灵敏的牛奶中钙含量测定技术具有显著的实用价值。
液体阴极辉光放电-原子发射光谱法在大气压下, 通过在金属阳极和进样溶液阴极间施加一几百到上千伏的电压, 使电极间的气体发生放电, 产生辉光电离, 形成微等离子体。 放电过程中, 液体电极中的溶液不断被气化, 使得溶解在溶液中的金属离子也进入到微等离子体中并受热激发, 进而产生发射光谱, 通过检测不同元素的特征辐射实现溶液中金属离子的定性与定量检测。 目前液体阴极辉光放电-原子发射光谱法已成功应用于水中多种金属元素的分析, 并展现了良好的分析性能[17, 18, 19, 20, 21, 22]。 本工作采用直接酸稀释进样, 采用自制便携液体阴极辉光放电-原子发射光谱仪, 建立了牛奶样品中钙含量的快速、 简便、 高灵敏且可现场应用的分析方法。
实验采用的硝酸为优级纯试剂(北京化工厂); 实验用水为二次离子交换水。
实验采用自主研制液体阴极辉光放电装置(配海洋光学HR-4000光纤光谱仪), 该装置采用注射进样, 结构如图1所示。
牛奶样品, 市售, 购自北京当地超市。
本装置放电室采用钨阳极, 以进样试液作为阴极(石墨为辅助阴极)。 溶液进样由柱塞泵控制, 由切换阀1号位吸入试液5 mL, 而后由2号位经进样管路推入放电室。 由光纤光谱仪采集钙元素在622 nm下的发射光谱。 自制液体阴极辉光放电-原子发射光谱仪器的条件参数: 放电电压700 V; 放电电流35 mA; 放电电极间距离2 mm; 试液流速4 mL· min-1; 光纤光谱仪积分时间100 ms; 进样玻璃管内径0.3 mm× 0.3 mm; 读数方式为峰高模式。
标准系列: 由钙标准储备液(1 000 mg· L-1, 购自中国计量科学研究院), 逐级稀释至浓度分别为0.0, 2.0, 5.0, 15, 20和50 mg· L-1的系列, 保持标准系列硝酸浓度为1%(V/V)。 实验所需其他浓度标准试液也由储备液逐级稀释而得。
准确吸取牛奶样品1 000 μ L至100 mL容量瓶, 用1%(V/V)硝酸稀释至刻度, 充分震荡摇匀, 此为稀释100倍的样品; 准确吸取牛奶样品500 μ L至100 mL容量瓶, 用1%(V/V)硝酸稀释至100 mL, 充分震荡摇匀, 此为稀释200倍的样品。 其他稀释倍数的牛奶样品试液参照以上方法制备。
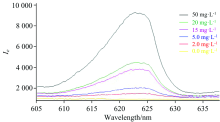
选取0~50.0 mg· L-1钙元素标准使用液, 通过光纤光谱仪采集其发射光谱。 谱图如图2所示, 在622 nm有较强的发射峰。 此外, 在该发射峰波长附近未发现显著的干扰谱线。 本工作采用622 nm作为分析谱线。
液体阴极辉光放电发射光谱仪固体阳极与液体阴极间施加的电压直接影响两极间微等离子体的产生以及等离子体的温度、 稳定性等。 实验采用5 mg· L-1 Ca元素标准溶液, 对660~710 V之间的放电电压对其发射强度的影响进行探究, 结果表明在放电电压低于670 V时, 两极间很难形成稳定的等离子体, 大于700 V时, 基线噪音变大显著。 670~770 V放电电压对Ca元素发射强度的影响如图3所示, 当放电电压在690 V以上时, 灵敏度增加趋势放缓。 综合考虑灵敏度及基线性能, 实验选择700 V放电电压。
试液酸化用酸以及酸度控制对液体阴极辉光放电-原子发射光谱法测定金属元素含量的准确度具有显著影响。 前期工作[18]曾报道了含有1%(V/V)硝酸、 1%(V/V)盐酸、 1%(V/V)硫酸介质对金属元素测定灵敏度的影响: 采用1%(V/V)硫酸介质, 发射强度最大; 采用1%(V/V)盐酸介质, 灵敏度和稳定性均较差; 采用1%硝酸(V/V)介质, 在实现较为理想灵敏度的同时, 具有最佳的稳定性。 牛奶样品中钙元素的含量水平较高, 一般原料奶钙含量在 105~120 mg· (100 g)-1之间[7], 考虑方法的稳定性, 故实验选取1%(V/V)硝酸作为牛奶样品的稀释试剂。
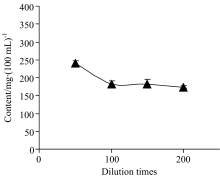
牛奶样品中含有较多的蛋白、 脂肪等有机质, 稀释倍数过低容易给钙元素分析带来基体干扰。 因此, 稀释倍数是保证牛奶中钙元素测定准确度的关键因素。 实验验证了50~200倍稀释倍数范围内, 稀释倍数对测定结果的影响。 结果如图4所示, 当稀释倍数大于100时, 钙含量测定结果趋于稳定, 不存在显著的基体干扰; 稀释倍数低于100时, 进样后容易产生较多的白色泡沫。 综合考虑牛奶中钙元素含量的一般浓度, 钙的检出限以及干扰因素, 实验一般选取稀释倍数100~200, 对于钙含量偏高的牛奶样品可以采用更高的稀释倍数。
由低浓度到高浓度分别测试钙标准系列在622 nm下的光谱发射强度。 采集谱图如图5所示, 以发射强度为纵坐标, 以钙标准溶液浓度为横坐标, 拟合得到钙标准系列的线性方程为I=151.7ρ Ca+171.3, R2=0.999 2。 以11次标准空白发射强度重复测试值的标准偏差的3倍除以标准曲线线性方程的斜率, 考察仪器的检出限, 为0.35 mg· L-1; 当牛奶样品稀释100倍时, 本方法对牛奶中钙元素的方法检出限为35 mg· L-1; 可以满足牛奶样品Ca元素的分析需求[参考浓度水平105~120 mg· (100 g)-1]; 对同一牛奶样品钙元素含量进行6次重复性测试, 相对标准偏差为4.6%。 单一样品测试时间少于1 min。
将本法应用于北京市购牛奶样品中钙元素的测定, 结果如表1所示, 不同浓度水平加标回收率在89.0%~110.7%之间。 平均回收率在100.2%~102.1%, 表明本方法可以较好地应用于实际牛奶样品中钙元素含量的快速测定。
| 表1 加标回收实验结果(n=7) Table 2 Experimental results of spiked recoveries (n=7) |
建立了基于自制便携液体阴极辉光放电-原子发射光谱仪快速测定牛奶中钙含量的方法。 采用本方法, 牛奶样品经稀硝酸酸化并适当稀释后直接进样, 无需复杂的样品前处理和大量的化学试剂, 方便易行, 有效避免了外来污染。 同时, 本方法在不需要使用任何辅助气体钢瓶的条件下, 在1 min内即可实现每个牛奶样品钙元素的快速分析, 且实验结果证明本方法对牛奶样品中钙含量的分析干扰少, 分析结果可靠性强。 此外所采用的自制仪器结构简单且可便携, 对工作条件要求低, 可以有效降低分析成本。 为牛奶中钙含量测定提供了一种新颖的快速测试手段, 可以满足牛奶钙含量质量控制及现场快速筛查的需求。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|