作者简介: 罗 微, 女, 1988年生, 华东交通大学讲师 e-mail: 15270030556@163.com
重金属污染一直影响着人们的健康生活, 如镉, 铅和铜等的污染, 故而土壤重金属的快速检测和如何预防, 一直受各国学者关注和研究。 传统土壤重金属检测方法(如原子吸收光谱法、 X荧光光谱法等)样品预处理复杂, 分析成本较高, 易形成样品的二次污染, 不能满足快速分析的要求。 激光诱导击穿光谱(LIBS)是一种典型的原子发射光谱, 它是基于分析物质中原子和离子受激发而发射的特征谱线信息, 进而研究物质成分的分析方法。 LIBS技术能够快速检测任何状态(固、 液和气态)物质元素的成分和含量, 被看作是未来化学检测和快速绿色分析领域的新兴技术。 LIBS技术具有对样本简单预处理(或不需要处理)、 多元素同步分析、 远距离测量、 适用性广等优势, 被广泛用于生活生产的各个领域, 已成为近年来国内外学者广泛关注和研究的热点之一。 在农业信息快速感知的大背景下, 以激光诱导击穿光谱技术为技术手段, 以土壤重金属铅元素为研究对象, 运用理论分析和数学建模相结合, 建立了多种基于单变量定标曲线的土壤重金属铅检测模型, 并进行了模型验证。 自制15个已知的铅元素浓度梯度的谱线土壤样本, 在获取了土壤LIBS数据之后, 对其进行预处理对比, 建立了基于谱峰强度、 谱峰积分、 洛伦兹拟合强度三种定标曲线模型, 对土壤中铅元素含量进行定量分析, 得出基于三种定标曲线模型对土壤中铅元素含量的预测决定系数 R2分别为0.918 0, 0.910 1和0.914 3, 三种定标曲线分析方法的预测结果都较好, 说明了LIBS结合单变量定标曲线法对土壤中铅含量的检测可靠性高。 最后选取部分样本数据进行验证, 结果较好。 研究结果为研发便携式农田土壤污染物检测技术与装备提供技术支撑, 也为农田精准管理和科学施肥奠定基础。
Heavy metal (like Pb, Cd, Cu, et al) in soil has affected the human health for a long time. So, the detection and prevention of soil Pb content have been a hot topic at home and abroad. Traditional methods of soil heavy metal detection, such as atomic absorption spectrometry (AAS), X fluorescence spectrometry (XRFS), are high cost, complicated, time-consuming, cannot meet the requirements of rapid analysis, and is easy to form secondary pollution of samples. Laser-induced breakdown spectroscopy (LIBS), a typical atomic emission spectrum, is a combination of laser technology and spectroscopic technology. It is based on the analysis of characteristic spectral line information that is excited to emit atoms and ions in a substance, and then compositions of the substance were studied. LIBS technology can rapidly detect the composition and content of material elements in any state (solid, liquid and gaseous). It is regarded as an emerging technology in the field of future chemical detection and rapid green analysis. LIBS technology has the advantages of simple pre-processing (or no processing required) for samples, multi-element simultaneous analysis, long-distance measurement, and wide applicability. Based on those advantages, it is widely used in various fields and viewed as one of the research hotspots. Under the background of agricultural informatization, the elements of Pb in the soil will be considered as the research carriers. And laser-induced breakdown spectroscopy (LIBS) technique combined with theoretical analysis and mathematical modeling will be employed to accurately detect the contents of Pb content. Then, the univariate calibration curve methods were built to predict heavy metal Pb content. Firstly, 15 soil samples with known Pb concentration gradient were selected for analysis. Soil LIBS spectral data were pretreated with different pre-processing methods. Three models based on LIBS intensity, peak areas, Lorentz fit intensity after normalized corresponding Pb content was established and fitted to analyze Pb content in soil quantitatively. The results show that the R2 of soil Pb content prediction based on three calibration curve models are 0.918 0, 0.910 1 and 0.914 3, respectively. The results of the three calibration curve analysis methods are good. It indicates that LIBS combined with univariate calibration curve method showed high reliability in detecting Pb in soil. The research results provide the theoretical foundation for developing the diagnosis and prevention technology of heavy metal contamination in soil and offer technical support for scientific spraying and precision management in agricultural production.
重金属元素长期以来污染着人们赖以生存的土壤, 影响着人类健康和生物繁衍。 近些年随着我国经济的快速发展, 重金属对农田污染的问题也越来越严重, 土壤肥力不断下降, 且重金属一旦污染土壤, 土壤中的重金属不易降解, 通过食物链进入到人们的餐桌, 严重威胁到人们的身体健康[1]。 因此, 迫切需要建立一种快捷、 准确的土壤中重金属元素检测方法, 准确检测出相应元素含量, 从而为研发土壤重金属污染的诊断、 修复和防治技术提供科学依据。
对于物质元素检测主要以仪器分析和化学检测为主, 如原子吸收光谱(atomic absorption spectroscopy)、 X射线荧光光谱(X-ray fluorescence)和电感耦合等离子体(inductively coupled plasma)等[2], 这些检测方法虽灵敏度高, 但检测限较低, 检测过程复杂, 周期长, 对使用人员要求较高, 检测元素种类有限, 样品预处理复杂, 所用试剂易造成环境二次污染等缺点[3]。 激光诱导击穿光谱(laser-induced breakdown spectroscopy, LIBS)结合了激光技术和光谱分析技术优点, 被广泛应用于重金属含量的检测, 采用高能量激光脉冲对待检对象进行烧蚀, 烧蚀点表面会产生瞬态等离子体, 等离子体中的所有元素都会发出带有特征波长的光辐射(元素的光谱“ 指纹” 信息), 同时获取激发产生的等离子体辐射信息[4, 5, 6, 7]。 LIBS技术能够快速检测任何状态(固、 液和气态)物质元素的成分和含量, 具有对样本简单预处理(或不需要处理)、 多元素同步分析、 远距离测量、 适用性广等优势被看作是未来化学检测和快速绿色分析领域的新兴技术[4, 5, 6, 7], 被广泛用于生活生产的各个领域, 已成为近年来国内外学者广泛关注和研究的热点之一。
国内外学者已经开展了基于LIBS技术对土壤重金属元素检测的大量研究。 方丽等在铅蓄电池厂含铅污泥中重金属铅元素含量的定量分析中, 应用激光诱导击穿光谱结合标准加入法, 准确测定了未知样品中的含铅量。 Khan等[8]应用LIBS技术检测土壤中铬(Cr)含量, 由此判断土壤Cr污染程度, 实验检测限为23.71 mg· kg-1, 污水管周围土壤的Cr质量分数为839 mg· kg-1, 水池污泥的Cr质量分数为1 829 mg· kg-1。
本研究以受重金属铅元素“ 污染” 的土壤为对象, 以LIBS为技术手段, 采用数据预处理结果对比、 数学建模、 预测结果反演相结合的方法, 运用单变量定标曲线法(基于谱峰强度、 谱峰强度积分、 洛伦兹谱线拟合强度)对不同土壤样本中的重金属元素铅(Pb)进行了定量分析与结果反演。 研究结果为研发便携式土壤污染物检测技术与装备提供技术支撑, 同时为开发土壤污染诊断、 修复和防治技术和方法提供理论依据, 更为高品质、 安全绿色农业生产保驾护航。
选用的土壤样本为单位试验田的“ 干净” 土壤样本(不含铅), 可以直接作为土壤基体进行实验。 参考国家土壤污染标准, 对土壤基体中添加含铅元素的硝酸铅盐溶液(Pb(NO3)2), 通过不同量的蒸馏水配比, 配备了含15个浓度梯度的铅元素的土壤样品, 并对样本进行编号(1#— 15#), 浓度梯度如表1所示。 在采集LIBS光谱数据时, 为了获得均匀平整的激光烧蚀表面, 需要将土壤样本粉末压片。 采用台式粉末压片机(FY-24, TJSC Co., China)在15 MPa的压强下, 将含铅的土壤样品(约2 g)连续加压3 min, 形成直径为13 mm、 厚度约为3~4 mm圆饼状土壤压片。
| 表1 15个浓度(mg· kg-1)的Pb含量土壤样品 Table 1 The Pb contents of 15 soil samples (mg· kg-1) |
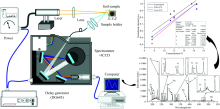
实验用激光诱导击穿元素分析仪(J200, LA-LIBS, ASI Co., USA)的基本结构如图1所示。 系统主要由激光器、 激光光路组件、 X-Y-Z3D样品平台、 光谱仪以及耦合的ICCD检测器、 光谱收集镜头、 数字脉冲延时发生器、 计算机等, 还有相关的附属装置(压片机、 Axiom软件和TruLIBS数据库等)。
为减少LIBS实验数据误差, 将土壤压片样本放置于3D平台上面, 方便获取新鲜的烧蚀点。 同时为了降低每次激光脉冲能量的波动对辐射谱线影响, 每个土壤压片样本在不同位置重复采样20次然后取平均值。 每个梯度样本采集50条光谱数据[9]。 脉冲能量设置为100 mJ, 单次采集频率1 Hz, 脉冲宽度8 ns, 透镜到土壤压片表面距离为97.8 mm(聚焦透镜的焦距为100 mm); ICCD相对于激光器的延迟时间为2.05 μ s, ICCD探测器的曝光时间为0.01 s, 门宽为2 μ s。
LIBS数据经转换和提取后, 为了减小实验参数、 样本基体效应、 实验环境等因素带来的干扰, 使数据便于分析, 需要对原始光谱数据经过一系列预处理操作。 本研究主要用到基线校正、 数据归一化、 异常值剔除和数据平均等方法。 元素特征谱线的识别和选取的基本依据为美国国家标准与技术研究院(NIST)的标准原子光谱数据库[10]中的元素标准谱线。 根据谱线识别依据和方法, 将数据库中的标准谱线和实验采集到的土壤压片样本谱线进行对比分析[11], 初步确定相应重金属元素, 实现定性分析。
在LIBS定量分析中, 定标曲线法是一种常用的方法。 在试验满足一定条件下, 激光诱导等离子谱线强度与待测样品中元素含量成正比关系[12, 13], 即I=acb, I是测得的特征谱线强度; c是待测样本浓度(单位为mg· kg-1); a是常数, 它的值取决于激发条件; b是元素自身含量函数。 根据实验获取到的样本谱线强度和样本对应元素浓度可以拟合相应元素的标定曲线, 最后根据拟合标定曲线和未知样本元素的LIBS谱线强度反演得到未知样本元素浓度含量。 实验结果受谱线展宽、 谱线中心漂移和谱线线型等影响导致元素对应的谱线较多[12, 13], 因此实验得到的特征峰不能代表其真实的强度, 利用谱峰的积分强度和特征谱线洛伦兹拟合强度与样本元素含量来设定标定曲线[11, 12, 13]。
模型的预测能力评价参数采用决定系数(coefficient of determination, R2)、 绝对误差和相对误差。
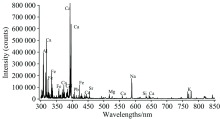
图2为实验随机获取2#样本的平均谱线, 土壤含铅元素样本的LIBS谱线波段区间为300~850 nm, 将标准原子光谱数据库光谱信息和样本谱线进行对比分析, 得到对应元素与谱线中谱峰的归属。 基于所选土壤基体成分相同, 在300~850 nm范围内曲线峰形比较相似, 在300~450 nm范围内, 谱线表现出众多的强度高的谱峰, 且元素分布比较丰富, 而在450~850 nm之间LIBS光谱曲线相对平缓, 光谱峰值较低。
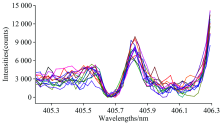
根据NIST的原子光谱数据库和采集到的光谱信息的对比, 选取区间为405.10~406.30 nm范围内的数据, 来建立铅元素的定量分析模型。 LIBS数据经转换和提取后, 需要经过一系列预处理方法(基线校正、 数据归一化、 异常值剔除等)来降低噪声和异常值所带来的影响[14]。 如图3所示为数据预处理后的405.10~406.30 nm范围内60 mg· kg-1(1#样本)浓度下采集到的15个LIBS光谱。
预处理之后, 将每个梯度样品土壤的多条谱线做平均, 得到15个不同浓度梯度下的元素特征谱线, 如图4所示。 图中展示了特征谱线405.82 nm处的光谱强度随着重金属含量的变化趋势, 随着加入铅元素的浓度增加谱线强度产生了较为明显的梯度增加。
土壤样本共分为15个不同的浓度梯度。 随机选取了10个浓度梯度下的土壤LIBS数据作为训练集样本, 构建定量分析的定标曲线, 剩余5个浓度梯度下的土壤LIBS数据作为检验集样本用于验证和反演。 检验集分别是浓度为2#, 4#, 7#, 10#和13#的土壤样本; 训练集分别是浓度为1#, 3#, 5#, 6#, 8#, 9#, 11#, 12#, 14#和15#的土壤样本。 实验发现在波长为405.82 nm处特征光谱达到最高峰值, 因此选取波长为405.82 nm处各个浓度梯度的特征光谱用来建立单变量定标模型。
2.3.1 基于谱峰强度的定标曲线模型
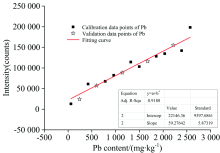
图5为基于谱峰强度的定标曲线, 图中“ ■” 数据点为训练集定标数据, “ ☆” 数据点为检验集定标数据, 图中实直线为训练集的拟合定标曲线。 由拟合结果分析可知, 铅元素含量与其对应样本的谱峰强度有较高的相关性, 决定系数R2为0.918 0。
2.3.2 基于谱线强度积分(峰面积)的定标曲线
图6为基于土壤LIBS谱线积分(峰面积)的定标曲线。 图中“ ■” 数据点为训练集定标数据, “ ☆” 数据点为检验集定标数据, 图中实直线为训练集的拟合定标曲线。 由拟合结果分析可知, 铅元素含量与其对应样本的谱线强度积分值有较高的相关性, 决定系数R2为0.910 1。
2.3.3 基于光谱曲线洛伦兹拟合的定标曲线
图7为铅元素与光谱曲线洛伦兹拟合强度建立定标模型。 图中“ ■” 数据点为训练集定标数据, “ ☆” 数据点为检验集定标数据, 图中实直线为训练集的拟合定标曲线。 由拟合结果分析可知, 铅元素含量与其对应样本的光谱洛伦兹拟合强度也有较高的相关性, 决定系数R2为0.914 3。
由定标曲线表达式计算得出预测结果与实际结果如表2。 根据建立的定标曲线的表达式, 可以对已知特征谱线的未知土壤样本中铅元素浓度进行反演预测。 实验选用2#, 4#, 7#, 10#和13#共5个浓度梯度下的检验集土壤样本对预测结果进行检验。
| 表2 对土壤中铅元素浓度的预测结果验证 Table 2 Verification of the prediction results of Pb contents in soil |
由表中预测及验证结果分析, 可知基于谱峰强度、 谱峰强度积分(峰面积)、 洛伦兹拟合强度三种定标曲线模型分析精度较高且相近。 验证结果表明, 三种定标曲线模型对2#样本的预测结果很差, 预测相对误差最低为83.66%, 而对其他浓度样本的预测结果良好, 相对误差最高仅为5.78%。 通过查阅相关文献资料, 对比实验各个步骤的细节, 综合分析认为造成这种现象的原因为2#土壤样本铅元素浓度过低, 未达到三种定标方法的检测限, 导致预测结果与实际浓度偏差过大, 由此得出未知样本元素浓度是LISB检测中要考虑的一个重要的参数。 对于4#样本的预测结果, 三种定标曲线模型分析精度有明显差异, 谱峰强度积分(峰面积)标定曲线模型的相对预测误差是5.00%, 而另外两种标定曲线模型的相对预测误差仅为1%, 原因可能是谱峰强度积分在计算时受到基体的影响。 对10#样本三种定标曲线模型的相对预测误差都为5%左右, 较高于其他三个样本, 主要是因为采集到的10#样本LIBS谱线波动较大, 预处理效果不佳, 考虑是激光能量波动和LIBS数据采集环境温度变化引起的, 这也是LIBS数据采集中时刻关注的重要影响因素。
本研究以LIBS技术为手段, 以土壤为研究载体, 以重金属铅为研究对象, 运用理论分析和数学建模相结合, 建立了多种基于单变量定标曲线法的土壤铅元素检测方法。 配备15个浓度梯度下受“ 污染” 土壤铅元素样本, 选取波长为405.82 nm处各个浓度梯度的特征光谱用来建立单变量定标模型。 经过光谱预处理后, 利用定标模型预测了土壤中铅元素的含量, 建立了基于谱峰强度、 谱线强度积分(峰面积)、 洛伦兹拟合强度的三种定标曲线模型, 预测决定系数R2分别为0.918 0, 0.910 1和0.9143。 结果验证时, 发现除浓度过低的2#浓度梯度外, 其余预测样本预测误差均比较小, 其中基于谱峰强度的定标模型较其他两种定标模型预测误差更小, 本研究实现了基于LIBS特征谱线的未知土壤样品中铅元素定量分析检测。 研究结果为后期开发高效、 适用、 可靠的LIBS土壤污染检测仪器设备提供技术支撑, 并为农田科学施药和精准化管理提供理论基础。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|