作者简介: 张 玉, 女, 1995年生, 东华大学化学化工与生物工程学院硕士研究生 e-mail: 1150119229@qq.com
L-精氨酸(L-Arginine, L-Arg)是蛋白质的重要组成部分, 也是人类某些疾病的重要诊断标准之一, L-Arg的浓度变化可能会导致许多疾病的问题, 因此如何高效且灵敏地检测L-Arg极其重要。 目前, 对L-Arg的研究大多数是利用其作为NO(一氧化氮)的前体, 来预防或缓解某些疾病的产生, 对于L-Arg的定性检测并不多, 而利用质子转移形成络合物/加成物的方式检测L-Arg更是少之又少。 基于异氟尔酮设计并合成了一种含有丙二腈以及2,4-二羟基苯甲醛的比色探针(ISO-CN-OH), 该探针可以用于快速检测L-Arg。 通过紫外吸收光谱研究发现, 当向探针ISO-CN-OH溶液中加入L-Arg后, 其紫外吸收光谱在669 nm处的吸收峰急剧增强, 且溶液的颜色由橙黄色变为墨绿色, 而其他氨基酸的加入不产生吸收峰以及溶液颜色的变化。 通过对探针ISO-CN-OH进行抗干扰性实验, 表明探针ISO-CN-OH对L-Arg具有专一选择性及良好的抗干扰能力。 通过对L-Arg进行光谱滴定研究, 实验结果表明在1.0~10.0×10-6 mol·L-1浓度范围内, 具有良好的线性关系( R2=0.997), 线性归方程式为 y=0.020 x+0.073, 根据 DL=3 σ/K可计算出ISO-CN-OH的检出限为8.5×10-8 mol·L-1, 这表明探针ISO-CN-OH具有高灵敏性。 通过固定探针ISO-CN-OH与L-Arg的总浓度为100 μmol·L-1, 改变L-Arg占总浓度的比例, 根据其吸收光谱的Job’s plot滴定曲线分析可知, 当L-Arg占总浓度比例为0.67时, 探针ISO-CN-OH在669 nm处紫外吸收强度达到最大值, 这表明探针ISO-CN-OH与L-Arg以1∶2的络合比进行配位络合。 为了更进一步了解探针ISO-CN-OH与L-Arg的配位机理, 进行了1H-NMR滴定实验, 在探针ISO-CN-OH的DMSO-d6溶液中分别加入0, 0.5, 1.0及2.0当量的L-Arg(d2O), 研究发现加入L-Arg后ISO-CN-OH的羟基峰消失, 且其羟基周围氢质子共振峰的位置明显发生了偏移。 该研究结果表明探针ISO-CN-OH通过将酸性的酚羟基质子转移到L-Arg碱性的胍基NH基团上, 导致—OH基团附近形成负电荷, 该负电荷与精氨酸的胍基部分络合, 从而形成络合物/加成物, 使得紫外可见光谱图在669 nm处出现新峰, 且溶液颜色由橙黄色变为墨绿色。 该研究为今后设计检测L-Arg探针分子奠定了基础。
L-Arginine (L-Arg) is an important component of protein and one of the important diagnostic criteria for certain diseases in humans. The concentration change of L-Arg may cause many health problems. Therefore, it is very important to detect L-Arg efficiently and sensitively. At present, most research work based on L-Arg is used as the precursor of NO (Nitric Oxide) to prevent or alleviate some diseases. It are rarely reported for qualitative tests of L-Arg, and the detection of L-Arg by proton transfer to form complex/adduct is even less. In this paper, a colorimetric probe ISO-CN-OH based on isophorone, malononitrile and 2,4-dihydroxybenzaldehyde was designed and synthesized. The method based on proton transfer forming complex/adduct for detection of L-Arg rapidly were found. The UV-Vis spectra showed that absorption peak of the probe at 669 nm increased sharply when L-Arg was added into the ISO-CN-OH and the color of the solution changed from orange yellow to dark green. However, no color and absorption peak change was observed while other amino acids were added. Besides, ISO-CN-OH could detect L-Arg specifically without any interference by competition experiments. What’s more, the titration experiment of L-Arg, showed There is A good linear relationship ( R2=0.997) between the relative absorption intensity ( A- A0) and the concentration of L-Arg within the concentration range of 1.0~10.0×10-6 mol·L-1. And the linear regression model was y=0.020x+0.073. According to DL=3 σ/K, the detection limit of ISO-CN-OH was 8.5×10-8 mol·L-1, which indicated that the probe had very high detection sensitivity. Fixing the total concentration of ISO-CN-OH and L-Arg was 100 μmol·L-1, and the ratio of L-Arg to the total concentration is changed to get the job’s plot titration curve. According to the job’s plot titration curve analysis, it is found that the UV absorption intensity of ISO-CN-OH reached the maximum at 669 nm when the ratio of L-Arg to the total concentration was 0.67, which indicated that ISO-CN-OH coordinated with L-Arg in the ratio of 1∶2. In order to further understand the coordination mechanism of ISO-CN-OH and L-Arg,1H-NMR titration experiment was carried out. 0, 0.5, 1.0 and 2.0 equivalent of L-Arg ( d2O) were added into the DMSO- d6 solution of ISO-CN-OH respectively. It was found that the hydroxyl peak of ISO-CN-OH disappeared and the hydrogen around the hydroxyl group shifted after adding L-Arg. The results showed that ISO-CN-OH causes the formation of negative charges near the —OH group by transferring acidic phenolic hydroxyl protons to l-ArG alkaline guanidine NH group. The forming negative charge complexed with the guanidine part of arginine to form a complex/admixture, which result in a new peak at 669 nm, and the color solution change. The study based on proton transfer forming complex/adduct for detection of L-Arg will provise certain guidelines for the design of L-Arg probe molecules in the future.
氨基酸是一种含有碱性氨基和酸性羧基的有机化合物, 它既是生命体中蛋白质的基本组成部分, 同时也是参与生命体的修复和再生的必须物质[1]。 在20种天然氨基酸中, 精氨酸(L-Arg)有不可代替的优势, 在一端的旁链处存在着高碱性的胍基, 其pKa高达12.48, 使得其在酸性、 中性及碱性条件下均带正电荷[2, 3]。 L-Arg作为NO(一氧化氮)的前体, 在动物的生存, 繁殖, 生长, 抗衰老和免疫方面起着重要的作用。 越来越多的临床试验表明, 在饮食中适当填加L-Arg可以减轻体重, 降低动脉血压, 抵抗氧化并使内皮功能正常化, 从而缓解高血压[4], 同时也可以促进孕妇在孕期胎盘和胚胎的生长[5]。 精氨酸在细胞分裂, 伤口愈合, 免疫系统, 激素的释放, 尤其是基因调节, 糖蛋白靶向和囊泡运输中起着重要作用[6, 7]。 因此, 对精氨酸的选择性识别研究是生物化学和医学科学领域的关键课题之一[8, 9]。
目前, 报道检测L-Arg的方法有很多但均存在一些缺点, 如使用高效液相色谱法(HPLC)[10]检测时对L-Arg的选择性差, 采用电化学[11]方法检测时对于精氨酸甲基化蛋白的修饰过程比较复杂, 选择离子交换色谱法[12]检测时对方法条件及仪器均具有较高的要求, 利用毛细管电泳[13]检测时样品处理过程较为复杂, 从而限制了它们在实际生活中的应用。 因此, 操作简单迅速, 高灵敏度以及价格低廉的探针就成了有效检测氨基酸的方法之一。
比色探针作为一种可以通过检测分析物的颜色及吸收光谱变化的检测方法, 可以实现对氨基酸定性以及定量的检测分析。 因此, 基于异氟尔酮设计并合成了可以用于精氨酸(L-Arg)检测的一种新型比色探针ISO-CN-OH。 通过对ISO-CN-OH进行光谱性能研究, 发现ISO-CN-OH对L-Arg具有高选择性以及高灵敏性, 并通过紫外可见吸收的Job’ s plot曲线及1H-NMR核磁滴定波谱, 详细研究了探针ISO-CN-OH与L-Arg的配位机理, 并利用配位模型图模拟出ISO-CN-OH与L-Arg的配位过程。
上海豫华仪器有限公司DF-101S集热式恒温式加热磁力搅拌器; 瑞士Bruker公司Bruker AVANCE/DMX600型核磁共振仪器; 美国热电集团Nicolet 8700型傅里叶变换红外光谱仪; PerkinElmer UV/Vis Spectrometer Lambda 35。 所用药品试剂和溶剂均为市售分析纯。
异氟尔酮-丙二腈(ISO-CN)按照文献[14]的方法合成。
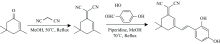
探针ISO-CN-OH的合成路线如图1所示。
将ISO-CN(372.5 mg, 2 mmol)与2, 4-二羟基苯甲醛(276.2 mg, 2 mmol)溶解在20 mL的无水乙醇中, 加入2~3滴哌啶, 将混合物在氮气保护下, 70 ℃搅拌回流过夜直至产物点出现(用TLC跟踪, 展开剂为石油醚/乙酸乙酯, V/V=2:1)。 将混合物冷却至室温, 旋蒸除去溶剂, 将残留物溶于二氯甲烷, 多次萃取, 经无水MgSO4干燥后, 旋转蒸发溶剂, 通过色谱柱进行收集(石油醚/乙酸乙酯, V/V=20:1), 得到红棕色固体粉末ISO-CN-OH, 45 ℃真空烘箱烘干至恒重(产率71.8%)。 结构表征如下: 1H NMR (600 MHz, DMSO-d6) δ 10.10 (s, 1H), 9.91 (s, 1H), 7.54 (d, J=8.7 Hz, 1H), 7.42 (d, J=16.1 Hz, 1H), 7.14 (d, J=16.1 Hz, 1H), 6.71 (s, 1H), 6.35 (d, J=2.3 Hz, 1H), 6.28 (dd, J=8.6, 2.3 Hz, 1H), 1.23 (s, 6H), 1.01 (s, 4H); 13C NMR (151 MHz, DMSO) δ 170.64, 161.27, 158.59, 157.98, 134.12, 129.46, 125.50, 120.96, 115.00, 114.02, 108.64, 102.91, 74.03, 42.83, 40.52, 40.40, 40.26, 40.12, 39.99, 39.85, 39.71, 39.57, 38.66, 32.15, 27.89, 26.81; IR (KBr), ν (cm-1): 3 431.74 (—OH), 2 220.83 (—C≡ N) 2 953.34 (—CH3), 1 615.47 (C=C)。
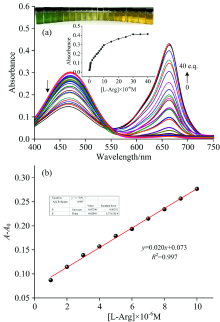
选择21种常见的氨基酸作为研究对象, 探究了探针ISO-CN-OH与不同氨基酸之间的紫外可见光谱性能, 实验结果如图2(a)所示。 发现在DMSO/H2O (95/5, V/V, PBS=7.0)溶液中, 探针ISO-CN-OH本身在471 nm处呈现吸收峰, 当分别向探针中加入10当量的L-His, L-Ala, L-Gly, Cys, L-Val, L-Pro, L-Leu, L-Phe, L-Ser, L-Met, L-Glu, L-Asp, L-Lys, L-Thr, L-Tyr, GSH, L-Asn, L-Trp, L-lle和L-Gln时, 在471 nm处的吸收峰并没有发生明显的改变, 但是在669 nm处出现了新的微弱的吸收峰, 且溶液的颜色并无明显的改变。 仅向溶液中加入10当量的L-Arg时, 光谱在669 nm处出现强吸收峰且溶液颜色由原本的橙黄色变为了墨绿色。 该吸收光谱实验结果表明, 探针ISO-CN-OH是对L-Arg具有高度选择性的比色探针, 且响应灵敏, 检测结果肉眼可视。
为了排除共存的氨基酸对L-Arg的识别产生干扰, 进行了对L-Arg的竞争性实验测试。 在其余20种氨基酸的ISO-CN-OH溶液中分别加入等当量的L-Arg, 由图2(b)可知, 其余20种氨基酸的存在并不会影响探针ISO-CN-OH对L-Arg的紫外识别。 因此, 探针ISO-CN-OH对L-Arg的紫外识别具有较强的抗干扰能力。
在DMSO/PBS(95/5, V/V, PBS=7.0)体系中, 进行紫外-可见光谱滴定实验研究。 如图3(a)所示, 随着L-Arg浓度的增加, 探针ISO-CN-OH在669 nm处的吸收峰强度逐渐上升, 441 nm处的吸收峰逐渐下降, 这表明ISO-CN-OH与L-Arg形成了稳定的复合物。 除了在669 nm处产生新的吸收, 在550 nm处还出现了等吸收点, 这也为ISO-CN-OH+L-Arg络合物的形成提供了进一步的证据。 当L-Arg的浓度在1.0~10.0×10-6 mol· L-1范围时, 根据ISO-CN-OH+L-Arg在669 nm处的吸收强度与不同浓度做线性回归曲线, 线性回归方程式为y=0.020x+0.073, R2=0.997, 如图3(b)所示, 根据DL=3σ /K, 其中σ 为探针ISO-CN-OH溶液平行测试20次的标准偏差, K为线性回归方程的斜率, 可计算出检出限为8.5×10-8 mol· L-1。
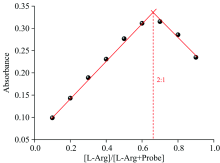
通过固定探针ISO-CN-OH与L-Arg的总浓度为100 μmol· L-1, 改变L-Arg占总浓度的比例, 测其在669 nm处的吸收强度。 由此获得探针ISO-CN-OH对L-Arg的Job’ s plot滴定光谱吸收曲线, 如图4所示。 当L-Arg占总浓度比例为0.67时, 发现探针ISO-CN-OH在669 nm处紫外吸收强度达到最大值, 根据计算公式n=Xmax/(1-Xmax)可得n=2, 表明探针ISO-CN-OH与L-Arg以1:2的络合比进行配位络合。
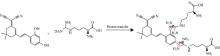
在确定了配位比的基础上, 通过核磁滴定实验来进一步确定配位机理。 在探针ISO-CN-OH的d6-DMSO溶液中分别加入0, 0.5, 1.0及2.0当量的L-Arg(d2O), 结果如图5(a)所示。 当加入L-Arg后, 探针上的羟基氢H2(9.83 ppm)和H4(8, 76 ppm)峰逐渐消失, 如图5(b)放大图所示。 此外, 羟基周围的氢信号峰发生了向高场的偏移, H1峰从7.08 nm逐渐偏移到6.96 nm, H3峰从6.67 nm逐渐偏移到6.54 nm, H5峰从6.32 nm逐渐偏移到6.10 nm, 且在高场区出现了L-Arg的特征峰Ha(3.15 ppm)和Hb(1.54 ppm), 如图5(a)所示。 上述结果表明探针ISO-CN-OH上的羟基与L-Arg结合形成了络合物, 从而引起了羟基以及周围氢化学环境的变化。 出现上述结果的原因是探针ISO-CN-OH具有两个酸性酚羟基, 且L-Arg属于强碱, 其pKa=12.48, 有足够的能力去除羟基中的质子, 因此探针ISO-CN-OH通过将酸性的酚羟基质子转移到L-Arg碱性的胍基NH基团上, 导致羟基基团附近形成负电荷, 该负电荷与精氨酸的胍基部分络合, 从而形成了络合物, 即ISO-CN-OH与L-Arg通过质子转移形成了稳定的络合物[15]。
基于以上光谱分析, 可以得到探针ISO-CN-OH与L-Arg的配位模型如图6所示。
通过设计并合成了一种可以用于检测L-Arg的比色探针, 采用各种光谱分析方法, 研究了其光学性能及配位机理, 发现该探针可以专一性识别L-Arg, 溶液颜色发生了从橙黄色到墨绿色的改变。 滴定实验表明L-Arg在1.0~10.0×10-6 mol· L-1范围内具有良好的线性关系, 最低检测限为8.5×10-8 mol· L-1, 表明该探针对L-Arg具有高灵敏度。 基于核磁共振谱滴定的方法, 通过对ISO-CN-OH与L-Arg的配位机理的研究, 发现ISO-CN-OH与L-Arg是通过质子转移方式形成络合物。 本研究为今后L-Arg新型探针分子的设计, 提供重要光谱研究方法与分析基础。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|