作者简介: 姚 蒙, 1994年生, 华南理工大学化学与化工学院硕士研究生 e-mail: 1578967184@qq.com
氯化钠水溶液中, 水分子之间的氢键相互作用随氯化钠浓度变化而发生改变, 导致不同浓度的水溶液光谱形状也不同, 因此NaCl溶液的光谱不满足朗伯比尔定律。 如果浓度c与吸光率A不满足朗伯比尔定律, 则利用光谱差减技术扣除溶剂水的吸收峰问题就会遇到瓶颈, 差减效果不能令人满意。 利用二元线性回归分析法和双边夹原理合成杂化光谱, 期望在偏离朗伯比尔定律体系, 可以理论上获得各种浓度的NaCl水溶液的杂化光谱, 并且保证杂化光谱与其代表的真实光谱高度相似。 主要结论如下: (1)浓度 c1和 c2的NaCl水溶液的红外光谱分别为$A_{c_1}$和$A_{c_2}$, 则浓度介于 c1和 c2之间的溶液光谱, 均可用 Ahc( c1, c2)=$\hat{a}A_{c_1}+\hat{b}A_{c_2}$来表示。 Ahc( c1, c2)与浓度为 c( c1< c< c2)的溶液的真实光谱 Ac高度类似。 (2) c2和 c1间隔越小, 杂化光谱 Ahc( c1, c2)与真实光谱 Ac的相似度越高, 因此可根据精度要求选择合适的$A_{c_1}$和$A_{c_2}$来拟合 Ahc 。 (3)杂化光谱 Ahc(2%, 30%)=$\hat{a}$A2%+$\hat{b}$A30%, 适用浓度区间2%~30%, 涵盖浓度范围宽, 效果令人满意。 (4)回归系数$\hat{a}$和$\hat{b}$与浓度 c关系为$\hat{a}$=-3.592 c+1.058 9,$\hat{b}$=3.565 c-0.0551 5。 在2%~30%浓度范围内, 选取浓度 c数值, 即可获得相应回归系数$\hat{a}$和$\hat{b}$, 再将$\hat{a}$和$\hat{b}$代入方程 Ahc(2%, 30%)=$\hat{a}$ A2%+$\hat{b}$ A30%, 即可获得NaCl水溶液的杂化光谱。 杂化光谱与相对应的真实光谱高度近似, Ahc(2%, 30%)≈ Ac, 完全可替代真实光谱。
If the solution concentration c and the spectral absorbance A is not obeyed Lambert-Beer’s Law, an individual solution sample should be prepared and acquired in order to obtain its infrared spectrum. The binary linear regression analysis and hybrid spectrum were applied to NaCl aqueous solution. The following conclusions have been reached: (1) The infrared spectra of NaCl aqueous solutions with concentrations of c1, c2 are $A_{c_1}$,$A_{c_2}$, respectively. Then the regression equation Ahc( c1, c2)=$\hat{a}A_{c_1}+\hat{b}A_{c_2}$ is set up, where the relationship among c1, c2 and c is c1< c< c2. Hybrid spectrum Ahc( c1, c2) can be very similar to real spectrum Ac if $\hat{a}$ and $\hat{b}$ values are selected properly. (2) The smaller difference between c2 and c1, the higher similarity between Ahc( c1, c2) and Ac is. (3) The regression equation Ahc(2%, 30%)=$\hat{a}$A2%+$\hat{b}$A30% can be applied to the concentration range 2%~30%. (4) The relationships between $\hat{a}$ and c,$\hat{b}$ and c are c=-3.592 c+1.058 9 and $\hat{b}$=3.565 c-0.055 15. If we select c, we can easily obtain $\hat{a}$ and $\hat{b}$ then $\hat{a}$ andb$\hat{b}$ are substituted into regression equation Ahc( c1, c2)=$\hat{a}A_{c_1}+\hat{b}A_{c_2}$. All hybrid spectra are very similar to the real spectra and they can even replace the real spectra.
氯化钠水溶液广泛应用于医学、 生物、 化工[1, 2, 3, 4]等行业, 因此, 研究NaCl水溶液的各种物理化学性质具有重要意义。 近年来, 众多研究者利用不同的实验方法和手段, 从不同的角度, 研究了NaCl水溶液的各种特性, 包括分子动力学[5]、 拉曼光谱等[6]。 此外, 红外光谱(IR)和化学计量学也是研究NaCl水溶液的常用手段。 浓度、 温度对NaCl水溶液红外光谱的影响是研究热点之一[7]。 Rauh等[8]利用化学计量学和红外光谱对溶液进行定量分析, 获得了Na+和Cl-在水溶液中的含量。 Peters等[9]通过建立数学模型来区分NaCl水溶液和KCl水溶液的红外光谱。 Max等[10]运用化学计量学中的因子分析法处理NaCl水溶液的红外光谱, 发现在整个盐溶解度范围内水都有两种稳定的存在形式, 阴离子和阳离子都与水分子有很强的相互作用。
然而, 运用化学计量学来分析红外光谱通常需具备扎实的专业知识和大量光谱数据, 并且能够熟练操作相关数据分析软件, 门槛高, 耗时长。 回归分析法[11]利用数理统计方法对实验的观测值进行处理, 并用此进行预测与控制, 操作简单, 原理易懂, 分析速度快。 由于水分子在中红外区有强吸收, 为控制水的吸收峰强度, 通常液体池厚度需要控制在微米量级, 这给水溶液的透射红外光谱测量带来很大困难[9, 10]。 而红外衰减全反射(attenuated total reflection, ATR)技术已成功地用于研究水溶液的红外光谱, 能够迅速得到溶解或分散于水溶剂中的溶质的高质量红外光谱[12, 13]。 本文利用FTIR-ATR技术获得不同浓度的NaCl水溶液的红外光谱, 运用线性回归分析法处理红外光谱数据。 如果溶液满足朗伯比尔定律, 已知浓度为c的IR吸光率谱A, 则乘以相应系数γ , 就可以得到浓度γ c的溶液吸光率谱γ A。 氯化钠溶液中, 氢键相互作用随氯化钠浓度变化而发生改变, 导致不同浓度的水溶液光谱形状也发生变化, 因此NaCl溶液的光谱不满足朗伯比尔定律。 从已知浓度c的光谱得到其他浓度的光谱就出现了新问题。 为解决偏离朗伯比尔定律体系的光谱问题, 利用杂化光谱的概念和二元线性回归分析, 开展相关研究工作。 首先, 以浓度为c1和c2的NaCl水溶液吸光率谱
NaCl购于广东化学试剂厂, 为分析纯试剂, 使用前未经进一步纯化。 超纯水用Milli-Q水净化系统制备得到。 NaCl水溶液的浓度用溶质质量(g)/溶液体积(mL)百分比表示, 例如1.0 g NaCl溶于水中, 转移到10 mL的容量瓶并定容, 得到的NaCl水溶液浓度为10%。 用同样的方法分别配制浓度为2%, 4%, 6%, …, 28%, 30%(步长2%)以及5%, 13%, 15%, 19%, 23%, 25%的NaCl水溶液。
水和NaCl水溶液的红外光谱由Nicolet iS50傅里叶变换红外光谱仪测量得到, 配备DTGS检测器。 衰减全反射附件所用晶体为金刚石, 入射角为45° 。 红外光谱测量采用的分辨率为4 cm-1, 测量波段为4 000~1 000 cm-1, 背景为空白ATR晶体, 样品为水或不同浓度的NaCl水溶液, 样品和背景各扫描32次, 室温25 ℃。
浓度为c1, c和c2(c1< c< c2)的NaCl水溶液的红外吸光度谱, 分别表示为
其中
将得到的数据导入Origin软件, 作图得到波数~Δ Ac曲线, 即红外光谱Ac与合成光谱
真实光谱Ac与杂化光谱Ahc(c1, c2)差谱的计算式如式(4)
将式(4)结果导入Origin软件, 作波数与Δ Ahc关系曲线, 即得到其红外差谱。 假设回归系数
选择希望的浓度c分别代入式(5)和式(6), 就可得到
水在2 500~1 900 cm-1波段没有吸收峰。 因此, 在进行二元线性回归分析时, 去除2 500~1 900 cm-1波段的数据, 只研究4 000~2 500 cm-1波段以及1 900~1 000 cm-1波段。
NaCl分子在4 000~1 000 cm-1波段没有红外吸收。 ~3 400和~1 640 cm-1处分别是水的OH伸缩振动吸收带和变角振动吸收带[14]。 研究表明, 水分子间的氢键作用力越强, OH伸缩振动频率向低波数位移越多, 该吸收谱带越宽[14]。 此外, 水的OH变角振动频率会随氢键作用力的增强而向高波数移动[9]。
图1是一系列不同浓度的NaCl水溶液的红外光谱, 氯化钠溶液浓度范围2%, 4%, 6%, …, 28%, 30%, 步长为2%。 随着NaCl浓度的增加, OH伸缩振动吸收峰的位置向高波数位移, 由3 320 cm-1移至3 373 cm-1, 同时OH变角振动吸收峰的位置向低波数位移, 由1 635 cm-1移至1 632 cm-1。 从图1可以看出, OH伸缩振动吸收峰的形状随溶液浓度也发生了明显变化。 图1结果表明, NaCl的加入影响了水分子的氢键结构, NaCl浓度越大, 氢键结构被影响的程度越大。
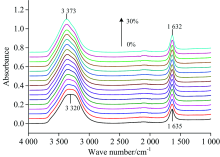 | 图1 不同浓度(0, 2%, 4%, …, 28%, 30%, 步长2%)NaCl水溶液的FTIR光谱Fig.1 FTIR spectra of NaCl aqueous solutions(0, 2%, 4%, …, 28%, 30%, step 2%) |
Sun利用拉曼光谱对纯水进行了研究[15], 并给出水的氢键结构模型。 水分子与周围的水分子形成氢键时, 可以是质子给体(donor, 记为D), 也可以是质子受体(acceptor, 记为A), 还可能同时是质子给体和质子受体。 水分子的主要氢键模型可分为DDAA, DDA, DAA和DA等。 DDAA氢键模型是四面体结构, DA氢键模型为环状或链状结构。 当温度为20 ℃时, 研究中通过对水的OH伸缩振动区域的谱带进行解卷积得到了5个子带, 分别位于3 014, 3 220, 3 430, 3 572和3 636 cm-1, 分别代表DAA, DDAA, DA和DDA氢键模型中的OH伸缩振动和未缔合的水分子的OH伸缩振动带。 此外, 经过拟合分析, 发现DDAA和DA氢键模型是水分子间氢键的主要结构。 对于特定的振动模式, 红外吸收波数与拉曼位移均对应于基态与第一激发态之间的跃迁, 因此水的红外吸收频率与相应谱带的拉曼位移相近。
图2是浓度分别为2%, 6%, 10%, 14%, 18%, 22%, 26%和30%的NaCl水溶液光谱与纯水的红外光谱的差谱。 差谱中, 在水的OH伸缩振动区域, 3 173和3 412 cm-1分别有一个强的负吸收峰和正吸收峰, 3 312和3 630 cm-1各有一个等吸收点。 图2表明, 随着氯化钠浓度变化, 各种氢键结构的水的百分含量发生明显变化。 显然, 这些变化导致氯化钠溶液不再满足朗伯比尔定律, 因此, 利用不同浓度的NaCl水溶液FTIR谱进行差减光谱操作, 不可能彻底扣除水的影响而得到希望的结果。 即对NaCl水溶液, 传统的光谱差减法是失效的。
图2表明, NaCl水溶液的傅里叶红外光谱随浓度改变而发生形状变化, 因此, 如果已知5%氯化钠溶液的红外光谱, 则理论上不能精准预测10%氯化钠溶液的红外光谱形状。 为此, 尝试利用双边夹原理解决上述问题。 期望由5%和15%溶液谱拟合得到它们之间的溶液, 如10%溶液的光谱。 已知浓度c介于c1和c2之间, 假定它们的光谱之间, 即因变量Ac 与自变量
| 表1 Ac与 |
表1中的因变量为A16%, 两个自变量分别是浓度低于16%和高于16%的NaCl水溶液的吸光度谱, 比如A8%和A24%。
对回归方程进行了有效性检验, 采用F检验法、 T检验法和r检验法[11]。 表2给出了利用软件SPSS对回归方程进行线性回归效果的显著性检验数据。 查统计表得Fα =3.00(置信度95%), 表2中F值远远大于Fα , 这表明A16%与
| 表2 回归方程的线性回归效果的显著性检验 Table 2 The significance test of linear regression effect of the regression equations between A16% and |
根据表1的线性回归方程, 计算残差Δ A16%=A16%-
表1中, 回归系数│
选择光谱A2%和光谱A30%作为自变量, 光谱Ac为因变量, 进行二元线性回归分析可得到一系列回归方程。 根据2.2节可知, 忽略
| 表3 Ahc与A2%和A30%的杂化光谱方程 Table 3 The hybrid spectra equations between Ahc and A2%, A30% |
采用F检验法、 T检验法和r检验法检验上述回归方程的有效性。 统计结果表明, 杂化光谱回归方程有意义。 估计标准误差很小(表3中, 估计标准误差最大数值为6.3× 10-4), 因此, 杂化光谱Ahc(c1, c2)与真实光谱Ac高度相似。 上述结果表明, 不需制备浓度28%真实溶液样品, 就可获得与真实光谱A28%高度类似的杂化谱Ah28%(2%, 30%)。
将真实光谱Ac与杂化光谱Ahc(2%, 30%)相减, 差谱数据Δ Ahc=Ac-Ahc(2%, 30%)导入Origin, 得到图5。 图5再次表明, 2%~30%浓度范围内任一浓度的光谱Ac, 可以用2%和30%的光谱合成得到的杂化谱替代, 杂化光谱Ahc与真实光谱Ac高度相似。
表4列出了回归方程中回归系数
| 表4 回归系数 |
假设
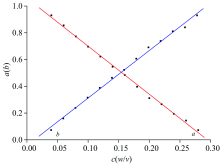 | 图6 回归系数与浓度拟合曲线 (a): (a): |
将浓度5%代入方程
随NaCl浓度变化, NaCl水溶液的傅里叶变换红外光谱形状发生改变。 浓度2%~30%范围内, NaCl溶液红外光谱不满足朗伯比尔定律。 利用二元线性回归分析和双边夹原理(c1< c< c2), 用c1溶液光谱
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|