作者简介: 汪 雨, 1995年生, 南昌大学材料科学与工程学院硕士研究生 e-mail: ywang0223@163.com
采用高温固相法在1 170 ℃还原气氛下保温3.5 h制备了(Ca1- xBa x)1.95SiO4:0.05Eu( x=0, 0.1, 0.3, 0.5, 0.6, 0.7, 0.8, 0.9, 1.0)系列新型荧光粉, 并研究了其基体晶相、 Eu离子价态、 光谱性能。 随着x值增大, 粉末物相组成发生如下改变: γ-Ca2SiO4( x=0)→T相和 γ-Ca2SiO4混合物(0≤ x<0.7)→T相(0.7≤ x<0.9)→Ba2SiO4相( x≥0.9), 即(Ca1- xBa x)2SiO4粉末只在富Ba端形成有限置换型固溶体, 即T相和Ba2SiO4相粉末。 点阵参数精确分析表明: 随着Ba离子增加, T相荧光粉(0.7≤ x<0.9) 处于M1, M2, M5点位碱土离子配位数增大进而晶格参数增大较为明显, 而Ba2SiO4相荧光粉( x≥0.9)中碱土离子配位数无变化晶格参数变化也较小; Eu离子以取代碱土离子方式进入晶格, 对晶格影响较小。 T相和Ba2SiO4相荧光粉XPS全谱分析结果类似, 均出现Ba(3 p3/2), Ba(3 d3/2), Ba(3 d5/2), O(1 s), Eu(4 d), Si(2 p3/2)电子结合特征峰; 其O(1 s)核心电子结合能精细谱也类似, 有2个光电子峰组成, 分别对应晶格氧、 间隙氧缺陷(Eu3+取代+2碱土离子造成); 进一步Eu(4 d)高分辨XPS分析表明, 随着 x值增大, T相粉末Eu2+/Eu3+比值增大(Eu离子形成+2可能性增大), 而Ba2SiO4相粉末Eu2+/Eu3+比值变化不明显。 在254和365 nm紫外激发下Ca1.95SiO4:0.05Eu( γ-Ca2SiO4相荧光粉)可用作红色荧光粉, 而(Ca1- xBa x)1.95SiO4:0.05Eu( x≥0.7, 即T相(其绿光宽谱发射峰中心在455 nm附近)或Ba2SiO4相荧光粉(其绿光宽谱发射峰中心在510 nm附近))可用作绿色荧光粉; T相荧光粉绿光发射比Ba2SiO4相荧光粉绿光发射对应波长更短; 随着 x值增加T相和Ba2SiO4相荧光粉发射光谱发生蓝移(即T相粉末中(Ca0.3Ba0.7)1.95SiO4:0.05Eu绿光发射波长最长, Ba2SiO4相粉末中(Ca0.1Ba0.9)1.95SiO4:0.05Eu 绿光发射波长最长); 随着 x值增加, T相荧光粉亮度提高, 而Ba2SiO4相荧光粉亮度降低, 即(Ca0.1Ba0.9)1.95SiO4:0.05Eu粉末的绿色荧光最亮(荧光寿命571.8 ns、 量子效率55%)。 由绿色荧光粉( x≥0.7)精细发射光谱可知: x值会影响Ba2SiO4相Eu2+占位倾向, x值越大Eu2+在Ba2SiO4相荧光粉中进入高配位点几率越小( x值小, Ca离子占据9配位点位, 有促进Eu离子倾向进入10配位作用), 但在T相中的 x值作用则不明显。 由此可见: 改变固溶度(即控制 x值), 可实现该系列荧光粉物相组成、 晶格参数、 离子价态、 荧光颜色及亮度的调控。
(Ca1- xBa x)1.95SiO4:0.05Eu ( x=0, 0.1, 0.3, 0.5, 0.6, 0.7, 0.8, 0.9, 1.0) new phosphor series were prepared by high temperature solid-state reaction at 1 170 ℃ under a reduction atmosphere for 3.5 hours in this paper. The matrix crystal structure, Eu ion valence, photoluminescence spectra and fluorescence lifetime and quantum efficiency had been investigated. The matrix phase constituents change as γ-Ca2SiO4 ( x=0)→T phase and γ-Ca2SiO4 mixture (0< x<0.7) →T phase (0.7≤ x<0.9)→Ba2SiO4(0.9≤ x≤1) as Ba ion content increasing. By XRD analysis, it is known that (Ca1- xBa x)2SiO4 powders form solid solution phases at the Ba-rich end, which are T-phase and Ba2SiO4-phase. Precision measurement of lattice parameters had been also done to T-phase (0.7≤ x<0.9) and Ba2SiO4 phase ( x≥0.9). For the former phase powder, the lattice parameters would increase because coordinated numbers for M1, M2, M5 sites are increasing as Ba ion content increasing, While, change from the latter one’s lattice parameters would be neglecting. Moreover, Eu ions enter into the crystal lattice by substituting for alkaline earth ions, with a minor impact. The surveys of X-ray photoelectron spectroscopy (XPS) spectra are similar, which all show characteristic electron binding energy peaks of Ba(3 p3/2), Ba(3 d3/2), Ba(3 d5/2), O(1 s), Eu(4 d) and Si(2 p3/2). The high-resolution spectrum of O(1 s) has two peaks, corresponding to lattice oxygen and interstitial oxygen defects (caused by Eu3+ substitution to alkaline earth ion+2), respectively. Moreover, the high-resolution XPS spectrums of the Eu(4 d5/2) shows that the Eu2+/Eu3+ ratio would increase as the increasing of Ba ions in the T-phase powders, while the Eu2+/Eu3+ ratio of Ba2SiO4-phase powders is not obviously changed. Ultraviolet photoluminescence photographs show that Ca1.95SiO4:0.05Eu ( γ-Ca2SiO4 phase phosphors) could be used as red phosphors, while (Ca1- xBa x)1.95SiO4:0.05Eu ( x≥0.7, T-phase (green emission centered at 455 nm) or Ba2SiO4-phase phosphors (green emission peak centered at 510 nm) could green phosphors. T-phase phosphors emission is blue shift comparing with Ba2SiO4 phase phosphor. Both T-phase and Ba2SiO4-phase phosphors are blue-shifted with the increase of x value. The brightest phosphor is (Ca0.1Ba0.9)1.95SiO4:0.05Eu (fluorescence lifetime 571.8 ns, quantum efficiency 55%, which is the shortest lifetime and highest efficiency among the green phosphors). The high-resolution photoluminescence emission spectra of green phosphor ( x≥0.7) show that that Eu2+ prefers more the site with 10 coordination than the site with 9 coordination as x value decreasing in Ba2SiO4-phase crystal (the Eu2+ activators with 10-coordination contribute more in green emission), but the site preference phenomenon is vague in the case of T-phase crystal. Overall, cation substitution (i. e. controlling the x value) should be a valid way to adjust the phase constituent, lattice, ion valence, photoluminescence CIE value and intensity for the phosphor.
稀土荧光粉是重要稀土产业之一[1, 2], 其中碱土硅酸盐系列因具有良好的热及化学稳定性、 原料广泛, 价格低廉备受关注。 通过调控碱土/硅离子配比, 其光学基体可为正(Me2SiO4)、 偏(MeSiO3)、 焦硅酸(Me3Si2O7), 在稀土掺杂后荧光发射波长、 激发波长、 荧光寿命调控范围极大。 近年来, 通过固溶取代[3](取代阴、 阳离子或离子团)调控基体物相设计开发新荧光粉成为研究热点之一, 如: Ba2SiO4:Eu2+绿色荧光粉其Ba离子被Ca、 Mg完全取代可得到红色荧光粉[4, 5]; M3MgSi2O8:Eu2+, Mn2+ (M=Ca, Sr, Ba)荧光粉调节M碱土离子种类及比例得到蓝色、 绿色、 乃至黄色的宽带发射荧光粉[6]。 硅酸钙盐涉及物相多(仅以正硅酸钙(Ca2SiO4)为例, 组分包含五种晶型[7]), 通常采用控制温度或碱土/硅离子配比来调控光学基体物相组成。 本文通过Ba部分取代Ca离子的方式来实现物相及发光性能调控, 并系统性讨论固溶对物相、 Eu离子价态、 光谱性能(激发和发射光谱、 寿命、 量子效率)的影响, 建立组分-结构-性能关联。
以BaCO3、 CaCO3、 SiO2(天津市大茂化学试剂厂, 分析纯)和Eu2O3(上海跃龙, 纯度为99.95 Wt%)为原料, 利用高温固相法合成(Ca1-xBax)1.95SiO4:0.05Eu系列荧光粉(x=0, 0.1, 0.3, 0.5, 0.6, 0.7, 0.8, 0.9, 1.0)。 其制备过程为: 按照化学计量比称量原料并混合, 并利用碳粉形成还原气氛(5 Wt%), 升温于1 170 ℃保温3.5 h, 随后随炉冷却, 研磨得到对应粉末样品。
采用PANalytical X射线衍射仪(Cu-Kα 源, 步长0.001° , 步宽0.001° , 每步滞留时间1 s)进行XRD(X-ray diffraction)分析。 利用ThermoFisher公司的K-Alpha(Al Kα 源, 0~1 486.6 eV)对样品进行XPS(X-ray photoelectron spectroscopy)测定。 选用PE公司的FS F-4500荧光光谱仪对样品进行PL(photoluminescence spectrum)测试。 并结合WFH-203B型三用紫外分析仪对样品的荧光发射进行观察, 同时数码相机记录254和365 nm激发下样品发光状态。 其量子效率(absolute PL quantum yields)和荧光寿命(lifetime)则应用Hamamatsu公司的C9920-02G量子效率测量仪测得。
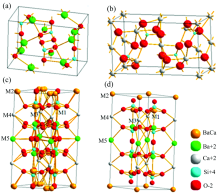
图1为(Ca1-xBax)2SiO4 (x=0, 0.1, 0.3, 0.5, 0.6, 0.7, 0.8, 0.9, 1.0)于1 170 ℃煅烧3.5 h得到粉末的物相分析结果。 当x=0时为γ -Ca2SiO4相[7][图2(b), 正交晶系, 空间群为Pbnm, a=5.082 Å , b=11.224 Å , c=6.764 Å , α =90° , β =90° , γ =90° , Ca2+的配位数为6], 0≤ x< 0.7时粉体为T相[8][图2(c), 5个碱土离子位置, 其中M1为Ba2+, Ca2+共享, Ba2+为10配位而Ca2+为9(或8)配位, M2为Ba2+, Ca2+共享, 均为10配位, M3为Ba2+配位数为10, M4为Ca2+配位数为6; M5为Ba2+配位数为10; Si有2个位置; O有5个位置]和γ -Ca2SiO4混合物; 0.7≤ x< 0.9时为T相, 随着Ba离子增加M1, M2, O1, O2和O3位点分裂减弱[8], 碱土离子位点M1, M2和M3配位数上升[如图2(d)所示, 当位点不分裂时, M1配位数为10, M2配位数为12, M3配位数为10]; 当0.9≤ x≤ 1时, 粉体为Ba2SiO4相[9][图2(a), 正交晶系, 空间群为Pnam, a=5.805 Å , b=10.214 Å , c=7.499 Å , Z=4, 碱土离子占据4c的2个位置, 配位数分别为10和9, 并分别沿c轴和b轴与硅氧四面体形成链状]。 由物相分析可知, (Ca1-xBax)2SiO4粉末只在富Ba端形成有限置换型固溶体, 即T相和Ba2SiO4相粉末。
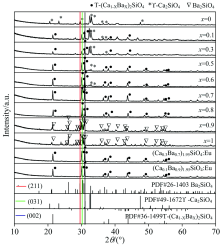 | 图1 (Ca1-xBax)2SiO4和(Ca1-xBax)1.95SiO4:0.05Eu粉末XRD图Fig.1 XRD patterns of (Ca1-xBax)2SiO4 and (Ca1-xBax)1.95SiO4:0.05 Eu (x=0~1, carbon powder 5 Wt%, 1 170 ℃ for 3.5 hours) |
利用晶格参数计算和衍射峰半峰宽(full width at half maxima, FWHM)进一步研究Ba离子含量(即x值)对单相粉末结构的影响(表1)。 Ba2SiO4相粉末(Ca1-xBax)2SiO4, x≥ 0.9) 中, x=0.9与x=1相比, 其晶格参数减小(依据(211)(031)(002)衍射面数据由dhkl=
| 表1 (Ca1-xBax)2SiO4和(Ca1-xBax)1.95SiO4:0.05Eu粉末的结构参数 Table 1 Cell parameters of (Ca1-xBax)2SiO4 and (Ca1-xBax)1.95SiO4:0.05Eu (carbon powder 5 Wt%, 1 170 ℃ for 3.5 hours) |
由图1和表1还可见Eu离子以取代碱土离子方式进入晶格, 掺杂后对(Ca1-xBax)2SiO4(x≥ 0.7)的物相组成无影响。 按照(Ca1-xBax)2SiO4(x≥ 0.7)的合成条件, 得到(Ca1-xBax)1.95SiO4:0.05Eu(x≥ 0.7)粉末。
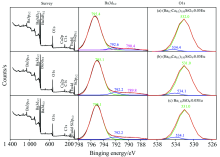
(Ca1-xBax)1.95SiO4:0.05Eu(x≥ 0.7)的XPS全谱及Ba, O核心电子结合能精细谱(经Shirley去除背底和高斯线性拟合[10])如图3所示。 Ba1.95SiO4:0.05Eu的XPS全谱中可见[x=1, 图3(c)]Ba(3p3/2), Ba(3d3/2), Ba(3d5/2), O(1s), Eu(4d), Si(2p3/2)峰(分别对应1 062, 795, 780, 532, 135和91 eV结合能); Ba(3d3/2)能级精细谱则可见2个结合能峰(795.4, 792.6 eV), 分别对应Ba在晶格中10配位和9配位置[11]; O(1s)能级精细谱也有2个光电子峰组成, 低结合能峰(约531.0 eV)对应晶格氧, 高结合能峰(约534.1 eV)对应氧缺陷(当Eu以+3进入晶格, 取代Ba2+, 产生间隙氧缺陷)。 (Ca0.1Ba0.9)1.95SiO4:0.05Eu的XPS全谱及Ba, O核心电子结合能精细谱[x=0.9, 图3(b)]与Ba1.95SiO4:0.05Eu分析结果相似, 但全谱中新增Ca(2p)(348 eV)峰, 且在Ba(3d3/2)精细谱中出现第3峰(Ca离子固溶在Ba2SiO4相引入的晶格畸变所致)。 而(Ba0.7Ca0.3)1.95SiO4:0.05Eu 的全谱及Ba, O核心电子结合能精细谱与Ba1.95SiO4:0.05Eu分析结果也相似[x=0.7, 图3(a)], 但也新增Ca(2p)结合峰, 且Ba(3d3/2)精细谱中3个结合峰, 分别对应10配位(M1, M2, M3)、 8配位(M5)位置、 Ca离子分享M1和M2所导致的微扰(Ca在M1和M2时配位数分别为8或9配位)[12]。
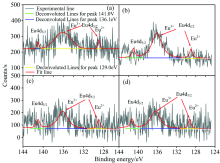
图4为(Ca1-xBax)1.95SiO4:0.05Eu(x≥ 0.7)Eu4d精细谱。 文献[13]报道Eu3+的4d5/2和4d3/2的光电子峰分别位于约135.0 eV和约140.5 eV处, 自旋轨道劈裂约为5.5 eV; 而Eu2+的4d5/2的结合能要比相应的Eu3+低约7 eV; 4个样品均存在3个电子峰, 即Eu3+的4d3/2和4d5/2分别对应141.0和136.1 eV(结合能的能差为4.9 eV); Eu2+的Eu(4d5/2)则对应129.0 eV, Eu2+和Eu3+的4d5/2的结合能相差7.1 eV, 与文献报道Eu4d精细谱基本一致。 Eu2+/Eu3+的4d5/2的光电子峰的积分强度比值在x=0.7[图4(a)]、 0.8[图4(b)]、 0.9[图4(c)]、 1[图4(d)]时分别为0.068, 0.197, 0.221和0.222。 结合2.1节结构分析可知, 随着Ba离子增加, T相粉末(0.7≤ x< 0.9)中处于M1, M2, M5点位配位数增大, 晶格参数明显增大, Eu离子形成+2可能性增大(0.8比0.7比值增加了89.7%); 而Ba2SiO4相粉末(0.9≤ x≤ 1), 碱土离子配位数没有明显改变, 晶格参数变化不明显, Eu离子形成二价几率不变(1比0.9比值增加了0.4%)。
2.3.1 紫外激发发光照相记录
图5为(Ca1-xBax)1.95SiO4:0.05Eu(从左至右x=0~1)紫外发光照相记录。 随x值增大, 254 nm紫外激发下(Ca1-xBax)1.95SiO4:0.05Eu依次呈现深红色、 红色、 浅红色、 粉红色、 淡蓝色、 蓝绿色、 绿色、 淡绿色的荧光; 365 nm的紫外激发下(Ca1-xBax)1.95SiO4:0.05Eu依次呈紫色、 粉紫色、 淡粉紫色、 淡蓝色、 亮蓝色、 蓝绿色、 绿色、 淡绿色的荧光。 由此可见, 254 nm激发下当x≥ 0.7表现为绿光发射; 而在365 nm激发下时x≥ 0.3时表现为绿光发射; 且两种激发条件下(Ca0.1Ba0.9)1.95SiO4:0.05Eu粉末最亮。 结合2.1结构分析结果可知, 紫外激发下Ca1.95SiO4:0.05Eu(γ -Ca2SiO4相荧光粉)可用作红色荧光粉而(Ca1-xBax)1.95SiO4:0.05Eu(x≥ 0.7, 即T相或Ba2SiO4相荧光粉)可用作绿色荧光粉。
 | 图5 (Ca1-xBax)1.95SiO4:0.05Eu紫外激发发光照相记录Fig.5 Photos of (Ca1-xBax)1.95SiO4:0.05Eu under UV light excitation (x=0~1, carbon powder 5 Wt%, 1 170 ℃for 3.5 hours) |
2.3.2 激发和发射谱
Ba2SiO4相荧光粉, 当x=1时(Ba1.95SiO4:0.05Eu)365 nm激发绿光峰的中心位置为511 nm[图6(d)], 而254 nm激发绿光发射中心为513 nm, 对应Eu2+的4fn-15d→ 4fn电子跃迁[图6(c)]; 以510 nm为监视波长测的Ba1.95SiO4:0.05Eu激发谱落在200~450 nm间, 其对应电荷转移吸收跃迁(charge transfer band, CTB), 在415 nm处有小锐锋则对应Eu3+的7F0→ 5L6跃迁[图6(b)]; 采用415 nm激发荧光发射谱与365 nm情况类似, 但整体强度略弱[图6(e)]。 当x=0.9发射谱和激发谱与x=1类似, 但绿光发射谱强度略大且发射峰红移(365 nm激发绿光发射峰中心为512 nm, 而254 nm激发峰中心为515 nm)。 T相荧光粉末(x=0.8, 0.7) 发射谱与Ba2SiO4相荧光粉(x=1, 0.9)相比, 绿色发射略弱且发射峰略微蓝移(365和254 nm激发下主峰位置在454和455 nm附近), 且存在微弱的红光发射(对应Eu3+的5D0→ 7F1跃迁, 612 nm对应Eu3+的5D0→ 7F2跃迁); T相荧光粉末415 nm激发发射谱与Ba2SiO4相荧光粉类似。 混合物相荧光粉(γ -Ca2SiO4和T相混合物, x≤ 0.7)随着Ba减少(x减小)其红色荧光发射渐强而绿光渐弱。
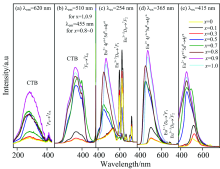 | 图6 (Ca1-xBax)1.95SiO4:0.05Eu光谱图Fig.6 Photoluminescent spectra of (Ca1-xBax)1.95SiO4:0.05Eu(x=0~1, carbon powder 5 Wt%, 1 170 ℃ for 3.5 hours) |
由VanUitert公式[14]E(cm-1)=Q*
由精细光谱图7和表2可知: T相荧光粉比Ba2SiO4相荧光粉发射峰整体蓝移[与图6(c)和(d)发射光谱一致]; 且T相和Ba2SiO4相荧光粉均随着Ba离子增加光谱蓝移(通常伴随配位晶体场效应减弱伴随光谱蓝移), 结合2.1节结构分析可知T相因为M1, M2和M5配位数增加, 而Ba2SiO4相则晶格参数的增大使得配位晶体场减弱)。 随着Ba离子增加, T相两个峰积分面积比值变化不大(x=0.7比x=0.8减小了 0.89% )而Ba2SiO4相峰积分面积比值减小(5.43%), 这意味着固溶度会影响Ba2SiO4相Eu2+占位倾向(Ca离子固溶促进Eu离子进入10配位位置)但在T相中则不会。
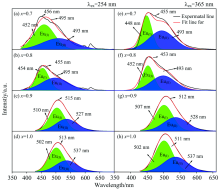 | 图7 (Ca1-xBax)1.95SiO4:0.05Eu绿光发射精细谱Fig.7 High-resolution emission spectrum of green (Ca1-xBax) 1.95SiO4:0.05Eu phosphors (carbon powder 5 Wt%, 1 170 ℃ for 3.5 hours) |
| 表2 (Ca1-xBax)1.95SiO4:0.05Eu 精细发射谱 Table 2 Data of (Ca1-xBax)1.95SiO4:0.05Eu high-resolution emission spectrum (Carbon powder 5 Wt%, 1 170 ℃ for 3.5 hours) |
2.3.3 荧光寿命和量子效率
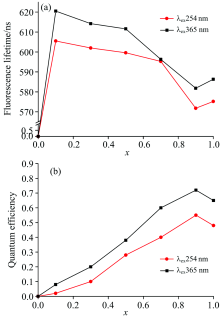
(Ca1-xBax)1.95SiO4:0.05Eu(x=0~1)荧光粉的绿色荧光寿命及量子效率如图8所示。 254 nm激发下绿色荧光寿命分别为0, 605.5, 602.0, 599.6, 595.3, 571.8和575.2 ns[图8(a)], 且对应的量子效率分别为0, 0.02, 0.10, 0.28, 0.40, 0.55和0.48[图8(b)]。 365 nm激发下荧光寿命依次为0, 620.5, 614.2, 611.6, 596.3, 581.8和586.3 ns[图8(a)], 且对应的量子效率分别为0, 0.08, 0.20, 0.38, 0.60, 0.72和0.65[图8(b)]。 由此可见: 紫外激发下(Ca0.1Ba0.9)2SiO4:Eu为最佳绿色荧光粉, 在254 nm (365 nm)激发下绿光荧光寿命571.8 ns (581.8 ns), 量子效率为0.55 (0.72)。
采用高温固相法在1 170 ℃碳的还原气氛下保温3.5 h得到(Ca1-xBax)1.95SiO4:0.05Eu(x=0~1) 系列荧光粉。 物相分析表明当x=0时物相为单一的γ -Ca2SiO4; 当0< x< 0.7时, 粉体为T相和γ -Ca2SiO4的混合相; 当0.7≤ x< 0.9时粉体为T相; 当0.9≤ x≤ 1时粉体为Ba2SiO4相; 即在富钡端荧光粉为固溶相。 Ba离子增加使得T相荧光粉碱土离子配位和晶格参数增大, 对Ba2SiO4相荧光粉碱土离子配位数无影响且对晶格参数影响也较小。 结合T相和Ba2SiO4相粉末的Eu4d高分辨XPS可知Ba离子增加促进T相Eu2+/Eu3+比值增大但对Ba2SiO4相影响不明显。 紫外激发下Ca1.95SiO4:0.05Eu(γ -Ca2SiO4相荧光粉)可用作红色荧光粉而(Ca1-xBax)1.95SiO4:0.05Eu(x≥ 0.7, 即T相或Ba2SiO4相荧光粉)可用作绿色荧光粉, 且(Ca0.1Ba0.9)2SiO4:Eu为最亮绿光荧光粉[其荧光寿命为571.8 ns (581.8 ns), 量子效率为0.55 (0.72)]结合T相和Ba2SiO4相精细发射谱可知, 紫外激发下T相比Ba2SiO4相荧光粉发射谱蓝移; 随着Ba离子增加, T相比Ba2SiO4相荧光粉发射谱蓝移, 且Ba离子浓度会影响Ba2SiO4相Eu2+占位倾向(Ca离子占据9配位, 当Ca离子较多Eu离子倾向进入10配位置)但在T相作用则不明显。
通过调控(Ca1-xBax)1.95SiO4:0.05Eu中Ba离子含量, 粉末物相组成可由混合相变为单相粉末, 在紫外激发下由红色荧光粉转变为绿色荧光粉(其绿光发射峰中心可为455 nm(T相荧光)或510 nm(Ba2SiO4相), 荧光寿命在570~620 ns, 量子效率在0~72%)T相粉中Ba离子促进二价Eu离子形成, 因而荧光亮度随着Ba含量增加而增大; 而Ba2SiO4相中Ca离子促使E
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|