作者简介: 宋 晨, 1986年生, 中国中医科学院中药研究所博士后 e-mail: sc01105023@126.com
中医临床常用生石膏(CaSO4·2H2O)治疗发热疾病, 通过对石膏显微晶体特征和微量元素特征的研究, 提出了微量元素锶(Sr)是石膏降温重要影响元素的假说。 实验通过偏光显微镜(optical polarized light microscopy, OPLM)、 X射线衍射(X-ray diffraction, XRD)、 电子探针微区分析(electron probe microanalysis, EPMA), 电感耦合等离子体质谱(inductively coupled plasma mass spectrometry, ICP-MS)等方法分析了来自五个产地33批石膏药材的显微晶体结构和微量元素组成。 OPLM分析结果显示: 石膏的显微晶体形态主要为长柱状和纤维状, 且和石膏的产地密切相关。 按传统要求认为品质好的样品, 其显微颗粒较大。 XRD分析结果显示: 除1批样品含有石英杂质, 其余样品在XRD下均未见其他矿物杂质。 EPMA分析结果显示: 石膏样品中主要矿物为石膏, 次要矿物为硬石膏, 两者呈现共生关系。 微区图像中的硬石膏矿物没有确定的晶形, 硬石膏和石膏的接触面都是不规则状曲线, 推测样品中包含的硬石膏不是原生的硬石膏, 而是石膏矿物在成矿后期转化而来。 ICP-MS分析结果显示: 微量元素锶(Sr)在石膏中含量较高, 是所有微量元素中绝对含量最高的, 与原始地幔中微量元素含量的对比结果显示, Sr元素在石膏样品中是最为稳定富集的微量元素, 它比原始地幔富集6倍以上, 最高到176倍。 石膏微区点位的CaO/SrO分析结果显示锶(Sr)元素在石膏中呈统计式均匀分布, 在石膏中主要以类质同象混入物的形式存在。 在随后进行的石膏水溶液中Sr元素含量测定的结果显示, 锶(Sr)在石膏煎煮液及石膏混悬液中的溶出量达到了理论值的2~4倍。 临床上大剂量使用石膏并先煎的方法, 可以促进Sr2+的溶出。 因为Sr2+具有抑制Na+的作用, 据此提出石膏降温的假说: 应用石膏降温时, Sr2+和Ca2+同时溶出, Sr2+抑制机体对Na+的吸收, 同时增加对机体Ca2+的供给, 共同调节发热的正调节介质Na+/Ca2+的比值, 石膏降温的物质基础是Sr元素和Ca元素共同的作用。
Clinical Chinese Medicine commonly used gypsum (CaSO4·2H2O) to treat febrile diseases. Based on the study of microscopic crystal characteristics and trace element characteristics of gypsum, the hypothesis that trace element strontium (Sr) is an important influential element for gypsum cooling is proposed. We analyzed the microscopic crystal structure and trace element composition of 33 batches of gypsum herbs from five producing areas by optical polarized light microscopy (OPLM), X-ray diffraction (XRD), electron probe micro-analysis (EPMA) and inductively coupled plasma mass spectrometry (ICP-MS). The results of OPLM analysis show that the microscopic morphology of gypsum is mainly long columnar and fibrous, and is related to the original area of gypsum. According to the traditional requirements, the samples with good quality have larger micro-particles. XRD analysis showed that except for one batch of samples containing quartz impurities, the other samples showed no other mineral impurities. The results of EPMA analysis showed that the main mineral in the gypsum sample was gypsum and the secondary mineral was anhydrite, which showed a symbiotic relationship. The anhydrite in the micro-area image has no definite crystal form, and the contact surfaces of anhydrite and gypsum are irregular curves. It is speculated that the anhydrite is converted from the gypsumin the later stage of mineralization rather than native. The results of ICP-MS analysis showed that the trace element strontium (Sr) was higher in gypsum, and the highest absolute content of all trace elements. The comparison with trace elements in the primitive mantle showed that the Sr element is the most stable and enriched trace element in the gypsum sample, which is more than 6 times more than the primitive mantle, up to 176 times. The analysis of the value of CaO/SrO in the micro-site of gypsum shows that the strontium (Sr) element is statistically uniformly distributed in the gypsum and exists mainly in the form of isomorphic mixtures in gypsum. The results of the determination of the Sr element content in the aqueous gypsum solution showed that the dissolution amount of strontium (Sr) in the gypsum decocted fluid and the gypsum suspension reached 2~4 times of the theoretical value. Gypsum was used in large doses in the clinic, and decocted first can promote the dissolution of Sr2+. Because Sr has the effect of inhibiting Na. The hypothesis of gypsum cooling: when gypsum is used for cooling, Sr2+ and Ca2+ are simultaneously dissolved. Sr2+ inhibits the absorption of Na+ to the body, increases the supply of Ca2+ to the body, and regulates the ratio of Na+/Ca2+ one of the positive regulation medium of fever. The material basis for the cooling of gypsum is the joint action of Sr and Ca.
生石膏(CaSO4·2H2O)是一味常用的矿物类中药, 在临床上主要用于治疗跟发热相关的疾病。 以石膏为主药可以配伍形成多个经方, 如白虎汤、 竹叶石膏汤和麻杏石甘汤等, 在长期的临床应用中降温效果显著。 石膏降温的物质基础和机理近百年来一直在探索之中, 张锡纯在《医学衷中参西录》中认为石膏中的硫和氧是石膏解热的物质基础[1]。 近几十年来, 石膏解热物质基础研究方面的文献有很多。 郭协埙提出天然石膏在动物实验上有退热作用, 而纯粹石膏则无退热现象, 并推测石膏退热有效成份是天然石膏内所含的杂质, 其退热机制尚未明确[2]。 夏怡等也证明了用纯的CaSO4·2H2O代替白虎汤中的石膏, 则白虎汤失去降温效果[3], 认为石膏含有的微量元素是石膏解热的可能物质基础。 李轩贞对不同产地的石膏中Mg, Fe, Mn, Cu进行了比较[4], 王焕第等、 王薇等和田腾跃等分别对比了15种、 23种和32种微量元素[5, 6, 7]。 刘元芬讨论了石膏炮制前后的微量元素含量变化, 发现炮制后只有Sr的含量相对增加, 其余各地石膏的微量元素含量均不同程度下降[8]。 孙姝和周灏分析了石膏微量元素和石膏解热之间的联系, 得出石膏退热作用的物质基础是多种微量元素共同作用的结果[9, 10]。 前人虽然做了很多工作, 但迄今为止尚未得出关于石膏解热物质基础的可靠科学假说。
石膏降温物质基础研究的前提是石膏的矿物组成和元素分布, 工作中采集了药用石膏药材, 运用偏光显微镜、 X射线衍射仪、 电子探针显微分析仪和电感耦合等离子体质谱仪四种仪器详细分析了石膏的显微特征, 宏观和微观矿物组成, 主量元素和微量元素, 通过测试结果弄清石膏的矿物组成和元素分布特点, 并进一步提出了石膏解热物质基础的假说。
偏光显微镜: ZEISS公司, 型号AxioScope.A1。
X射线粉晶衍射: 德国布鲁克公司, 型号D8 Advance。 工作参数: Cu靶, 扫描范围: 10° ~70° , 步长0.02° , 工作电压40 kV, 工作电流40 mA。 采用布鲁克公司EVA软件对样品的XRD原始数据进行标准化处理, 并将所得衍射数据与国际标准X射线衍射数据卡片进行匹配。
电子探针: 日本电子株式会社, 型号JXA-8230。 工作参数: 工作电压为15 kV, 电子束流值为5×10-9 A, 束斑直径选择30 μm。
电感耦合等离子体质谱: 美国赛默飞公司, 型号Thermo X Series 2。 RF功率1 300 W, 扫描方式跳峰, 冷却气流量15 L·min-1, 辅助气流量1.2 L·min-1, 采样锥孔径1.1 mm, 截取锥孔径0.9 mm。
实验采集了33批石膏药材(每个批次选一个典型样品), 分别为: 湖北应城13批; 湖北荆门6批(包括龙源和长兴); 山东平邑9批; 山东泰安3批; 四川眉山2批。 样品形态包括块状石膏和纤维石膏, 其中块状石膏4批, 纤维石膏29批。 颜色包括白色, 淡黄色和淡红色, 其中白色样品18批, 淡黄色样品10批, 淡红色样品5批。 本次石膏样品中有16批是半透明, 17批不透明, 没有发现透明的透石膏。 产地采集石膏样品统计结果显示石膏样品大多数都是纤维石膏, 颜色以白色为主, 不透明和半透明的样品批次相当。 详细样品采集情况见表1。
| 表1 石膏产地, 颜色, 透明度和形态信息表 Table 1 Gypsum producing area, color, transparency and shape information table |
偏光显微镜: 将样品制成30 μm的永久薄片, 置于偏光显微镜上进行单偏光和正交偏光的观察。
X射线粉晶衍射: 将石膏样品在玛瑙研钵中研成粉末状(160~200目), 置样品池中, 表面压平, 进行检测。
电子探针: 将样品制成45 μm的永久厚片, 然后在表面上镀碳粉, 置于样品池中进行分析。
电感耦合等离子体质谱: 取样品50 mg, 按照中华人民共和国国家标准GB/T14506.30—2010进行样品制备。
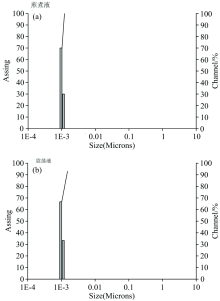
石膏的煎出液制备: 选用山东省的石膏6批, 粉碎筛析, 选取粒径在200目(75 μm)~500目(25 μm)之间的粉末用于实验, 生石膏:高纯水按20 g:100 mL煎煮30 min, 煎液10 000 r·min-1离心后, 过0.22 μm滤膜, 用激光粒径检测, 与纯水进行对比, 确认不存在微粒(图1)。
石膏的震荡液制备: 选用山东省的石膏6批, 粉碎筛析, 选取粒径在200目(75 μm)~500目(25 μm)之间的粉末用于实验, 生石膏:高纯水按20 g:100 mL震荡30 min, 10 000 r·min-1离心后, 过0.22 μm滤膜, 用激光粒径检测, 与纯水进行对比, 确认不存在微粒(图1)。
通过对33批石膏的镜下观察, 统计显微镜下石膏的形态、 大小、 解理、 消光类型和最高干涉色。 镜下显微形态以长柱状为主(18批), 其余为纤维状(9批)和粒状(6批), 其中鳞片状作为次要显微形态出现在4批中。 样品中纤维状和长柱状宽度在0.005~0.4 mm之间。 粒状颗粒大小在0.01 mm×0.01 mm~0.3 mm×0.8 mm之间。 一组解理在12批样品中出现, 其余21批都未出现解理。 消光类型是斜/平行消光13批, 斜消光17批, 平行消光2批, 仅1批单独出现波状消光。
石膏的微观颗粒形态与石膏的产地相关: 山东平邑石膏以纤维状为主[图2(a)], 偶见长柱状和粒状; 山东泰安石膏均为粒状见图2(d); 湖北应城, 湖北荆门龙源矿[图2(c)]的石膏都是长柱状[图2(b)]; 四川眉山一批为长柱状, 一批为粒状; 湖北荆门长兴的石膏都为纤维状。 石膏的显微形态和地质过程息息相关, 不同的地质过程可以改变石膏微观颗粒的大小与形态。
传统上, 石膏以色白、 半透明、 纵断面纤维状、 具丝绢样光泽、 无杂质者为佳。 四川眉山和湖北荆门龙源矿的石膏都是白色半透明纤维状石膏, 具有丝绢光泽, 没有其他杂质, 符合上述传统认为的优质石膏标准。 在微观颗粒大小上, 四川眉山[图2(f)]和湖北荆门龙源矿[图2(c)]的石膏微观颗粒大小明显大于其他产地的石膏。 推测石膏的品质和石膏显微颗粒大小相关, 品质优良者, 微观颗粒较大。
本次实验共分析五个产地石膏样品。 图3(a, b)分别是五个产地石膏的X射线衍射谱和眉山-1, 应城2-4的物相分析。 经过全谱拟合, 30批产地药材的物相均为单一物CaSO4·2H2O(卡片号01-074-1433), 无其他物相; 应城2-4样品主要物相为CaSO4·2H2O, 次要物相为SiO2(卡片号01-079-1906)。 这些样品之间角度值和峰强都比较一致。 结果显示除了1批样品含有石英杂质, 其余样品在XRD下均未见其他矿物杂质, 说明纯度较高。
实验电子探针中共计打点56个, 涉及到石膏药材10个批次。 电子探针打点的结果为38个点是石膏, 16个点是硬石膏, 还有2个点是加拿大树胶(制片粘合剂)。 在以往的电子探针微区分析中石膏和硬石膏的电子探针分析结果都显示为CaSO4。 这是因为由于电子探针的电子束能量太高打到矿物表面时会灼烧矿物, 而石膏的晶体结构不是很稳定, 所以会在分析过程中失去两个水分子变成硬石膏。 解决这个问题的方法就是需要降低电子探针加速电压(实验由30 kV降为15 kV)和电子束电流的强度(实验由3×10-8 A降为5×10-9 A)和扩大电子束束斑的直径大小(5 μm增至30 μm)。
电子探针实验结果显示, 在石膏的样品中主要矿物为石膏, 次要矿物为硬石膏。 石膏和硬石膏呈现共生关系。 未发现除石膏和硬石膏之外的矿物。 发现的硬石膏矿物没有确定的晶形, 硬石膏和石膏的接触面都是不规则状曲线, 推测硬石膏是后期石膏转化而来, 而不是原生的硬石膏。 薄片中个别危区出现硬石膏较多, 形成了硬石膏包裹石膏的现象。
图4是龙源-1样品的背散射电子影像图。 图中清晰的显示在微观尺度上, 硬石膏和石膏是共生矿物。 其中灰色矿物是石膏, 灰白色矿物是硬石膏, 形成了硬石膏包裹石膏的局部现象。 在自然界中生成硬石膏有两种模式。 一是Sabkha环境下在非常早期的蒸发岩成岩的岩石间隙中形成, 二是在硫酸钙蒸发岩地层深埋的过程中由石膏转化为硬石膏[11]。 图中硬石膏和石膏的接触均为不规则状曲线, 推测此硬石膏为石膏形成后转化而来, 在图示的局部区域石膏较多, 呈现硬石膏包裹石膏的现象。
 | 图4 龙源-1 BSE图 1, 2, 3: 石膏; 4, 5, 6, 7, 8: 硬石膏Fig.4 Longyuan-1 BSE diagram 1, 2, 3: Gypsum; 4, 5, 6, 7, 8: Anhydrite |
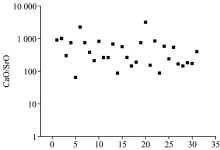
元素在矿物中存在的状态主要有两种, 类质同象和独立矿物态。 当独立矿物颗粒比较大时, 可以通过肉眼或者显微镜直接观察到这些矿物, 但如果其矿物颗粒小到超显微时, 就只能用一些特殊的仪器进行测量分析。 其中电子探针分析就可以探测确认微量元素在矿物中的存在形态。 选取所有含SrO的探针点, 计算CaO/SrO的值(图5)。 结果显示SrO在石膏中呈统计式均匀分布, 且并不存在为零或者非常小的值, 说明SrO未形成独立矿物, 在石膏中主要以类质同象混入物的形式存在。 这种现象的形成主要是由于Sr2+半径(1.13 Å )和Ca2+(0.99 Å )的离子半径较接近, 在石膏形成的过程中, Sr原子会替代晶格中的Ca原子。
共测试了五个产地33批石膏药材样品的微量元素, 6个石膏煎出液和6个石膏震荡液样品。 每批样品测试31个元素。 由于微量元素含量彼此之间数量级相差较大, 且存在奇偶性(原子序数为偶数的元素丰度远远大于相邻原子序数为奇数的元素丰度)。 为了消除这种效应, 把原始地幔(代表初始化的地球)作为微量元素的标准, 将石膏中的微量元素含量和原始地幔的微量元素含量做对比, 可推测出石膏在形成过程中富集了哪些元素。
图6是五个产地采集的部分石膏药材的原始地幔标准化图, 显示石膏整体相对于原始地幔元素而言是亏损的。 石膏相对于原始地幔富集Sr, W, As元素, 其中Sr元素的富集可达到6倍以上, 最高富集176倍。 部分石膏富集Sb, Tl, Pb, Bi, Cs, Ba元素, 其余相对原始地幔都亏损的元素为Li, Be, Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Ga, Rb, Nb, Mo, Cd, In, Ta, Th, U, Hg。
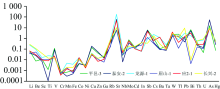 | 图6 五个产地石膏药材微量元素配分模式图(标准化原始地幔数据来自Mcdonough & Sun, 1995)[12]Fig.6 Primitive mantle-normalized multi-element patterns of gypsumin five producing areas (standardized primitive mantle data from Mcdonough & Sun, 1995)[12] |
五个产地石膏的配分模式大致上一样, 个别元素略有不同。 比如平邑, 泰安和应城富集Bi元素, 而眉山, 荆门都亏损Bi元素。 这种现象说明各地石膏的成因都相似, 个别元素的不同与当地成矿条件有关。
图7是石膏煎煮和直接震荡后的水溶液原始地幔标准化图, 其中红色代表的是石膏煎煮的水溶液, 而蓝色则是石膏震荡水溶液。 从图7可以看出煎煮和常温震荡对石膏中微量元素的溶出影响基本一致。 在煎煮液中Sr和Pb元素的溶出要高于室温震荡, 其中Pb元素高出7~110倍, Sr元素高出21.1%~76.6%, 与石膏水溶液中的含量和石膏中的含量密切相关。
 | 图7 采集山东石膏水溶液微量元素配分模式图(标准化原始地幔数据来自Mcdonough & Sun, 1995)[12]Fig.7 Primitive mantle-normalized multi-element patterns of gypsum aqueous solution from Shandong Province (standardized primitive mantle data from Mcdonough & Sun, 1995)[12] |
石膏(CaSO4·2H2O)在水中的溶出一直是研究石膏关注的问题。 根据最新的文献研究表明石膏在水中25 ℃的溶解度为0.014 7~0.018 2 mol·L-1, 100 ℃时溶解度0.012 5~0.016 25 mol·-1[13]。 石膏的化学式为CaSO4·2H2O, 相对原子质量为172.112, 溶解度换算后为2.53~3.13 g·L-1(25 ℃), 2.15~2.80 g·L-1(100 ℃)。 理论上处理后的石膏水溶液中Ca2+的含量为589~729 mg·L-1, 实际的测试结果为616 mg·L-1(平均)。 测试结果和理论基本相符合。
由于石膏水溶液是CaSO4·2H2O饱和溶液, 根据溶解度和石膏矿石中Sr的含量可计算出水溶液中溶出的理论Sr含量。 平邑-4为136.22 μg·g-1, 泰安-1为1 242.38 μg·g-1。 平邑-4理论上处理后的石膏水溶液中Sr的含量为344.64~426.37 μg·L-1, 但实际测量结果为693 μg·L-1(浸泡, 震荡), 1 223 μg·L-1(煎煮后), 泰安-1理论上处理后的石膏水溶液中Sr的含量是3 143.22~3 888.65 μg·L-1, 但实际测量结果为7 045 μg·L-1(浸泡, 震荡), 8 532 μg·L-1(煎煮后), Sr的实际溶出是理论值的2~4倍。 分析认为溶解是一个动态平衡, 当Ca2+饱和时, Sr2+仍然持续溶出。 临床大剂量应用石膏, 并要求石膏先煎, 增加原始药物数量和煎煮时间, 这两者都会促进Sr2+的溶出。
Sr元素是人体内必需的一种微量元素, 与人体骨骼的发育、 心血管的功能与结构以及神经和肌肉的兴奋等息息相关, 在人体中具有重要作用。 Sr与血管的功能及构造有着千丝万缕的关系, 其作用机制是在肠内与钠竞争吸收部位, 从而减少人体对钠的吸收, 增加钠的排泄, 以此来预防心血管疾病的病发率和减少心血管疾病的死亡率[14]。 在发热的正调节介质中, Na+/Ca2+比值是其中之一。 升高Ca2+, 降低Na+会使体温降低。
(1) 偏光显微镜观察结果显示石膏显微晶体形态主要为长柱状和纤维状, 且和石膏的产地密切相关。 石膏品质好的样品, 其显微颗粒较大。
(2) 电子探针显示在石膏矿物的微区中含有极微量的硬石膏。 XRD显示硬石膏的含量都在检测限之下, 说明它在石膏中的含量非常少。 CaO/SrO的值说明SrO未形成独立矿物, 在石膏中主要以类质同象混入物的形式存在。
(3) 电感耦合等离子体质谱测试的结果证实Sr是最为稳定富集的微量元素, 且临床大量使用石膏并先煎能大幅促进Sr2+的溶出。 在发热的正调节介质中, Na+/Ca2+比值是其中之一。 升高Ca2+, 降低Na+会使体温降低。
据以上三点提出石膏降温的假说: 在发热过程中, Sr2+通过和Ca2+相似的特性, 抑制Na+, 调节发热的正调节介质Na+/Ca2+的比值, 和Ca2+共同降温。
石膏降温的物质基础是Sr元素和Ca元素共同的作用。
致谢: 感谢XRD的测试单位清华大学物理实验室和尉京志老师, 电子探针的测试单位北京科技大学的钢铁冶金新技术国家重点实验室和左小剑老师, LA-ICP-MS的测试单位河北省廊坊市区域地质矿产调查研究所。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|