作者简介: 张 浪, 女, 1989年生, 国防科技大学空天科学学院工程师 e-mail: 383795240@qq.com
激发态粒子是化学反应过程的天然示踪剂, 当前激发态粒子研究主要都是在一维简单火焰下进行。 为了考察复杂情况下激发态分布对化学反应热的定量表征规律, 进行了甲烷/空气同轴射流扩散火焰的试验, 开展了甲烷/空气详细燃烧机理与激发态燃烧机理的同轴射流预混火焰和扩散火焰的数值模拟, 分析了OH*和CH*的分布特性, 研究了激发态对反应热的表征关系。 结果表明: 通过试验ICCD相机和相应滤光片获取的OH*和CH*的化学发光图像和数值模拟中OH*和CH*摩尔分数分布的模拟结果吻合, OH*分布主要分为三个燃烧区域, CH*分布主要为两个燃烧区域。 扩散火焰中OH*和CH*分布呈现单峰, 反应热呈现双峰现象, 反应热与激发态变化趋势相似, 达到第一峰值后激发态逐渐减小为零, 而反应热达到第一峰值后先降低再缓慢上升到第二峰值, 最后减小至零。 扩散火焰中沿轴向方向, 当C2H+O=CH*+CO(R12)反应速率达到峰值时, 反应热达到第一波峰; H+O+M=OH*+M(R2)反应速率达到峰值时, 反应热达到第二波峰。 预混火焰中随着局部当量比的增加, OH*和CH*的摩尔分数明显增大, 分布区域更广; 反应热和激发态粒子OH*和CH*的分布趋势一样, 在激发态粒子OH*和CH*质量分数增大时, 反应热也增大, 当激发态粒子OH*和CH*的质量分数达到峰值的时候, 反应热也达到峰值; 沿轴向方向, OH*和CH*的四个生成反应速率的峰值都在同一位置, 反应热也达到最大值, CH+O2=OH*+CO(R1)和C2H+O=CH*+CO(R12)反应速率相比H+O+M=OH*+M(R2)和C2H+O2=CH*+CO2(R11)反应速率更快。
Excited particle is a natural tracer of the chemical reaction process, but the research on the excited particle is mainly carried out under simple one-dimensional flame. In order to investigate the distributions excited state under complex conditions of chemical reaction heat quantitative characterization of rule, the methane/air coaxial jet diffusion flame test has carried out detailed ground state and excited of methane/air premixed flame burning mechanism of coaxial jet diffusion flamen and numerical simulation, analyzes the distribution characteristics of OH* and CH*, the excited state is studied on the relationship of the heat of reaction. The results showed that the chemiluminescence diagram of OH* and CH* obtained by ICCD camera and corresponding filter and the simulated results of the mole fraction distribution of OH* and CH* in the numerical were consistent. The OH* distribution was mainly divided into three combustion regions, and the CH* distribution was mainly divided into two combustion regions. The distribution of OH* and CH* in the diffusion flame presents a single peak, and the reaction heat presents a bimodal phenomenon. The changing trend of the reaction heat is similar to that of the excited state. After reaching the first peak, the exciter state gradually decreases to zero, while the reaction heat first decreases and then slowly increases to the second peak, and finally reduces to zero. In the diffusion flame, when the mass fraction of OH* and CH* in the radial direction reaches the peak, the heat of reaction also reaches the first peak. In the axial direction when the reaction rate of C2H+O=CH*+CO(R12) reaches the peak, the heat of reaction reaches the second peak. In premixed flames, with the increase of local equivalent ratio, the mass fraction of OH* and CH* increases obviously, and the distribution area is wide. When the mass fraction of OH* and CH* in the radial direction reaches the peak, the heat of reaction also reaches the peak. In the axial direction, the peaks of the four reactions rates of OH* and CH* are all in the same position, and the heat of reaction also reaches the maximum. The reaction rates of CH+O2=OH*+CO(R1) and C2H+O=CH*+CO(R12) are faster than that of H+O+M=OH*+M(R2) and C2H+O2=CH*+CO2(R11).
反应热是燃烧诊断中标识反应区和监控燃烧状态的重要参数之一, 直接测量火焰的反应热一直很困难, 因此燃烧中反应热的分布成为研究的热点。 化学反应中激发态自由基的电子能级跃迁产生的离散光谱辐射, 即化学发光[1]。 OH* , CH* 和C* 等激发态自由基产生的化学发光可用来描述火焰结构、 标识燃烧反应位置、 氧燃当量比以及热释放率等信息[2, 3], 被广泛应用于火焰燃烧状态的在线诊断。 Haber最早提出OH* 和CH* 与化学发光特性与放热率之间的关系, 结果表明OH* 能很好的标识反应热。 Panoutsos等[4]对比了8种不同的激态反应模型, 分析了对冲火焰中激发态粒子OH* 和CH* 与燃烧特性之间的关系, 结果表明OH* 可以很好地标识放热区。 曾科等[5]研究了一维模型负压下CH4/Air层流预混火焰, 结果表明富燃和贫燃情况下都是OH* 最先达到峰值。 胡悦[6]等研究了OH* 与放热率之间的关系, 分析了OH* 浓度最大值与反应热最大值之间的关系。
之前对激发态粒子的研究多为一维, 无法反映局部当量比的影响, 无法直观观察激发态粒子的分布特征, 当前的热点是二维或三维激发态研究。 Allison[7]等对二维燃烧进行了研究, 分析了火焰结构特点。 何磊[8]等对甲烷/氧气层流同轴射流扩散火焰进行了研究, 结果表明OH* 的分布形态可以表明是富氧燃烧还是贫氧燃烧。 Kojina[9]对二维层流预混火焰进行研究, 分析了激发态粒子的分布特性。 He等[10]研究了扩散火焰中OH* 化学发光与反应热的关系。
以上研究仅针对H2的火焰, 或者仅研究OH* 分布, 实际上CH* 分布也具有重要意义。 本工作以甲烷/空气作为研究对象, 在自适应建表(ISAT)加速燃烧的前提下, 基于GRI Mech 3.0详细燃烧机理结合OH* 和CH* 生成与淬灭化学反应机理, 对火焰中OH* 和CH* 的二维分布以及反应热进行研究, 探讨其分布特性及激发态粒子与反应热之间的关系。
选用Fluent进行数值模拟计算, 燃烧模型选用有限速率/涡耗散模型, 化学反应及燃烧模型中守恒方程为
式(1)中, ρ 为密度, Yi是组分i的质量分数, v为速度, Ji为物质i的扩散通量, Ri是化学反应中组分i的净产生速率, Si为源项。
Ji由浓度梯度产生, 可由式(2)计算得到
式(2)中, Di, m是混合物中物质i的扩散系数。 多个化学反应的组分i的净生成速率由式(3)得到
式(3)中, Mw, i是组分i的分子量,
以甲烷/空气同轴射流燃烧为研究对象, 为准确模拟甲烷的燃烧过程, 考察了包含激发态粒子反应在内的多组分甲烷燃烧机理。 基态粒子化学反应模型采用GRI-Mech3.0机理, 共包含53个组分, 325个基元反应, 完整地描述了基态粒子的产生与消耗。
探究OH* 和CH* 在燃烧中的分布特性以及与反应热的关系, 因此燃烧机理中还需考虑OH* 和CH* 的生成与淬灭, 详细机理如表1所示。 综合基态与激发态的组分及反应, 最后得到37个组分, 237个反应步的详细化学机理。
| 表1 OH* /CH* 自由基化学反应动力学参数 Table 1 Kinetics parameters of OH* and CH* radicals reaction |
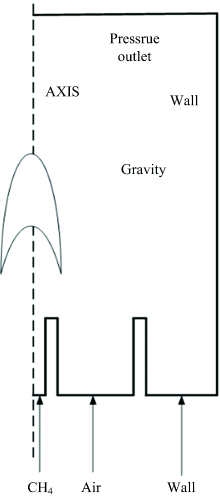
以实验室采用的同轴燃烧器作为数值计算的对象, 如图1所示, 火焰为对称性结构, 选取1/2截面进行数模计算, 计算区域沿轴向长度为100 mm, 沿径向总长为25 mm, 中心燃料出口为1 mm, 空气出口2 mm, 燃料和空气之间的壁厚2 mm, 且向上延伸5 mm, 具体二维计算区域如图2所示, 对表2和表3的工况进行数值模拟。
| 表2 扩散火焰工况 Table 2 Diffusion flame conditions |
| 表3 预混火焰工况 Table 3 Premix flame conditions |
燃料气体的进口边界条件为速度入口, 空气为压力入口, 底部右侧为壁面, 计算域的右边设置为壁面, 实验中采用玻璃罩, 左边界设置为对称轴, 上边界设置为压力出口边界条件, 操作压力为101 325 Pa。 为保证模拟的准确性, 所有网格均采用结构化网格, 网格质量均在0.95以上, 网格总数约为62万。
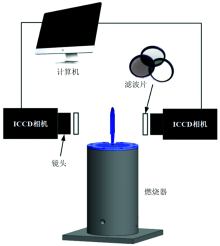
同轴射流燃烧器是用于产生射流扩散火焰的一种典型燃烧器, 结构简单, 主要分为中心射流喷嘴和同轴射流喷嘴两部分, 同样具有内外两个腔体, 但由于内外分别通入燃料和氧化剂, 不涉及混合, 此处两个腔体只作为集气腔, 保证喷嘴上游压力稳定。 贴壁面安装隔网, 在其中填充若干钢珠, 防止回火, 同时起到一定的整流作用, 保证出口处的气流速度均匀分布。 燃料由中心集气腔进入中心射流喷嘴, 再从射流喷嘴出口流出, 与同轴射流空气进行扩散燃烧。
由于化学发光十分微弱, 因此必须使用ICCD相机采集发光信号; 成像系统主要由ICCD相机、 镜头、 近摄镜、 滤波片构成, 相机可探测的波段为190~1 080 nm, 包含研究所需的300~500 nm波段, 并且曝光时间、 转换速率等参数均较好的满足试验需求。 为拍摄不同激发态粒子化学发光的空间分布, 在镜头前加装对应波段的滤波片, 过滤掉其他波段信号的干扰。 因主要研究OH* 和CH* 两种激发态粒子, 对应的中心波长分别为308和431 nm。 详细试验参考胡悦的甲烷-空气预混火焰中化学发光定量化测量放热率的试验研究[14]。
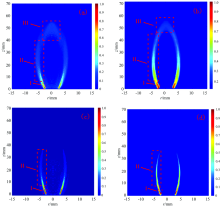
图3为扩散火焰工况2下OH* 和CH* 的二维分布实验结果和模拟结果的对比, (a)和(b)分别是OH* 摩尔质量分布的实验结果和模拟结果, (c)和(d)分别是CH* 摩尔质量分布的实验结果和模拟结果。 从图中可以看出模拟结果与实验结果有相同的变化趋势以及很好的吻合性。 OH* 分布主要分为三个燃烧区域, 离开喷嘴处摩尔质量最大的第一燃烧区, 然后向火焰下游延伸的第二燃烧区, 此区域范围较大, 第三燃烧区摩尔质量逐渐减小, 此区域范围较小。 CH* 分布主要为两个燃烧区域, 离开喷嘴的第一燃烧区域摩尔质量最大, 然后向火焰下游扩散形成第二燃烧区。 模拟结果得到摩尔分数稍大, 这是由于燃烧机理相对于实际燃烧有简化, OH* 和CH* 的生成和淬灭略有偏差, 但该偏差对模拟结果影响较小, 可以认为本数值模拟能够准确地反映激发态粒子OH* 和CH* 的分布以及燃烧情况。
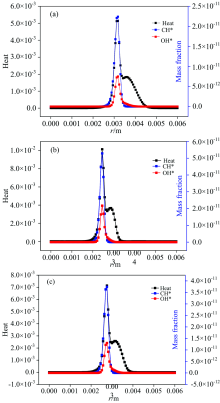
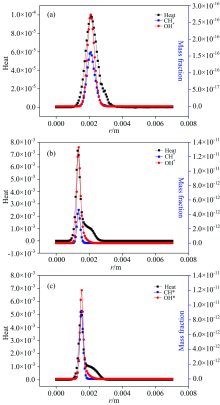
由图4(a, b, c)中可以看出三种工况下中心CH4速度不变, 逐渐增大空气流速时, 反应热和OH* 和CH* 的分布趋势一致, OH* 和CH* 质量分数增大时, 反应热也增大, 当激发态粒子OH* 和CH* 的质量分数达到峰值的时候, 反应热也达到峰值。 空气速度分别是0.12, 0.4和1.0 m·s-1时, 反应热的第一峰值和激发态粒子的峰值分别位于0.003 1, 0.002 75和0.002 4 mm, 燃烧区域逐渐向中心轴移动, 由此可以看出OH* 和CH* 能标识反应热。
与激发态粒子分布特性不一样的是反应热呈现双峰现象。 反应热第一峰值的变化与OH* 和CH* 相似, 随着燃烧反应的进行, 反应热迅速增加达到第一波峰, 随后迅速减小, 但减小到离开激发态粒子的反应区域后与OH* 和CH* 的分布不相同, OH* 和CH* 是迅速减小到零, 但反应热产生拖尾现象, 释放热量逐渐增加到第二峰值后再缓慢减小。
反应热达到第一峰值后迅速减小, 然后出现第二个波峰后再逐渐减小为零, 为了解此现象将对化学反应速率进行分析。
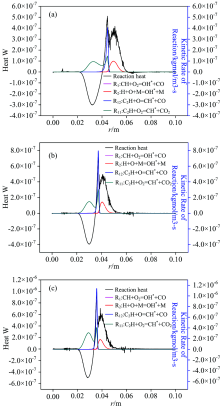
图5(a, b, c)为不同空气速度下反应热、 OH* 、 CH* 生成速率的轴向分布图, 从图中可知CH4速度不变, 逐渐增大空气速度, 不同工况下反应热和激发态粒子OH* 和CH* 的生成速率分布趋势一样, 反应热存在第一峰值和第二峰值呈现双峰现象。
CH* 的主要生成反应机理是C2H+O2=CH* +CO2(R11)和C2H+O=CH* +CO(R12)。 离开喷嘴出口CH4迅速反应生成C2H, 此时甲烷和空气接触区域内氧气含量高, 与C2H反应生成CH* 。 随着氧气参与反应后逐渐转变成游离氧, 在反应区域内游离氧的含量增加, 游离氧是R12的反应物, 因此反应速率增加, 此刻两者反应速率都达到最大, 释放的热最多, 反应热达到第一峰值。
OH* 的主要生成反应机理是CH+O2=OH* +CO(R1)和H+O+M=OH* +M(R2), 离开喷嘴后燃烧区域内氧气含量高, 但是CH含量很少, 因此R1反应速率很小。 随着火焰不断向下游方向传播, 游离氢和游离氧的质量分数不断增加, 两者迅速结合反应生成OH* , 使R2的反应速率增加, 从而反应热增加, 达到第二波峰, 因此反应热呈现双峰现象。
从图6(a, b, c)中可以看出, 在三种工况下中心预混气体和空气速度不变, 逐渐增大中心预混气体的当量比, 反应热和激发态粒子OH* 和CH* 的分布趋势一样, 在激发态粒子OH* 和CH* 质量分数增大时, 反应热也增大, 当激发态粒子OH* 和CH* 的质量分数达到峰值的时候, 反应热也达到峰值, 由此可以表明激发态粒子OH* 和CH* 能标识反应热。
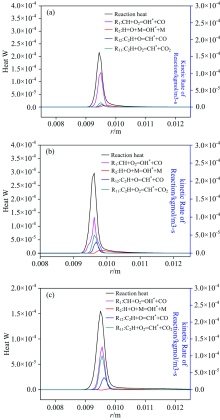
图7(a, b, c)为不同空气流速下反应热、 OH* /CH* 生成速率的轴向分布图, 从图中可见中心预混气体和空气速度不变, 逐渐增大中心预混气体的当量比, 反应热和激发态粒子OH* 和CH* 的生成速率分布一样。 当激发态粒子的反应速率达到最大值时, 反应热也达到最大值。
本研究是模拟预混火焰燃烧, 中心预混气体的当量比大于1, 因此CH* 的主要生成反应机理是C2H+O2=CH* +CO2(R11), OH* 的主要生成反应机理是 CH+O2=OH* +CO(R1)。 H+O+M=OH* +M(R2)和C2H+O=CH* +CO(R12)的反应物为游离氧, 反应速率较R1和R11的反应速率小。 激发态生成反应速率最大的位置也是在反应热最大的位置, 由此可见在激发态粒子生成速率最大时, 释放的热量最多, OH* 和CH* 能标识反应热。
开展了包含激发态反应机理的甲烷/空气同轴射流预混火焰和扩散火焰的二维数值研究, 结果表明:
(1) 在相同工况下激发态摩尔分数的数值模拟结果与试验结果吻合;
(2) 扩散火焰中OH* 和CH* 分布呈现单峰, 反应热呈现双峰现象, 反应热与激发态变化趋势相似, 达到第一峰值后激发态逐渐减小为零, 而反应热达到第一峰值后先减小再缓慢增加达到第二峰值, 最后减小为零。
(3) 扩散火焰中, 沿径向OH* 和CH* 的质量分数达到峰值时, 反应热也达到第一峰值; 沿轴向方向, 当C2H+O=CH* +CO(R12)反应速率达到达到峰值时, 反应热达到第一波峰值, H+O+M=OH* +M(R2)反应速率达到达到峰值时, 反应热达到第二波峰;
(4) 预混火焰中, 沿径向方向OH* 和CH* 的质量分数达到峰值时, 反应热也达到峰值; 沿轴轴向方向, OH* 和CH* 的四个生成反应速率的峰值都在同一位置, 反应热也达到最大值, CH+O2=OH* +CO(R1)和C2H+O=CH* +CO(R12)反应速率相比当H+O+M=OH* +M(R2)和C2H+O2=CH* +CO2(R11)反应速率更大。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|