作者简介: 高瑞琳, 女, 1993年生, 北京中医药大学中药学院硕士研究生 e-mail: gaoruilin02@163.com
近红外定量建模过程常以模型评价指标对样本集选择、 光谱预处理方法、 潜变量因子数、 变量选择等参数进行逐步优选, 然后采用优选参数建立模型, 此建模过程并未充分考虑参数间的协同作用对模型的影响, 导致模型的质量存在风险。 系统建模思想将定量建模过程看作一个整体, 将样本集选择、 光谱预处理、 变量筛选、 校正等作为要素, 基于要素间的关联性进行参数轨迹全局优化, 优选出一组最佳建模参数来建立模型, 从而保障模型质量。 该研究基于系统建模思想开展了脑心通胶囊中丹酚酸B的近红外定量建模。 采用高效液相色谱法对56份丹参样品中的丹酚酸B进行含量测定, 同时采集其近红外光谱, 采用D-最优设计样本集划分方法、 光谱预处理方法、 潜变量因子数及变量筛选方法作为自变量, 以模型评价指标为因变量优选最佳建模参数轨迹并建立定量分析模型。 结果表明, 采用Kennard-Stone(K-S)算法从56份样本中选择3:1的校正集样本、 建模光谱波段为4 000~10 000 cm-1、 预处理方法为二阶求导和标准正则变量变换校正, 潜变量因子数为7时所建立的定量分析模型效果最优。 模型的校正标准偏差(RMSEC)、 预测标准偏差(RMSEP)均为0.001 8, 表明模型稳健且预测准确度高。 校正决定系数(R2cal)为0.994 0, 预测决定系数(R2pre)为0.995 2, 相对分析误差(RPD)为9.19, 表明模型可用于高质量的定量分析和预测。 本研究基于系统建模思想, 采用D-最优设计实现了建模参数轨迹全局优化, 建立了丹酚酸B的定量分析模型并且显著提升了模型的稳健性和预测性, 为高效、 快速测定脑心通胶囊中丹酚酸B含量提供了方法, 对脑心通胶囊中间体及成品的质量控制具有重要意义。
NIR quantitative modeling mainly involves four process parameters: the selection of sample set, spectra pre-processing, latent variables and variable selection methods. And in the traditional method, the optimization of the PLS modeling parameters was step by step according to the model evaluation indexes and the inter-influence among the parameters was rarely considered in the model development. This is risky because the modeling path is not necessarily the best approach to step by step optimization. The system modeling method is global trajectory parameter optimization idea based on the correlation between the parameters, which is a systematic approach to improve the efficiency and accuracy in the development of a quantitative model. The purpose of this study is based on the system modeling idea to develop a NIR quantitative model for the analysis of salvianolic acid B in Naoxintong capsule. The content of salvianolic acid B in 56 samples of Salvia miltiorrhiza was determined by high-performance liquid chromatography (HPLC), and the near-infrared spectra were also collected. D-optimization design method was used to optimize the modeling parameters including the sample set partition, spectral pre-processing, latent variable factor number and variable selection. The global optimal parameter trajectory was applied in the preparation of the quantitative analysis model. The results showed that the best quantitative model was developed by the spectral data pretreatment of 2D+SNV (2nd Derivative + Standard Normal Variate), choosing the latent variable factor number of 7 and spectral region of 4 000~10 000 cm-1 in combination with the 56 samples were randomly divided into a calibration set and a validation set according to the proportion of 3:1 by a K-S algorithm. Its standard deviation of calibration (RMSEC) and prediction (RMSEP) were both 0.001 8, which demonstrated the high analytical accuracy and robust fitting. The calibration coefficient of determination (R2cal) and the prediction coefficient of determination (R2pre) were 0.994 0 and 0.995 2, respectively. The ratio of the standard error of prediction to the standard deviation (RPD) was 9.19, further confirming that the model can be used for high-quality quantitative analysis. Based on the system modeling idea, the D-optimal design approach was adopted to implement the global trajectory parameter optimization in the process of establishing the quantitative model in this paper. Furthermore, a quantitative model for salvianolic acid B was developed with robust predictability and high accuracy. The model provided an efficient and rapid method to quantify salvianolic acid B of Naoxintong capsule, which was of great significance for the quality control of intermediates and products of Naoxintong capsule.
脑心通胶囊为黄芪、 赤芍、 丹参、 全蝎、 水蛭等16味药材粉碎加工制成的中药复方制剂, 具有益气活血、 化瘀通络的功效, 临床上治疗心脑血管疾病具有显著疗效[1]。 目前, 脑心通胶囊的质量控制主要采用指纹图谱分析及指标成分丹酚酸B定量分析的方法[2], 检测过程繁琐费时, 且难以实现脑心通胶囊制剂过程中间体的快速评价和质量控制。
近年来, 近红外光谱(near-infrared spectroscopy, NIR)分析技术凭借其快速、 可靠、 无损、 环保等优势, 在中药材、 中药制剂[3]、 中药生产过程以及药物质量快速评价[4]中得到日益广泛的应用[5]。 稳健可靠的定量模型是近红外技术成功应用的前提和保证。 常规近红外定量建模过程采用逐步优化的思路[6], 这样的建模思路并未充分考虑建模参数间的关联性对模型性能的影响, 致使定量模型的质量存在风险[7]。 系统建模思想[7]将建模过程看作一个整体, 将样本集选择、 光谱预处理、 变量筛选、 校正等作为要素, 基于要素间的关联性对建模参数轨迹进行全局优选, 采用最优参数轨迹构建模型, 保障了模型质量。 本研究基于这一思想, 采用D-最优设计以关键建模参数为自变量, 模型评价指标为因变量, 基于参数间关联性进行多次建模试验, 根据定量建模结果拟合预测模型, 以最优模型性能为目标对建模参数轨迹进行全局优选, 优选出最佳参数轨迹, 建立了稳健的丹酚酸B偏最小二乘法(partial least square, PLS)定量模型, 为脑心通胶囊生产过程及产品的快速质量评价提供有效方法。
Antaris傅里叶变换近红外光谱仪(美国Thermo Nicolet公司)配备InGaAs检测器, 积分球漫反射采样系统, Result操作软件; Agilent 1260型高效液相色谱仪(美国安捷伦科技公司); Agilent Eclipse XDB-C18色谱柱(5 μ m, 4.6 mm× 250 mm); 拜杰高速多功能粉碎机BJ-400A型, BP211D型电子天平(德国赛多利斯科学仪器有限公司)。
乙腈(色谱纯, 批号175157, 赛默飞世尔科技(中国)有限公司), 蒸馏水(广州屈臣氏食品饮料有限公司), 甲醇(分析纯, 批号20170515, 北京化工厂), 丹酚酸B(上海源叶生物科技有限公司, 纯度≥ 98%, 批号P10J9F52565)。 丹参药材由陕西步长制药有限公司提供。 将丹参药材随机编号, 粉碎, 过六号筛, 低温干燥后备用。
1.3.1 色谱条件
采用Agilent Eclipse XDB-C18色谱柱(5 μ m, 4.6 mm× 250 mm), 流动相为乙腈(A)和0.1%磷酸水溶液(B), 梯度洗脱(0~20 min, 23%A; 20~25 min, 23%~95%A; 25~35 min, 95%~23%A; 35~40 min, 23%A), 检测波长286 nm, 流速1.0 mL· min-1, 柱温30 ℃, 进样量10 μ L。
1.3.2 对照品溶液制备
精密称取丹酚酸B对照品适量, 加80%甲醇配制成浓度为2.002 mg· mL-1对照品溶液。
1.3.3 供试品溶液制备
取样品细粉约0.5 g, 精密称定, 置于具塞锥形瓶中, 精密加入80%的甲醇50 mL, 称定重量, 超声提取30 min, 放冷后, 再称定重量, 用80%甲醇补足减失的重量, 摇匀, 滤过, 取续滤液, 即得。
1.3.4 方法学考察
1.3.4.1 线性关系考察
精密量取丹酚酸B对照品溶液0.05, 0.25, 1.0, 2.0和2.5 mL, 分别用80%甲醇稀释于5 mL容量瓶中, 即得各系列浓度对照品溶液。 对照品溶液进样10 μ L, 测定峰面积, 作为线性关系考察。
1.3.4.2 精密度、 稳定性、 重复性、 加样回收率考察
精密吸取丹酚酸B对照品溶液, 重复进样6次, 测定丹酚酸B峰面积值, 作为精密度考察; 取同一份供试品溶液, 分别于制备后0, 2, 4, 8, 12和24 h进样分析, 测定丹酚酸B峰面积值, 作为稳定性考察; 精密称取同一批丹参样品6份, 按照1.3.3节所述方法制备供试品溶液, 进样分析, 测定丹酚酸B含量, 作为重复性考察; 精密称取6份已知含量的丹参样品约0.3 g, 分别精密加入对照品溶液3.5 mL, 按供试品制备方法制备, 进样分析, 测定丹酚酸B峰面积, 作为回收率考察。
1.3.5 样品测定
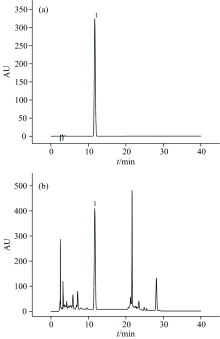
分别精密吸取对照品和供试品溶液10 μ L注入液相色谱仪, 记录40 min色谱图。 见图1。
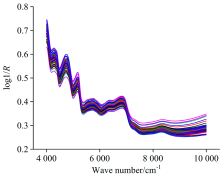
以积分球漫反射方式采集近红外光谱, 光谱采集范围为4 000~10 000 cm-1, 分辨率8 cm-1, 扫描32次, 增益8, 以仪器内置背景为参照, 对56份丹参样品进行光谱采集, 每份样品重复测定3次, 取其平均光谱作为丹参各样品的近红外光谱。 丹参样品的原始近红外光谱图见图2。
运用Unscrambler7.0(挪威CAMO公司)软件对光谱进行预处理。 采用Matlab7.0(美国Mathwork公司)软件进行变量筛选及模型计算。
为构建稳健的定量模型, 选择多元散射校正(MSC)、 标准正则变换散射校正法(SNV)、 SG平滑(SG)、 二阶导数法(2D)、 标准正则变换组合二阶导数法(2D-snv)等不同的光谱预处理方法对原始光谱进行预处理, 再分别采用间隔偏最小二乘法(iPLS)、 组合间隔偏最小二乘法(siPLS)、 移动窗口偏最小二乘法(mwPLS)对光谱变量[8]进行筛选, 建立丹酚酸B定量模型。 以校正决定系数(
D-最优设计[9]具有试验次数少、 多目标同步优化、 预测参数精密度高等特点, 可用于建模参数轨迹全局优化。 采用Design Expert 8.0.6软件进行D-最优试验设计, 优选出最佳建模参数轨迹并建立丹酚酸B定量模型。 以关键建模参数样本集划分比例(X1)、 潜变量因子数(X2)、 光谱预处理方法(X3)、 变量筛选方法(X4)为自变量, 以
| 表1 D-最优试验设计因素水平表 Table 1 Experimental factor levels and response variables for the D-optimal design |
依据1.3.4节所述方法对系列对照品溶液进行含量测定, 以浓度(mg· mL-1)为横坐标, 峰面积为纵坐标绘制标准曲线, 计算得标准曲线为y=11 712x-124.35, 相关系数R2=0.999 9, 表明丹酚酸B对照品浓度在0.020 0~1.001 0 mg· mL-1的范围内线性关系良好; 精密度考察中各对照品峰面积的RSD为0.80%, 表明仪器的精密度良好; 稳定性考察中供试品丹酚酸B峰面积的RSD为0.95%, 表明供试品溶液在24 h内稳定性良好; 重复性考察测得供试品中丹酚酸B的含量分别为0.065 42, 0.066 48, 0.067 19, 0.066 38, 0.065 38和0.066 21 mg· mg-1, RSD为1.04%, 表明方法的重复性良好; 测得丹酚酸B的回收率处于99%~103%范围内, RSD为1.38%, 表明方法准确度良好。 方法学考察结果表明, 线性关系、 精密度、 稳定性、 重复性及加样回收率均符合要求, 表明丹酚酸B含量测定方法可靠。
根据D-最优试验设计因素水平表设计进行55次试验, 按照试验表中建模参数轨迹建立定量模型, 并对模型的性能进行评价。 D-最优试验设计及结果见表2。 由表2可知, 不同的建模参数轨迹构建的PLS定量模型在性能方面表现出显著的差异。 因此可以看出, 优选最佳建模参数对于构建稳健的定量模型尤为重要。
| 表2 D-最优试验设计及结果 Table 2 Experimental results of D-optimal design |
采用Design Expert 8.0.6软件对试验数据进行拟合, 建立响应指标与建模参数间的拟合模型, 确定丹酚酸B定量模型的最佳建模参数轨迹。 各模型拟合与分析结果见表3。 可知各拟合模型P值均小于0.000 1, 决定系数R2均在0.99以上, 表明拟合模型对不同建模参数轨迹下的模型性能拟合良好, 可用于实际预测。 以最大
| 表3 模型拟合与分析结果 Table 3 Model fitting and analysis results |
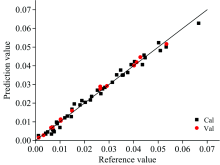
以优选的建模参数轨迹建立丹酚酸B定量模型, 模型的RMSEC, RMSEP较小且均为0.001 8, 表明模型的预测误差小, 精度高并具有较好的拓展性和稳健性; 校正决定系数
基于系统建模思想, 采用科学系统的D-最优设计以关键建模参数为自变量, 模型评价指标为因变量, 基于参数间的关联性进行多次建模试验。 试验充分考察了建模参数间协同关系对模型性能的影响, 以最优模型性能为目标优选出最佳的建模参数轨迹, 构建了全局最优的丹酚酸B近红外定量模型。 该模型的稳健性和预测准确度高, 可实现丹酚酸B含量的快速测定, 为高效、 快速、 无损地获取脑心通胶囊中丹酚酸B含量提供保证, 对脑心通胶囊的质量控制具有重要意义。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|