作者简介: 叶萍, 1998年生, 南京理工大学化工学院本科生 e-mail: 1069367569@qq.com
在太阳光照射下, 利用半导体光催化去除污染物是最绿色、 有效的方法之一, 其核心问题是获得高效光催化剂。 目前研究最多的光催化剂是TiO2和ZnO等, 但由于其禁带宽度大故不能充分利用太阳光, 从而限制了其实际使用。 除了对TiO2等改性以改进其可见光催化活性外, 开发其他材料作为光催化剂也是解决的重要途径。 铋基化合物半导体由于原材料丰富、 种类多、 太阳光响应性好及优良的光催化活性而成为重要研究对象。 其中卤氧铋系化合物[BiOX, X=Cl, Br, I]由于层状结构特点而具有良好的光催化活性, 但单独使用时光催化效率较低。 研究表明, BiOX间能通过形成固体溶液(即彼此呈分子分散的固体混合物)进一步改善其光催化降解污染物的能力。 本文利用低温湿化学法, 以Bi2O3为铋源, 在醋酸溶液中加入一定比例的KI/KBr或KI/KCl水溶液, 室温下反应0.5 h, 分别得到片状结构的BiOCl1- xI x和BiOBr1- xI x固体溶液。 X射线衍射(X-ray diffraction, XRD)分析结果表明, 所合成的BiOCl1- xI x和BiOBr1- xI x样品结晶性良好, 且能在 x=0~1的范围内形成固体溶液。 透射电子显微镜(transmission electron microscope, TEM)测得所制备的固体溶液呈不规则的薄片状。 X射线光电子能谱(X-ray photoelectron spectroscopy, XPS)测试进一步证明了其表面元素组成及化学状态。 紫外-可见漫反射光谱(diffuse reflectance spectroscopy, DRS)分析表明, 随着碘元素含量的增加, 固体溶液的吸收边界发生红移、 禁带宽度减小, 故可见光吸收能力增强、 产生的载流子数目将增加。 在可见光激发下对甲基橙(methyl orange, MO)降解的光催化性能研究表明, BiOCl0.25I0.75及BiOBr0.25I0.75拥有最高的光催化活性。 循环实验表明, BiOCl0.25I0.75及BiOBr0.25I0.75都具有较高稳定性。 光催化机理研究发现, 这些卤氧铋样品光催化降解MO过程中的活性物种主要为空穴和超氧离子自由基。 结合其能带结构, 认为固体溶液的形成不但增加了可见光吸收能力, 而且调变了其能带结构, 相对于BiOI而言, 固体溶液的形成降低了价带电位, 提高了导带电位, 因而增强了光生电子的还原能力及空穴的氧化能力, 故催化性能提高。 该工作的创新之处在于: 采用的固体溶液制备方法, 避免了高温水热法或加入表面活性剂等, 而且所制备的BiOCl1- xI x和BiOBr1- xI x固体溶液, 尤其是BiOCl0.25I0.75和BiOBr0.25I0.75, 在可见光激发下对MO具有良好的降解能力, 且催化剂的重复使用及稳定性良好, 有望在环境治理中得到应用。
The usage of semiconductor photocatalysts for removal of contaminants is one of the greenest and most effective methods under sunlight, whose core is obtaining high-efficient photocatalysts. The most widely studied photocatalysts are TiO2, ZnO, etc., but they cannot fully utilize sunlight due to their large band gapenergy, thus limiting their practical use. In addition to modifying TiO2 to improve its visible light catalytic activity, the development of other materials as photocatalysts is also an important solution. Bismuth based compound semiconductors have become important research objects for their abundant raw materials, various types, good solar response and excellent photocatalytic activity. Bismuth oxyhalide compounds [BiOX, X=Cl, Br, I] exhibit excellent photocatalytic activity owning to layered structure, but they still have low photocatalytic efficiency when used alone. However, their photocatalytic degradation efficiency could be improved by preparing solid solutions (a mixture of solids that are molecularly dispersed with each other). In this work, a low-temperature wet chemical method can be used to obtain solid solutions BiOCl1- xI x and BiOBr1- xI x with sheet like structures, which is prepared by the reaction of a certain proportion of KI/KBr or KI/KCl aqueous solution with Bi2O3/HAc solution for half an hour at room temperature. X-ray diffraction (XRD) patterns showed that the synthesized BiOCl1- xI x and BiOBr1- xI x samples have good crystallinity and can form a solid solution in the range of x=0~1. The prepared solid solution was found to have an irregular sheetlike shape by a transmission electron microscope (TEM). X-ray photoelectron spectroscopy (XPS) tests further demonstrate their surface element composition and chemical state. Ultraviolet-visible diffuse reflectance spectroscopy (DRS) analysis indicates the red-shifted absorption edge of the solid solution and decreased band gap energy as the iodine content increased, so the visible light absorption capacity is enhanced and the number of generated carriers is agumented. The photocatalytic tests of MO degradation under visible light excitation manifest that BiOCl0.25I0.75 and BiOBr0.25I0.75 exhibit the highest photocatalytic activity. Cyclic experiments show that BiOCl0.25I0.75 and BiOBr0.25I0.75 have high stability. Photocatalytic mechanism studies show that the active species in the photocatalytic degradation of MO in these bismuth oxyhalide samples were holes and superoxide ion radicals. Combined with their energy band structures, it is believed that the formation of solid solution not only increases the visible light absorption capacity, but also modulates its energy band structure. Compared with BiOI, the formation of solid solution lowers the valence band position and raises the conduction band position. Therefore, the reducing ability of the photogenerated electrons and the oxidizing ability of the holes are enhanced, so that the catalytic performance is improved. The novelty of this work is low-temperature solid solution preparation, which avoids hydrothermal method or the addition of surfactants. Furthermore, the prepared BiOCl1- xI x and BiOBr1- xI x solid solutions, especially BiOCl0.25I0.75 and BiOBr0.25I0.75, have excellent photocatalytic degradation ability for MO under visible light excitation. Moreover, the catalysts have good stability, so it is expected to be applied in environmental management.
光催化技术是解决能源短缺和环境污染的有效方法。 近年来铋基化合物半导体由于其原料成本低廉, 制造工艺相对简单以及光催化活性[1]良好而备受关注。 BiOX[2, 3, 4] (X=Cl, Br, I)是一种高度各向异性的层状结构半导体, 其X原子层之间由X原子通过范德华力结合, 结合力较小, 结构疏松, 容易沿(001)方向解离。 且BiOX的导带主要由Bi(6p)轨道构成, 价带主要由O(2p)和X(np)(n分别为3, 4和5)轨道杂化构成, 因此其属于间接带隙半导体。 独特的能带结构使BiOX具有优异的光催化性能[5], 但单独使用时, 仍存在光吸收范围窄、 光生电子与空穴容易复合等缺点。
BiOX的另一特点是能通过相互间形成固体溶液或复合物而改善其光催化效率[6, 7, 8, 9]。 有研究等以Bi(NO3)3为铋源, 在NH3· H2O中加入一定比例的KCl/KBr溶液, 制备了xBiOBr-(1-x)BiOI和xBiOI-(1-x)BiOCl固体溶液, 在可见光下对于甲基橙降解具有较好的活性。 Cao[10]等利用化学沉积法将BiOI和BiOBr复合形成BiOI/BiOBr异质结复合光催化剂, 所生成的60%BiOI/BiOBr光催化剂光催化性能最好, 在可见光照射5 h后, 下对甲基橙降解效率可达60%以上。 虽然在制备BiOX时常以Bi(NO3)3作为铋源, 但Bi3+极易水解, 制备过程中若不加入无机酸或有机溶剂阻止其水解, 极易形成碱式硝酸铋, 影响产物的纯度; 若加入大量的无机酸或有机溶剂, 或使用溶剂热法、 水热法, 会造成大量的化学废料或能源浪费。 本工作采用低温湿化学法制备BiOCl1-xIx或BiOBr1-xIx(x=0~1)固体溶液, 利用XRD, TEM, XPS, DRS等对样品的晶体结构、 性质及能带结构进行了表征, 并以MO为模拟污染物, 研究了其在可见光激发下的光催化性能。
试剂: 氧化铋(Bi2O3)、 冰醋酸(HAc)、 氯化钾、 碘化钾、 溴化钾、 草酸铵(国药集团化学试剂有限公司)、 无水乙醇、 异丙醇(南京化学试剂有限公司)、 甲基橙(广东省化学试剂工程技术研究开发中心)、 苯醌(上海统亚化工有限公司)。
仪器: 光化学反应仪(XPA-7), 紫外-可见分光光度计(UV-1201), X射线粉末衍射仪 (XRD; Bruker), 透射电子显微镜 (TEM; JEM-2100, JEOL), X射线光电子能谱仪 (XPS; PHI), 紫外-可见漫反射光谱仪(DRS; UV-2550)。
称取0.47 g Bi2O3 (1 mmol)溶于10 mL HAc溶液中, 剧烈搅拌反应, 观察到黄色的Bi2O3迅速变白, 继续搅拌30 min后, 加入30 mL去离子水, 在搅拌过程中白色固体逐渐溶解, 溶液逐渐变透明。 将溶有2 mmol (1-x)KCl/xKI或(1-x)KBr/xKI(x=0, 0.25, 0.5, 0.75, 1)的20 mL水溶液加入到上述溶液中, 出现黄色沉淀, 继续搅拌反应30 min。 离心收集产品, 用去离子水洗涤3次、 无水乙醇洗涤1次后, 置于室温中晾干。
光催化实验在多试管搅拌式光化学反应仪中进行, 以500 W氙灯为光源, 插入420 nm滤光片。 以甲基橙(MO; 10 mg· L-1)为模拟废水。 称取0.02 g催化剂加入50 mL甲基橙溶液中, 暗室中先超声分散5 min, 然后磁力搅拌1 h, 待染料溶液-催化剂之间达到吸附平衡后, 开启光源, 进行光催化反应。 每隔20 min用吸管取出3 mL溶液, 离心, 取上层清液, 通过紫外-可见分光光度计(在465 nm处)测定MO吸光度。 为了保证光催化反应在相同条件下完成, 每次离心管中的残余催化剂粉末倒回光催化反应管中, 并补加原始MO溶液至50 mL。 在测试光催化剂的稳定性时, 将光催化反应结束后的催化剂样品离心回收, 并用乙醇和水洗涤几次, 烘干, 然后按上述步骤对MO进行光催化实验。
2.1.1 XRD分析
图1(a)为所合成的BiOI, BiOCl0.25I0.75, BiOCl样品的XRD图, 其中BiOI和BiOCl的所有衍射峰分别对应于四方晶系的BiOI(JCPDS No.73-2062)和BiOCl (JCPDS No.06-0249)。 由图可知, 三种样品的衍射峰高而且尖锐, 说明样品结晶性较好。 对于BiOCl0.25I0.75样品, 位于24.3° , 29.7° 和31.7° 的衍射峰分别对应于BiOCl 的(101)晶面和BiOI的(012)和(110)晶面, 但与纯样品相比, 峰位置发生了偏移, 这是由于Cl-的离子半径(1.81 Å )小于I-(2.16 Å ), 故当晶格中的I-被Cl-取代后, 衍射峰向2θ 数值增大的方向移动, 符合Vergard规律[11], 证明形成了固体溶液。
 | 图1 所合成样品的XRD图 (a): BiOCl1-xIx; (b): BiOBr1-xIx(x=0, 0.75, 1)Fig.1 XRD patterns of the as-prepared samples (a): BiOCl1-xIx; (b): BiOBr1-xIx(x=0, 0.75, 1) |
图1(b)为所合成的BiOI, BiOBr0.25I0.75, BiOBr样品的XRD图, 其中BiOI和BiOBr的所有衍射峰分别对应于四方晶系的BiOI(JCPDS No.73-2062)和BiOBr (JCPDS No.09-0393)。 与BiOCl0.25I0.75类似, BiOBr0.25I0.75样品的结晶性良好, 从衍射峰的位移可证明形成了固体溶液。
2.1.2 TEM表征
图2(a— e)分别为BiOCl, BiOCl0.25I0.75, BiOI, BiOBr和BiOBr0.25I0.75样品的TEM图。 BiOCl和BiOBr样品均为由纳米片组装而成的花状分级结构, 直径大约在2~3 μ m。 BiOI呈片状结构, 大小不均匀。 类似于BiOI, 固体溶液BiOCl0.25I0.75及BiOBr0.25I0.75的TEM照片中都没有观察到花状形貌, 均呈片状, 尺寸不均匀, 分析认为由于固体溶液中I-的含量高所致。
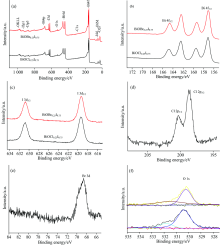
2.1.3 XPS表征
图3为BiOCl0.25I0.75及BiOBr0.25I0.75的XPS图谱。 对于BiOCl0.25I0.75, 图3(a)全谱显示, 样品中包含Bi, O, Cl, I和C, 无其他杂质, 其中C元素为样品表面污染碳, 以C(1s) 284.8 eV为内标, 校正其他元素的结合能。 Bi(4f)的高分辨XPS图显示两组峰[图3(b)]: Bi3+(结合能为164.6和159.4 eV)和Bi(3-X)+(结合能为162.2和156.8 eV)的特征峰。 其中Bi(3-X)+的形成是由于I的还原所致[12]。 I 3d3/2和I 3d5/2的结合能分别为631.1和619.2 eV[图3(c)], Cl 2p3/2及Cl 2p1/2的结合能为199.54和198.0 eV[图3(d)]。 O(1s)的XPS图可拟合为两个峰[图3(f)]: 结合能在530.2 eV对应于Bi— O中氧的结合能, 531.7 eV对应于表面吸附水中氧的结合能。 类似地, BiOBr0.25I0.75样品的的XPS图谱也显示相应的元素的结合能, 其中Br3d的结合能为69.0 eV, 见图3(e)说明得到了固体溶液。
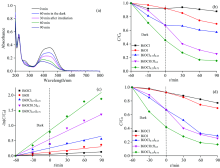
2.1.4 DRS表征
图4(a)为所制备样品的DRS图。 由图可知, BiOCl只能吸收紫外光, 吸收边缘位于382 nm。 BiOBr能吸收可见光, 吸收边缘延长至433 nm左右。 BiOI对可见光的相应范围最宽, 吸收边缘达657 nm。 对于固体溶液BiOCl0.25I0.75与BiOBr0.25I0.75, 吸收边缘分别位于630与634 nm, 与BiOI很接近, 这是由于固体溶液中I元素含量高所致。 BiOX为间接跃迁型半导体, 以(α hν )1/2对hν 作图[图4(b)], 根据曲线作切线并外推至横轴, 交点即为其禁带宽度Eg, 则BiOCl, BiOBr, BiOI, BiOCl0.25I0.75和BiOBr0.25I0.75样品的禁带宽度分别为3.32, 2.79, 1.72, 1.80和1.82 eV。 随着I元素含量的增加, 样品吸收边界逐渐向长波方向移动, 禁带宽度减小, 故可见光吸收能力增强、 产生的载流子数目将增加。
2.2.1 光催化活性
BiOCl0.5I0.5为催化剂时, MO的吸光度随光照时间变化的一组曲线见图5(a)。 由图可知, MO的最大吸光波长位于465 nm。 初始MO的吸光度为0.36。 吸附后, 吸光度降至0.26。 光照后, MO的吸光度随着光照时间而降低。 根据吸光度计算MO的降解率。
所制备BiOCl1-xIx在可见光激发下降解MO的活性如图5(b)所示, 其中, BiOCl0.25I0.75固体溶液的光催化活性最好, 150 min内, MO的降解率达85%。 相同的时间内, BiOCl, BiOCl0.75I0.25, BiOCl0. 5I0.5及BiOI作为催化剂时, MO的降解率分别为12%, 43%, 75%及31%。 MO在这些样品上的降解基本符合Langmuir-Hinshelwood动力学模型, 即-ln(C0/C)=kt[图5(c)]。 从动力学拟合曲线斜率可得BiOCl, BiOCl0.75I0.25, BiOCl0. 5I0.5, BiOCl0.25I0.75和BiOI反应速率常数分别为0.000 8, 0.004, 0.009, 0.013和0.002 min-1。 由此可见, 与纯的BiOCl和BiOI样品相比, BiOCl0.25I0.75固体溶液在可见光下降解MO的活性得到明显提高。
与BiOCl1-xIx类似, 由图5(d)可知, 在可见光照射下, BiOBr0.25I0.75固体溶液表现出最好的光催化活性, 150 min内对MO的降解率达83%, 高于BiOBr(19%), BiOBr0.75I0.25(71%), BiOCl0. 5I0.5(75%)和BiOI(23%)。 BiOBr, BiOBr0.75I0.25, BiOBr0.5I0.5, BiOBr0.25I0.75和BiOI光催化反应速率常数分别为0.001, 0.008, 0.009, 0.013和0.002 min-1(图略)。
为测试所制备的BiOCl0.25I0.75和BiOBr0.25I0.75固体溶液的光催化稳定性, 进行了可见光激发下的多次催化循环实验。 如图6(a)和(b)所示, 经过四次循环实验后, MO的降解率基本不变, 说明片状BiOCl0.25I0.75和BiOBr0.25I0.75固体溶液光催化剂的稳定性良好。
 | 图6 (a) BiOCl0.25I0.75与(b) BiOBr0.25I0.75催化MO降解的循环性能测试Fig.6 Recycling tests of (a) BiOCl0.25I0.75 and (b) BiOBr0.25I0.75 catalysts for MO degradation under visible light irradiation |
2.2.2 光催化机理研究
如图7(a)所示, 分别以异丙醇(iso-propyl alcohol, IPA), 草酸铵(ammonium oxalate, AO)和苯醌(benzoquinone, BQ)为羟基自由基(· OH)、 空穴(h+)和超氧离子自由基(·
尽管BiOCl(Eg=3.32 eV)不能被可见光激发, BiOBr(Eg=2.79 eV)仅能吸收很少的可见光, 但当与大量的BiOI形成固体溶液后, 禁带宽度明显降低至1.80及1.82 eV, 故能充分利用可见光, 从而产生更多载流子。 结合活性物种实验, 固体溶液的光催化机理推测为: 在可见光激发下, 电子激发至导带, 与溶液中的O2形成·
(1)通过低温湿化学法合成了BiOCl1-xIx及BiOBr1-xIx固体溶液, 结晶度良好; 随着碘含量的增加, 固体溶液的禁带宽度减小, 可见光响应范围变宽。
(2)研究了BiOCl1-xIx及BiOBr1-xIx在可见光激发下降解甲基橙溶液的的光催化性能, 结果表明, BiOCl0.25I0.75与BiOBr0.25I0.75的光催化活性最佳, 且稳定性良好。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|