作者简介: 刘丰奎, 1984年生, 上海安杰环保科技股份有限公司高级工程师 e-mail: 182376777@163.com
含锂药剂在用于临床治疗精神疾病时需要对患者血清中锂元素浓度进行监测以在控制正常药效的同时防止锂中毒事故的发生。 目前临床医学检验血清中锂元素含量主要采用火焰原子吸收光谱和基于离子选择性电极的电化学技术。 但火焰原子吸收光谱技术需要使用乙炔钢瓶和空气压缩机, 存在仪器不能便携, 对实验室条件要求苛刻等缺点; 电化学方法存在电极处理与更换繁琐, 分析效率相对偏低等问题。 同时, 仪器可便携、 操作简单且对锂元素分析具有良好分析性能的液体阴极辉光放电-原子发射光谱技术尚未应用于医疗领域血清中锂含量的测定。 因此, 基于自制便携液体阴极辉光放电-原子发射光谱装置, 建立了血清中锂元素的高灵敏度分析方法。 系统考察了10~100倍血清样品稀释倍数对血清样品测试的干扰, 结果表明, 当血清样品稀释20倍以上时, 未发现显著的基体干扰, 可以较好地保证结果的可靠性。 对影响锂元素分析性能的分析谱线、 试液酸度等参数进行了系统优化, 结果表明671 nm为锂元素最佳测试谱线; 试液酸度对锂元素分析的灵敏度和稳定性影响显著, 采用1%硝酸( V/V)试液酸度可以保证良好的分析性能。 在优化的系统参数和实验条件下, 锂元素标准曲线的回归方程为: Ie=7 299 ρLi+400; R2=0.998 3。 当血清样品稀释20倍时, 该方法对锂元素的检出限为0.2 mg·L-1。 对同一血清样品6次重复测试考察本方法的重复性, 相对标准偏差小于5%。 将本方法应用于血清标准样品(Trace Elements Serium L-2)中锂含量分析, 测定值与证书标称值一致。 表明该方法可以较好地应用于医疗检验领域实际血清样品中微量锂元素含量的测定。
The lithium in serum of the patients should be monitored to achieve the regular medical effect and prevent from lithium poisoning when the medicine containing lithium is adopted to treat the manic depression. At present, flame atomic absorption spectrometry and electrochemical methods are commonly used in lithium determination in clinic area. However, for the flame atomic absorption spectrometry method, the instrument can’t be portable as the C2H2 cylinder is necessary, for which the demands for the laboratory are critical. As for the electrochemical technique, the treatment of the electrodes is tedious and the analytical efficiency is somewhat low. The solution cathode glow discharge-atomic emission spectrometry, which has proved to be sensitive for Li determination with simple operation and portable instrument, has never been used in clinic Li test in serum. Therefore, a novel method was established for sensitive determination of lithium in serum based on a home-made portable solution cathode glow discharge- atomic emission spectrometer. The serum samples were pumped into the discharging chamber after dilution and acidification. Lithium in serum was excited by the plasma generated between the solution cathode and the solid metal anode, and the characteristic spectrum came into being in the common atmosphere and the signal collection and analysis were carried out by using a fiber optical spectrometer. The influence of dilution times within 10~100 on matrix interferences was comprehensively investigated and the results showed that no significant matrix interferences were observed when the dilution times were above 20 and the reliability could be basically ensured. The parameters influencing the analytical performances, including the analytical emission line, the acidity of the testing solution, etc, were optimized. The results showed that 671 nm was proved to be the ideal analytical emission line due to the strongest emission intensity and the non-significant spectral interferences while the best analytical performance could be achieved when 1% HNO3( V/V)was adopted to keep the acidity of the solution on the premise of the suitable stability. Under the optimized conditions, the equation of the linear calibration curve was as follows: Ie=7 299 ρLi+400; R2=0.998 3. The limit of determination for lithium in the serum was 0.2 mg·L-1 when the serum sample was diluted by 20 times. The relative standard deviation for the repeatability test based on 6 times tests of the serum was below 5%. This method was applied to the analysis of serum standard material. The detection result was in favorable agreement with the certified value, which showed that this method can be used in the determination of lithium in real serum samples of clinical tests.
锂是一种有效的情绪稳定剂, 对人体中枢神经有调节作用。 适量的锂浓度能安定情绪, 如碳酸锂治疗狂躁型抑郁症有较好的效果[1]。 但碳酸锂治疗窗口较窄, 美国精神病学协会推荐有效浓度为0.5~1.2 mmol· L-1, 最佳治疗范围为0.6~0.7 mmol· L-1, 所以临床治疗时需对患者进行血锂浓度监测, 避免出现因锂药剂过量引起的中毒反应[2]。
目前, 医疗领域血清样品中锂元素的测定方法主要包括火焰原子吸收光谱法[3]和基于离子选择性电极的电解质分析技术[4]。 火焰原子吸收光谱技术需要乙炔燃气, 仪器不能便携, 对实验室条件要求较为苛刻; 电化学方法存在电极处理较为繁琐且需定期更换等缺点, 在很大程度上制约了分析效率。 因此, 医疗检验领域亟需建立新型、 高效且仪器简单的血清中锂元素的分析技术。
液体阴极辉光放电-原子发射光谱作为一种新颖的适宜液体样品金属元素分析的手段, 已有相应的应用报道, 并展现出良好的分析性能[5, 6, 7, 8, 9, 10]。 该技术在大气压下, 以进样溶液为一极, 金属为一极, 通过向电极间施加高压, 从而导致电极间的气体发生放电, 产生辉光放电等离子体。 放电过程中, 液体电极中的溶液不断被气化, 使得溶解在溶液中的金属离子也进入到等离子体中并被激发, 产生发射光谱, 从而实现溶液中金属离子的检测。
目前, 基于液体阴极辉光放电-原子发射光谱法的环境水中锂含量分析的方法研究也已有所涉及[11, 12], 但该技术尚未应用于医疗领域锂元素的检测中。 因此, 本文结合酸化、 直接稀释进样的方式, 采用自制便携液体阴极辉光放电-原子发射光谱仪, 建立了血清锂含量高灵敏测定的新技术。 该技术无需气体钢瓶, 且具备仪器便携, 操作简单, 分析效率高等优势, 在医疗患者血清中锂元素的监测领域具有广阔的应用前景。
实验用的硝酸为优级纯试剂; 实验用水均为二次离子交换水。
血清微量元素标准物质(Trace Elements Serium L-2), 挪威SERO公司。
实验用自制液体阴极辉光放电-原子发射光谱装置, 结构如图1所示。
本装置以试液作为阴极, 以金属钨为阳极, 在钨阳极和试液阴极之间施加一定电压, 两极间气体电离产生等离子体, 溶解在试液中的金属离子受热激发, 由光纤光谱仪采集锂元素在671 nm下的发射光谱。 自制液体阴极辉光放电-原子发射光谱仪器的条件参数如表1所示。
| 表1 液体阴极辉光放电光谱仪工作参数 Table 1 Working parameters of SCGD-AES |
标准系列: 由Li标准储备液(1 000 mg· L-1, 购自中国计量科学研究院), 逐级稀释至浓度分别为0, 0.1, 0.2, 0.3, 0.4和0.5 mg· L-1的系列, 保持标准系列硝酸浓度为1%(V/V)。
实验所需其他浓度标准试液也由储备液逐级稀释而得。
样品处理: 吸取血清样品0.25 mL, 加入50 μ L浓硝酸, 用去离子水稀释至5 mL, 此为稀释20倍的样品, 样品试液中硝酸浓度为1%(V/V)。
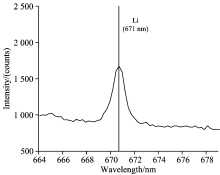
采用光纤光谱仪采集0.1 mg· L-1锂标准溶液在671 nm下的发射谱图, 如图2所示。 671 nm为锂元素的最强发射谱线, 且在发射峰附近未发现显著的光谱干扰。 因此, 本实验采用671 nm作为锂元素测定的分析谱线。
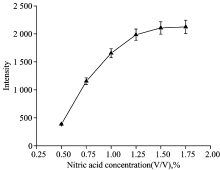
实验考察了试液在0.50%~1.75%(V/V)硝酸酸度对0.15 mg· L-1锂元素测定灵敏度的影响。 结果如图3所示, 在所选酸度范围内, 发射强度随酸度的增大而增大, 但当酸度大于1.00%(V/V)时, 发射强度增大趋势趋缓, 测试精度降低, 同时发现等离子体较难产生, 且等离子体稳定性趋于变差。 综合考虑, 实验采用1.00%(V/V)硝酸作为试液采用的酸度。
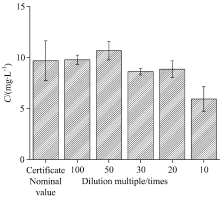
对血清标准样品[证书标称浓度(9.69± 1.95) mg· L-1]用去离子水进行10倍~100倍稀释, 测定锂元素含量, 结果如图4所示, 表明: 当稀释倍数在20倍以上时, 测定值在证书标称值范围内。 实验测试过程中, 在保证方法检出限满足待测样品检出要求前提下, 在稀释20倍以上的基础上, 应尽可能选取较高的稀释倍数。
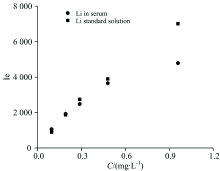
实验对比了锂浓度在0.1~1.0 mg· L-1水溶液基体和以血清稀释液为基体的试液在相同测试条件下的发射强度。
结果如图5所示, 随着血清稀释倍数的减小(浓度增大), 基体干扰趋于明显。 在0.5 mg· L-1(稀释倍数20倍)及以下浓度, 基体干扰不显著。 因此, 对血清样品应进行20倍以上的稀释, 以期尽可能消除基体干扰的影响。
对标准系列按照浓度从低到高进行测试, 以发射强度作为纵坐标, 以锂元素的浓度作为横坐标, 拟合得到工作曲线的线性方程, 为Ie=7 299ρ Li+400; R2=0.998 3, 其中, Ie为发射强度, ρ Li为锂标准溶液浓度。 以标准溶液11次测定的标准偏差的3倍对应的血清锂含量作为检出限。 当稀释倍数为20时, 血清Li的方法检出限为0.2 mg· L-1。 以样品6次平行测定的相对标准偏差考察方法的精密度, 结果均小于5%。
按照上述测定方法, 对血清微量元素标准物质(Trace Elements Serium L-2)进行测试, 平行测试3次, 取平均值。 测定结果如表2所示, 测试值为9.70 mg· L-1, 测定值在证书标称值允许范围内, 表明本方法应用于血清中锂含量的测定, 结果准确、 可靠。
| 表2 血清标准样品测试结果(n=3) Table 2 The results of determination for serum standard samples (n=3) |
建立了基于便携式液体阴极辉光放电-原子发射光谱装置测定血清样品中锂元素含量的新方法。 血清样品经硝酸酸化、 20倍以上稀释后, 直接导入自制便携液体阴极辉光放电装置放电室, 由光纤光谱仪采集血清中锂元素在671 nm发生波长下的光谱图, 实现血清中锂元素的定量测定。 本方法无需使用气体钢瓶、 占用实验室空间小、 可以实现仪器的便携化, 同时具备样品消耗量小, 分析灵敏度高、 速度快以及成本低等优异的分析性能及性价比优势, 可以较好地应用于医疗检验领域。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|