作者简介: 陈硕然, 1987年生, 苏州科技大学化学生物与材料工程学院教师 e-mail: chensr@mail.usts.edu.cn
Cu2+是人体正常代谢所必需的微量元素之一, 但是过量的Cu2+会造成代谢紊乱, 进而诱发各种疾病。 长期以来, 铜材料的过度使用和后处理不当导致生活环境中的Cu2+浓度超标, 成为重金属污染物之一, 因此生活环境中Cu2+含量的检测成为人们关注的热点。 基于荧光探针的荧光光谱法由于选择性好、 灵敏度高等优点被广泛应用于离子检测领域。 利用荧光探针分子与待检测离子可发生选择性的弱相互作用, 研究者们探索并设计了诸多可用于Cu2+检测的荧光探针。 然而普通的荧光探针由于灵敏度较差或选择性不理想等问题缺乏实际应用价值。 设计并合成了一种新的化学型荧光探针分子9,10-二(3’-羟基-4’-亚甲胺氨基硫脲苯基)蒽(b-HTPA)。 该探针分子通过与Cu2+的络合作用, 改变自身的电子排布结构, 使得其荧光性能发生显著变化, 由此对Cu2+产生灵敏的响应。 通过上、 下转换荧光光谱来研究b-HTPA对Cu2+检测的各项性能, 并结合拟合计算得出最终结果。 选择性研究结果表明, 相比其他13种金属阳离子, Cu2+对b-HTPA荧光猝灭效果最为显著, 空白探针分子荧光与加入Cu2+后的荧光强度比可达150∶1。 灵敏性研究结果表明, b-HTPA对Cu2+的最低检测限为2.78×10-7 mol·L-1, 远低于中国卫生部《生活饮用水卫生标准》(GB5749—2006), 表现出良好的荧光响应灵敏性和理想的最低检测限。 响应时间测试结果表明, b-HTPA与Cu2+在02 min时间范围内反应速率最大, 并在约10 min后反应完全, 说明b-HTPA在对Cu2+检测中可以短时间产生响应, 降低实际应用中的检测时间和周期。 还使用八乙基卟啉钯(PdOEP)作为光敏剂, 以b-HTPA为湮灭剂, 利用上转换荧光光谱对b-HTPA/PdOEP/Cu2+体系的灵敏性和检测限进行测试研究。 结果表明, 探针的上转换荧光强度随着Cu2+浓度的增加而降低, 具有良好的响应性, 通过拟合计算, 得出b-HTPA对Cu2+的检测限为3.78×10-6 mol·L-1, 低于《生活饮用水卫生标准》规定的检测下限。 设计合成的新型荧光探针分子9,10-二(3-羟基-4-亚甲胺氨基硫脲苯基)蒽对Cu2+具有高选择性、 高灵敏度和理想的检测限, 且响应速度快, 展现了上转换发光在检测领域具有应用潜力。
Cu2+ is one of the essential trace elements for human metabolism, while excess ingestion will cause metabolic disorders even diseases. However, Cu2+ has been elevated levels in living environment due to overuse and inappropriate reprocessing measures of copper, which makes Cu2+ one of the toxic heavy metal pollutions. Therefore, the continuous concern over Cu2+ pollution has been a hot issue and attracted interest in the detection methods for Cu2+. Fluorescent spectrometry based on fluorescence probe has been widely used in ion detection field owing to good selectivity and high sensitivity. So far, researchers have developed fluorescence probes for Cu2+ detection based on selectional weak interaction between probe molecules and ions to be measured. However, these strategies all involve selectivity or sensitivity drawbacks, making the probes difficult for practical applications. Here, we designed and synthesized a new molecule 9,10-bis (3’-hydroxy-4’-thiosemicarbazide) phenylanthracene (b-HTPA) as a fluorescence probe for Cu2+ detection. The electron configuration of b-HTPA would change through coordinating with Cu2+, which would cause the remarkable change of fluorescence property of the b-HTPA as responsiveness for Cu2+. Characterizations of the detection of b-HTPA for Cu2+ were mainly carried out by down/up conversion fluorescence spectral. Results of selectivity research showed that Cu2+ has the strongest fluorescence quenching effect compared with the other thirteen kinds of metal cations. Besides, upon addition of Cu2+about 150-fold decreasement of fluorescence intensity was observed compared to other metal cations. The results indicated the good selectivity of b-HTPA to Cu2+. Results of sensitivity research showed that the detection limit of b-HTPA to Cu2+ was 2.78×10-7 mol·L-1 which was much lower than the hygienic standard for drinking water (GB5749—2006), which indicated high fluorescent response sensitivity and ideal detection limit. The results of response time test revealed that interaction rate between b-HTPA and Cu2+ was very high in the first two minutes and completely reacted within ten minutes, which showed that b-HTPA could be capable of reacting intensively with Cu2+ in short time which may save detection period. Moreover, up-conversion fluorescence spectra were also used for the sensitivity evaluation of b-HTPA to Cu2+ with palladium(Ⅱ) octaetylporphyrin (PdOEP)as the sensitizer. The research results showed that intensity of up-conversion fluorescence obviously declined upon the addition of Cu2+ and the detection limit was 3.78×10-6 mol·L-1 which is also lower than the hygienic standard. This work designed and synthesized the 9,10-bis (3’-hydroxy-4’-thiosemicarbazide) phenylanthracene as a fluorescence probe for Cu2+ detection, and the probe was proved to have highly selective and sensitive. Moreover, the probe b-HTPA had ideal detection limit and short detection period, which gave it great potential in the field of Cu2+ detection.
铜是人体重要的微量元素之一, Cu2+在造血、 结缔组织构建、 神经系统维护等方面具有不可替代的作用, 但是过量的Cu2+会造成代谢紊乱, 甚至引发疾病[1]。 与此同时, 作为一种性能优良的金属材料, 铜材料被广泛应用于建筑、 机械制造、 医疗器械等领域[2]。 随着工业化进程的推进, 铜材料的过度使用和不当的后处理工艺, 导致高浓度的Cu2+逐渐出现在人们的生活区域, 尤其是生活用水, 成为重金属污染物之一[3]。 因此, 如何检测生活环境中的Cu2+含量吸引了众多研究者的关注[4]。
目前, 基于荧光分子探针的荧光光谱法由于选择性好、 灵敏度高、 响应快且操作简单的优点得到广泛应用[5, 6]。 荧光分子探针(简称荧光探针)能够与待检测离子发生选择性的弱相互作用或者络合等化学作用, 导致荧光分子结构改变, 从而引起分子的荧光性质(如荧光强度、 荧光位移和荧光寿命等)发生显著变化, 通过这种变化来实现对待测离子的检测[7, 8]。 基于分子识别的荧光探针, 不仅具有多种优点如极佳的选择性和高的灵敏度、 样品用量少、 检测方法快捷便利, 并且己经实现了对金属离子、 阴离子和有机生物活性分子的检测从而受到广泛关注[9]。
近年来, 研究者们基于上述原理探索并报道了多种可用于Cu2+检测的荧光探针[10]。 目前最常用的设计方法, 是利用探针分子与待检测离子发生选择性的弱相互作用, 如氢键、 配位键作用力, 引起探针分子荧光强度的改变来构建荧光探针[11]。 该类荧光探针通过与待检测离子之间可逆的作用力结合, 可以实现特定环境中待测离子的动态变化, 且原理和制作简单, 具有一定的应用价值。 但是, 该类探针分子与待测离子的结合容易被环境中诸如pH、 温度、 极性等因素干扰, 产生灵敏度低、 选择性差等问题, 极大的限制了该类荧光探针的应用[12]。
基于此, 更加稳定的反应型荧光探针被开发和设计出来。 利用探针分子与待检测离子之间的化学反应, 破坏探针分子原有的结构并形成新的化学结构, 改变探针分子取代基团的电子能力或者共轭程度, 从而改变探针分子/待测离子体系的荧光强度或者波长, 造成宏观颜色变化, 达到对离子检测的目的[13]。
上转换发光能够将长波长的光转换为短波长的光, 基于三线态-三线态湮灭机制上转换(TTA-UC)由于具有低的激发光能量阈值和高的上转换量子产率, 目前受到研究者的青睐[14]。 TTA-UC体系由三线态能量给体(光敏剂)与三重态能量受体(湮灭剂)构成, 其上转换机制经历多个微观通道过程: 光敏剂吸收低频光跃迁至单线态(1S* ), 经由系间窜越(ISC)通道形成三线态(3S* ); 而后经由三线态-三线态能量转移(triplet-triplet energy transfer, TTET)通道将能量传递给湮灭剂生成三线态湮灭剂(3A* ); 再通过三线态-三线态湮灭(TTA)产生激发单线态湮灭剂(1A* ), 最终跃迁回至基态, 并发出上转换荧光, 实现频率上转换[15]。
基于上述理论, 本文设计并合成了一种的新的化学型荧光探针分子9, 10-二(3’ -羟基-4’ -亚甲胺氨基硫脲苯基)蒽(b-HTPA), 通过紫外吸收光谱和上、 下转换荧光光谱来研究探针的光谱性质。 并选取其他13种阳离子作为参比, 确定b-HTPA对Cu2+的选择响应性; 配制不同浓度的Cu2+进行荧光检测, 分析和计算b-HTPA对Cu2+的灵敏性和检测限。 选择响应性和灵敏性研究结果表明, 新型荧光化学探针分子9, 10-二(3’ -羟基-4’ -亚甲胺氨基硫脲苯基)蒽能够应用于对重金属离子Cu2+的检测。
4-溴-2-羟基苯甲醛、 9, 10-二硼酸酯蒽、 1, 4-二氧六环、 无水乙醇和碳酸钾购于百灵威化学技术有限公司; 四(三苯基膦)钯(0)购于江苏强盛功能化学股份有限公司; N, N-二甲基甲酰胺(DMF)购于国药集团化学试剂有限公司; 无水硫酸钠、 乙酸、 石油醚购于上海润泽化学试剂有限公司; 氨基硫脲和氯化钠购于无锡晶科化工有限公司; 甲苯购于天津博迪化工有限公司; 二氯甲烷购于上海伊皮特化学试剂有限公司; 其他试剂, MnCl2, NH4Cl, ZnCl2, MgCl2, CdCl2, PbCl2, LiCl, NaCl, KCl, CaCl2, NiCl2, CoCl2, FeCl2, CuCl2均购于国药集团化学试剂有限公司。 所有试剂均为分析纯。 八乙基卟啉钯(PdOEP)购于Frontier公司。
AVANCE Ⅲ 型核磁共振谱仪(瑞士Bruker公司), INOVA400(EI)型质谱仪(瑞士Bruker公司), FA2004型电子天平(上海一言仪器仪表有限公司), U-3500型紫外-分光光度计(日立公司), FLS-920型荧光光谱仪(英国爱丁堡公司), SZCL-3B型磁力搅拌器(上海振华仪器公司), 上转换荧光用PR655型的SpectraScan光谱仪测量, 泵浦光源使用激光器代替(二极管泵浦固态型, 激发波长为532 nm, 60 mW· cm-2)。
1.2.1 9, 10-二(3-羟基-4-亚甲胺氨基硫脲苯基)蒽(b-HTPA)的制备
(1)在250 mL的三口烧瓶中加入4-溴-2-羟基苯甲醛(2.84 g, 14.19 mmol· L-1), 9, 10-二硼酸酯蒽(2 g, 4.73 mmol· L-1)溶于100 mL 1, 4-二氧六环和24 mL乙醇, 将K2CO3 (9.84 g, 69 mmol· L-1)溶于48 mL蒸馏水, 与上述溶液混合。 在混合溶液中鼓入氮气15 min, 随后加入四(三苯基膦)钯(0)(0.39 g, 1.2 mmol· L-1), 继续鼓入氮气5 min, 在氮气氛围中加热回流, 反应过程中通过点板跟踪反应进度, 展开剂为二氯甲烷∶ 石油醚=1∶ 1, 反应进行至48 h, 原料9, 10-二硼酸酯蒽的点几乎消失, 停止反应。
(2)反应结束后, 将反应溶液减压蒸馏后可得到黑色固体混合物, 选用二氯甲烷和饱和食盐水多次萃取分离有机相; 加入无水Na2SO4除水后, 使用柱层析法分离产物, 所用展开剂为二氯甲烷∶ 石油醚=1∶ 1, 再通过重结晶二次提纯, 得到黄色中间产物1.2 g, 产率为60%。
(3)称取上述中间产物(1 g, 2.39 mmol· L-1), 氨基硫脲(3 g, 7.17 mmol· L-1)溶于40 mL甲苯, 在混合溶液中鼓入氮气15 min, 随后加入5 mL乙酸作为催化剂, 在氮气氛围下加热回流, 反应过程点板跟踪, 反应进行24 h, 待中间产物的点几乎消失, 停止反应。 反应结束后, 将反应溶液减压蒸馏后得到固体混合物, 使用柱层析法分离产物, 所用展开剂为二氯甲烷∶ 石油醚=1∶ 1, 再通过重结晶二次提纯, 得到淡黄色产物0.5 g, 产率为37%。
1.2.2 光谱测试
探针光谱测试使用pH为7.0的HEPES作为缓冲溶液。 在3 mL比色皿中加入b-HTPA溶液(DMF∶ H2O=2∶ 1, V/V), 然后加入HEPES缓冲溶液, 使b-HTPA最终浓度为10 μ mol· L-1。
(1)紫外吸收光谱。 将装有2 mL b-HTPA溶液的比色皿与相同体积的HEPES缓冲溶液放入通过U-3500型紫外分光光度计进行紫外吸收光谱的测试。
(2)下转换荧光发射光谱。 将装有2 mL b-HTPA溶液的比色皿放入FLS-920型荧光光谱仪中, 选用波长为380 nm激光作为激发光源, 在入射光的垂直方向上对比色皿中缓冲溶液进行检测。
(3)上转换荧光发射光谱。 将装有2 mL b-HTPA溶液的比色皿放入光纤光谱仪槽中, 使用波长为532 nm激光作为激发光源, 在入射光的垂直方向上对比色皿中缓冲溶液进行检测。
1.2.3 b-HTPA对Cu2+选择性荧光光谱测试
配制Mn2+, N
1.2.4 b-HTPA对Cu2+灵敏性及最低检测限的测定与计算
不同Cu2+浓度溶液的配制: 使用1 mol· L-1 Cu2+溶液, 滴加至b-HTPA溶液体系, 配制成b-HTPA浓度为10 μ mol· L-1, Cu2+溶液分别为0.2 , 0.4, 0.6, 0.8, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 40, 60, 80和100 μ mol· L-1的混合溶液。
在DMF∶ H2O=2∶ 1(V/V, pH 7.0)测试体系中, 激发光波长为380 nm, 探针浓度为10 μ mol· L-1, 逐渐增加Cu2+的浓度测定其荧光发射光谱的变化。
最低检测限计算公式[16]
其中δ 为空白条件下的标准偏差; k为被测物浓度和荧光之间的线性关系斜率。
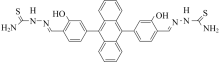
本文制备的b-HTPA结构式如图1所示。
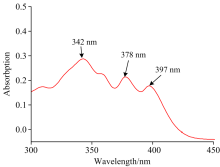
图2为b-HTPA(10 μ mol· L-1)在DMF∶ H2O=2∶ 1 (pH 7.0)溶剂中的紫外-可见吸收光谱图。 由图可知, 在DMF溶液中, 其吸收带分别为342, 378以及397 nm, 这是b-HTPA中蒽基团的电子振动所产生的特征峰, 其中342 nm处为叠加峰, 考虑到荧光测试结果的准确性, 本文选择380 nm作为荧光发射光谱激发光源。
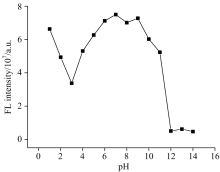
为了确定b-HTPA可应用的pH环境, 本文考察了探针(10 μ mol· L-1)的荧光强度随pH值的变化(测试条件: λ ex/λ em=380/440 nm)。 由图3所示, 可以观察到, pH值在13范围内, 荧光强度随pH值升高而降低; pH值在37范围内, 荧光强度随pH值升高而升高; pH值在79时, 荧光强度变化幅度较小; pH值在911范围内, 荧光强度随pH值升高而降低; 而pH值在1214范围内, 荧光已经发生猝灭。 其可能原因为随着H+浓度的变化, b-HTPA分子官能团电荷会发生一定程度的转移, 进而对荧光结构造成影响, 改变荧光发射能级, 影响分子的荧光特性。 由此可知, b-HTPA荧光强度可在pH值为69的较宽范围内保持稳定, 说明b-HTPA可以实现在生物细胞内Cu2+的检测应用。 因此, 本文选择了DMF∶ H2O=2∶ 1 (V/V, pH 7.0)作为溶液体系。
对目标金属离子的高选择性是检验探针分子能够作为该金属离子荧光探针的基本条件。
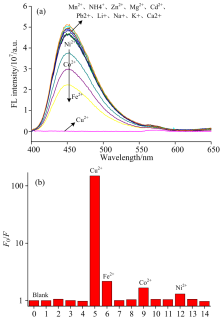
为了探究探针对Cu2+的选择性, 选取了包括Cu2+的14种阳离子进行荧光测试。 在相同检测条件下, 向探针溶液体系中分别滴加14种不同的金属离子, 配制成b-HTPA浓度为10 μ mol· L-1, 金属离子为100 μ mol· L-1的混合溶液, 进行荧光光谱测试, 如图4(a)所示。 不同金属离子混合溶液, 均检测出有不同强度的荧光, 而Co2+, Ni2+, Fe2+和Cu2+四种离子混合溶液引起不同程度的荧光猝灭行为, 其中Cu2+的猝灭效果最为显著, 几乎完全猝灭。
图4(b)为在条件相同的情况下, 空白b-HTPA荧光与加入14种不同金属阳离子的b-HTPA荧光强度之比(F0/F)。 从中可知, Cu2+对b-HTPA荧光的猝灭度达到150倍, 与之相比, 其他金属离子对b-HTPA荧光没有引发明显的猝灭或增强现象。 这是因为荧光探针本身的电子排布为D-π -D结构, 具有强荧光, 当Cu2+与b-HTPA发生络合后, b-HTPA变为A-π -A结构, 导致探针的荧光被抑制, 体系颜色变化明显, 由无色变为黄色, 发生荧光猝灭。 因此, 本文中b-HTPA对Cu2+有很好的荧光响应, 且对Cu2+表现出高选择性。
配制不同浓度Cu2+与b-HTPA(10 μ mol· L-1)混合溶液, 通过荧光光谱的分析, 研究b-HTPA对Cu2+的响应灵敏性, 并拟合计算最低检测限。
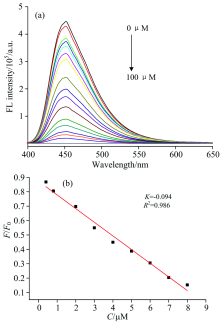
图5(a)为b-HTPA荧光强度随Cu2+浓度的变化图。 从图中可知, 随着Cu2+浓度的增加, 探针的荧光强度随之降低。 当Cu2+浓度≥ 40 μ mol· L-1时, 其荧光强度不再发生变化(猝灭度达到90%以上)。
图5(b)为b-HTPA/Cu2+混合溶液体系相对荧光强度F/F0随着Cu2+浓度的变化图。 本文选择了08 μ mol· L-1的Cu2+浓度范围, 对b-HTPA/Cu2+体系相对荧光强度F/F0进行拟合。 且在该浓度范围得出一条较好线性相关的工作曲线, 相关系数为k=0.094, R2=0.986。 δ 根据空白溶液的相对标准偏差计算得到, 数值为8.51× 10-3, 通过3倍信噪比方法计算, 依据公式3δ /k(k为矫正曲线的斜率)计算出了探针分子9, 10-二(3-羟基-4-亚甲胺氨基硫脲苯基)蒽对Cu2+的检测限为2.78× 10-7 mol· L-1, 远低于中国卫生部《生活饮用水卫生标准》(GB5749— 2006)。 因此, b-HTPA对Cu2+在中性缓冲溶液中表现出好的荧光响应灵敏性和较为理想的最低检测限。
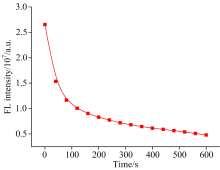
通过对b-HTPA/Cu2+体系的010 min时间范围的荧光响应测试, 研究了b-HTPA对Cu2+的响应时间问题。 图6是在探针(10 μ mol· L-1)溶液中加入Cu2+(100 μ mol· L-1)后, b-HTPA/Cu2+体系荧光强度变化图。 从图中可知, b-HTPA/Cu2+体系的荧光强度随着时间的增加而逐渐降低, 即发生荧光猝灭现象。 b-HTPA/Cu2+体系的荧光强度在02 min内急剧降低, 之后的荧光强度降低速率放缓, 约在10 min后基本上保持不变(猝灭度达到90%以上)。 说明b-HTPA与Cu2+在02 min时间范围内相互作用速率最大, 并在约10 min后反应完全, 且其反应产物的荧光强度之后的10 min都保持相对稳定, 表明该反应产物具有光稳定性。 这些结果表明, 9, 10-二(3’ -羟基-4’ -亚甲胺氨基硫脲苯基)蒽可以迅速与Cu2+反应完全。 且由于b-HTPA与反应产物的稳定性, 使得实验方法极为可靠。
通过下转换荧光光谱的研究, 本文确定了b-HTPA对Cu2+具有良好的荧光响应灵敏性和较为理想的最低检测限, 基于多种手段检测和研究的理念, 使用八乙基卟啉钯(PdOEP)作为光敏剂[17], b-HTPA为湮灭剂, 利用上转换荧光光谱对b-HTPA/Cu2+体系的灵敏性和检测限进行探索研究。
b-HTPA的上转换荧光强度随Cu2+浓度的变化趋势如图7(a)所示。 随着Cu2+浓度的增加, 探针的上转换荧光强度发生相应的降低。 图7(b)为Cu2+浓度为0100 μ mol· L-1时, 对b-HTPA/Cu2+体系相对荧光强度F/F0进行拟合得到的一条线性相关的工作曲线, 工作曲线相关系数为k=0.012, R2=0.954。 δ 为b-HTPA与光敏剂两种组分空白溶液的相对标准偏差, 测试计算得其数值为1.26× 10-2, 依据公式3δ /k(k为矫正曲线的斜率)计算出b-HTPA/PdOEP上转换体系对Cu2+的上转换检测限为3.78× 10-6 mol· L-1。 该检测限同样低于中国卫生部《生活饮用水卫生标准》(GB5749— 2006)中规定的检测下限, 可以应用于Cu2+检测领域。
设计并合成了一种新型荧光化学探针分子9, 10-二(3’ -羟基-4’ -亚甲胺氨基硫脲苯基)蒽(b-HTPA), 通过上、 下转换荧光光谱来研究b-HTPA对Cu2+检测的各项性能进行研究。 选择性研究结果表明, 相比其他13种金属阳离子,
Cu2+对b-HTPA荧光猝灭效果最为显著, 空白b-HTPA荧光与加入Cu2+后的荧光强度比可达150∶ 1, 证明b-HTPA对Cu2+具有高选择性; 灵敏性研究及检测限分析结果表明, b-HTPA对Cu2+的检测限为2.78× 10-7 mol· L-1, 远低于中国卫生部《生活饮用水卫生标准》(GB5749— 2006), 表现出好的荧光响应灵敏性和较为理想的最低检测限; b-HTPA响应时间测试结果表明, b-HTPA与Cu2+在02 min时间范围内相互作用速率最大, 并在约10 min后反应完全, 说明b-HTPA可以在短时间与Cu2+发生最强响应, 降低应用中的检测时间和周期。 上转换荧光光谱对b-HTPA/Cu2+体系的灵敏性和检测限的研究结果表明, 探针的上转换荧光强度随着Cu2+浓度的增加而降低, 具有良好的响应性, b-HTPA对Cu2+的检测限为3.78× 10-6 mol· L-1, 低于《生活饮用水卫生标准》规定的检测下限。 本文合成的新型荧光探针分子9, 10-二(3-羟基-4-亚甲胺氨基硫脲苯基)蒽对Cu2+具有高选择性, 高灵敏度和理想的检测限, 且响应速度快, 在Cu2+检测领域具有应用潜力。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|