作者简介: 杨 磊, 1979年生, 莆田学院环境与生物工程学院副教授 e-mail: yanglei7867245@163.com
为提高碳点对汞离子光化学识别的选择性及检测方法的可行性, 以柠檬酸和磺胺为原材料采用热解法制备一种新型氮、 硫共掺杂碳点(NS-CDs)。 用红外光谱仪、 紫外-可见光吸收光谱仪、 透射电镜、 元素分析仪和荧光光谱仪等对其结构和光学性能进行表征。 结果表明: 该量子点水溶性和分散性高, 平均粒径4.78 nm左右, 具有类石墨结构; 其在3 446和3 261 cm-1处存在N—C和O—H键振动吸收峰; 2 966和2 923 cm-1处为C—H键振动吸收带; 1 630和1 570 cm-1处吸收峰归属于苯环骨架C=C双键振动; 1 388 cm-1处为—CH3剪式振动峰; 1 268, 1 192, 1 146及1 071 cm-1处的振动吸收峰表明存在为C—N, C—S, C—O, C—O—C及—$SO_{3}^{-}$键, 912 cm-1处为环氧基的特征吸收峰, 739 cm-1处吸收带归属于N—H键变形振动, 可见, 该碳点不仅含有苯环骨架结构, 还有N和S等元素参与的成键结构存在。 其在21.4°处出现一个明显且宽的(002)晶面衍射特征峰, 晶格间距为0.41 nm, 稍大于石墨晶格间距(0.34 nm)。 NS-CDs的C, N, S和O元素含量分别为68.72%, 7.37%, 6.24%及17.67%, 与红外分析结果吻合。 NS-CDs在309 nm处有一个由C=C键的π→π*电子跃迁产生的较强吸收峰, 且在可见光区域内有一个很长的拖尾; 同时在335 nm处出现了一个由C=O键的 n→π*电子跃迁而产生的吸收肩峰。 当激发波长小于390 nm时, NS-CDs原液荧光发射峰值随激发波长增大而逐渐增大, 且在390 nm时, 荧光强度最强; 大于390 nm时, 随激发波长增大而逐渐减弱。 同时发现随激发波长增加, 发射峰逐渐红移。 当NS-CDs溶液逐渐稀释时, 其最佳激发峰也由390 nm蓝移至360 nm; 当pH值<11.0时, NS-CDs的荧光强度变化很小, 在pH值为7.0时荧光峰最强; 在pH>12.0时, 荧光强度急剧下降, 故选用PBS缓冲溶液(pH 7)进行金属离子检测实验。 在16种金属离子中只有Hg2+对NS-CDs荧光强度具有极其显著的影响, 使碳点荧光完全猝灭, 基于NS-CDs对Hg2+具有高选择性及Hg2+对NS-CDs强荧光猝灭作用, 建立了其对Hg2+的荧光化学识别方法。 该识别方法的线性方程为 y=5.559 02 x-13.860 39, 其线性范围为1×10-3~1×10-9 mol·L-1, R2为0.9947, 检出限为7.11×10-3 nmol·L-1, 相对标准偏差小于2.5%, 对实际样品检测精度和回收率高, 可用于实际水样中Hg2+的检测, 在生物和环境分析领域具有良好的应用前景。
To improve the selectivity of carbon dots to the photochemical recognition of mercury ions and the feasibility of its detection methods, a new kind of Nitrogen-Sulfur codoped carbon dots(NS-CDs)material with high fluorescence was prepared by thermal decomposition method and using citric acid and sulfanilamide as raw materials. Its structure and optical properties were characterized by infrared spectrometer, UV-Vis absorption spectrometer, transmission electron microscope, elemental analyzer, fluorescence spectrometer, etc. The results showed the quantum dot had graphite like structure, high water solubility and dispersibility, and its average particle size was about 4.78 nm. There are the following absorption peaks in the infrared spectra of NS-CDs: N—C and O—H bond vibrational absorption peaks at 3 446 and 3 261 cm-1, C—H bond vibrational absorption bands at 2 966 and 2 923 cm-1, the C=C double bond vibrational absorption peak of the benzene ring skeleton at 1 630 and 1 570 cm-1, shear vibration peak of —CH3 at 1 388 cm-1, the vibrational absorption peaks of C—N, C—S, C—O, C—O—C and —S
随物质需求不断丰富发展, 自然界对污染物的吸收和消纳严重不足, 如汞作为重金属的污染源之一, 毒性强而且危害持久, 尤其在自然界中不断富集累积, 最终通过食物链危害生态平衡和人类健康, 故对环境中汞离子实时检测具有重要意义[1]。 汞离子检测方法较多, 其中荧光光谱法[2]较紫外分光光度法[3]、 电化学法[4]、 原子吸收光谱法等具有快捷简便、 选择性好、 灵敏度高等优点。 而基于荧光量子点构建的Hg2+荧光传感法[5]具有光学稳定性好, 灵敏度高等特点, 其中荧光碳点(CDs)因量子产率与光稳定性高、 生物相容性好、 毒性低、 制备简便等优点, 倍受分析工作者关注[6]。 CDs制备方法有: 热处理、 激光灼蚀、 电化学氧化、 电弧放电、 超声及微波处理等[7, 8], 其中热处理法较常见, 如Miao[9]等通过热解柠檬酸和尿素制备一种可发射多色光的CDs; Karakoç ak等[10]用柠檬酸和乙二胺作原料采用微波辅助热解法制备了一种可用于生物标记的发红光的氮掺杂CDs; So. R C等[11]以柠檬酸和5-氨基-1, 10-邻菲罗啉作试剂采用一步水热法设计出新颖的氮掺杂多层核/壳结构能发出红、 绿及蓝三色光的AC-CDs。 关于CDs用于汞离子的测定已有文献报道[12, 13, 14, 15], 如Yu等[12]以柠檬酸和N-(2-羟乙基)乙二胺为原料采用微波辅助溶剂热法制备了荧光N掺杂碳点(N-CDs), 并制备了其接枝聚乙烯胺/聚丙烯酰胺荧光水凝胶膜, 该膜可检测Hg2+, 其检出限为0.089 μ mol· L-1; Sadeghinejad等[13]以柠檬酸、 尿素及硫脲为原料制备了可用Hg2+荧光传感器检测的CDs, 其线性检测浓度为0.1~20 μ mol· L-1, 检出限为62 nmol· L-1; Li等[14]采用微波辅助法制备了一种可用作Hg2+无标记荧光探针的氮硫共掺杂碳点(检出限为2 μ mol· L-1), 其也可用作活体细胞成像; Iqbal等[15]以柠檬酸和三聚氰胺为原料固相法制备了N-CDs, 基于其和Hg(Ⅱ )间强静电作用和电子转移, 当加入谷胱甘肽(GSH)后可制备出开-关-开光化学传感器, 对Hg2+和谷胱甘肽具有显著的高选择识别性能, 相应检出限分别为20和40 nmol· L-1。 尽管此类荧光碳点在Hg2+传感应用方面取得良好效果, 但构建一个选择性和灵敏度高、 检出限低的Hg2+传感器, 仍是人们所渴求的。
本研究以柠檬酸为前躯体、 磺胺作为氮和硫源, 通过热解法制备了一种新型氮、 硫共掺杂碳点(NS-CDs)。 基于该碳点具有良好的水溶分散性、 对Hg2+的高选择性及Hg2+对NS-CDs的荧光猝灭作用, 建立了一种测定Hg2+的新型光化学传感方法, 相比上述文献Hg2+检测方法具有高选择性, 检测线性浓度范围广和检出限低等优点。
Cary Eclipse分子荧光光谱仪, 美国瓦里安; TECNAI F30场发射透射电镜, 荷兰Philips公司; TENSOR27傅里叶型红外光谱仪, 德国BRUKER; UV2250紫外/可见分光光度计, 岛津制作所; XRD-6100 X-射线衍射仪, 岛津制作所; Vario EI Ⅲ 元素分析仪, 德国Elementar。
磺胺、 柠檬酸、 氢氧化钠、 氯化钙、 氯化镁、 氯化铜、 氯化钡、 氯化铬、 硝酸银、 氯化镍、 氯化锰、 硝酸铅、 氯化铁、 醋酸汞及汞离子标准溶液等均购自国药试剂, 均为分析纯; 3 500 Da透析袋购自上海源叶生物科技公司; 0.22 μ m水性滤膜由海宁市郭店桃园膜分离设备厂提供。
于烧瓶中称2 g柠檬酸与1 g磺胺放入200 ℃油浴中加热熔融, 由黄色变为橘黄色时停止加热反应后取出, 将其溶解于250 mL 10 mg· mL-1氢氧化钠溶液中, 用玻璃棒搅拌30 min, 再用水系0.22 μ m微孔滤膜过滤悬浮小颗粒, 将滤液用3 500 Da透析袋透析, 每8 h换1次水, 直至该系统稳定且外液面pH 7后, 将袋内浅棕黄色溶液倒入干净试剂瓶中, 即得氮、 硫共掺杂碳点(NS-CDs)原液。 将其置于4 ℃冰箱中保存备用。 并取适量NS-CDs溶液进行离心操作后冷冻干燥48 h, 得到固态样品, 研磨备用。
用红外光谱仪在4 000~400 cm-1测定NS-CDs的红外光谱; 用紫外-可见光谱仪在190~800 nm测其UV-Vis吸收光谱; 通过TEM在300 kV下对其进行微观形貌分析, 并用SigmaScan Pro4软件统计其粒径; 用Vario EI Ⅲ 元素分析仪对其进行元素分析; 使用X-射线衍射仪分析其结构, 其中CuKα 射线(λ =0.154 2 nm), 电压40 kV, 电流30 mA; 将NS-CDs原液、 稀释液及用于离子选择测定和Hg2+测定的待测液(用pH为7.0的PBS缓冲溶液调整pH至7.0)进行分子荧光光谱测定。
将1× 10-2 mol· L-1的Ca2+, Ag+, Cu2+, Mn2+, Zn2+, Sn2+, Mg2+, K+, Ni2+, Al3+, Cd2+, Ba2+, Pb2+, Na+, Hg2+, Fe3+等16种金属离子, 各取2 mL, 再加入2 mL NS-CDs原液, 摇匀放置10 min后, 在390 nm激发光和5 nm狭缝下, 测其荧光光谱, 并考察离子对NS-CDs荧光猝灭行为。
图1(a)是氮、 硫共掺杂碳点的透射电镜图及其粒径统计分布图(图1右上角的插图), 由图1(a)可见, 采用脱水缩合碳化法制备的NS-CDs具有量子点属性, 其平均粒径为(4.78± 0.98) nm, 并具有良好的分散性。 图1(b)为其高分辨透射电镜图, 该图表明NS-CDs呈现出间距为0.23 nm晶格结构, 该值与石墨的100衍射面接近[16], 可见所制备的NS-CDs具有类石墨的结构。
 | 图1 NS-CDs的TEM图(a)和其高分辨TEM图(b); 插图: 粒径分布图Fig.1 TEM image (a) and high resolution TEM image (b) of NS-CDs; Inset: particle size distribution diagram |
| 表1 NS-CDs的元素组成 Table 1 The elemental composition of NS-CDs |
采用红外、 XRD及元素分析表征NS-CDs的结构及组成。 由图2(a)知3 446和3 261 cm-1处对应N— C和O— H键振动吸收峰; 2 966和2 923 cm-1处为C— H键振动吸收带; 在1 630 cm-1处的吸收峰, 为官能团苯环骨架C=C双键振动峰及C=O双键振动吸收峰[17]; 1 570 cm-1处对应苯环C=C键振动吸收峰; 1 388 cm-1分别为— CH3剪式振动峰; 1 268, 1 192, 1 146及1 071 cm-1处的振动吸收峰表明存在为C— N, C— S, C— O, C— O— C及— $SO_{3}^{-}$键[17, 18], 912 cm-1处吸收峰为环氧基特征峰, 739 cm-1处归属于N— H键变形振动[19]。 可见, 该碳点不仅含有苯环骨架结构, 还有N和S等元素参与的成键结构。 图2(b)为NS-CDs的X-射线衍射图谱, 其在21.4° 处出现一个明显且宽的衍射特征峰, 可得(002)衍射峰的晶格间距为0.41 nm, 稍大于石墨晶格间距(0.34 nm), 可能为在碳点中引入N, S及含氧基团所致[20, 21]。 对NS-CDs的元素分析表明, 其C, N, S和O含量分别为68.72%, 7.37%, 6.24%及17.67%, 可见该碳点不仅含氮和硫, 也含氧元素。 这与红外分析的结果较吻合。
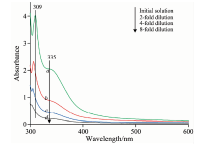
图3是NS-CDs的UV-Vis吸收光谱图。 由图3中起始溶液吸收曲线可见, 在309 nm处有一个较强的吸收峰, 这是由C=C键的π → π * 电子跃迁产生的, 且在可见光区域内有一个很长的拖尾[11]。 同时在335 nm处出现了一个吸收肩峰, 其为C=O键的n→ π * 电子跃迁而产生[22]。 研究中发现氮、 硫共掺杂CDs紫外-可见吸收光谱中π → π * 跃迁形成的吸收峰随溶液稀释倍数增大发生蓝移。
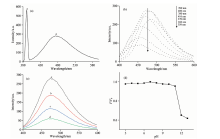
在狭缝狭缝宽度为5 nm时, 对氮、 硫共掺杂碳点的荧光光谱研究发现, 当激发波长为390 nm, NS-CDs原液荧光发射峰最强, 为280.1 a.u.[图4(a)]; 当激发波长< 390 nm时, 其峰值随激发波长增大而逐渐增大, 且在390 nm时, 其荧光强度最强; 当激发波长> 390 nm时, 荧光强度随激发波长增大而逐渐减弱。 同时发现随激发波长增加, 发射峰逐渐红移[图4(b)]。 这种依赖激发波长的荧光发射行为与炭点类文献报道的现象一致[23, 24]。 当NS-CDs原液逐渐稀释时, 其荧光峰值逐渐减弱, 且相应最佳激发峰也由390 nm蓝移至360 nm[图4(c)]。 配制pH值为3~13共计11个NS-CDs溶液并测其荧光强度, 结果如图4(d)所示。 图中F0为pH 7.0时样品的荧光强度, F为不同pH值样品的荧光强度。 由图可知, 当pH值< 11.0时, NS-CDs的荧光强度变化很小, 在pH值为7.0时最强; 在pH> 12.0时, 荧光强度急剧下降。 这可能因强碱性碳点表面的某些基团去质子化而引起[25]。 在金属离子检测应用中, 由于金属离子在溶液中水解, 使溶液pH值下降, 所以在实际检测中应控制好溶液pH值, 因此选用PBS缓冲溶液(pH 7, 10 mmol· L-1)进行金属离子检测实验。
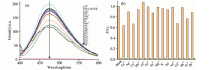
在任意一种离子检测实验中, 均会存在干扰离子对检测体系的影响。 因此, 为了考查NS-CDs对Hg2+的选择性, 实验选择了Ca2+, Ag+, Cu2+, Mn2+, Zn2+, Sn2+, Mg2+, K+, Ni2+, Al3+, Cd2+, Ba2+, Pb2+, Na+, Fe3+等15种离子对NS-CDs体系进行检测, 结果见图5(a)。 16种离子中只有Hg2+对NS-CDs荧光强度具有极其显著的影响, 使碳点荧光完全猝灭, 而另外15种离子中仅Al3+使NS-CDs荧光略有增强, Ca2+, Cu2+, Cd2+及Fe3+四种离子使其荧光稍有降低, 而其余离子对碳点荧光强度几乎无影响。
在相同浓度1× 10-2 mol· L-1干扰离子存在下, 以F/F0为纵坐标(其中F0空白样品的荧光强度, F为干扰离子存在下的荧光强度), 作干扰离子对NS-CDs检测汞离子荧光强度影响柱状图[图5(b)]。 由图5(b)可知, 除Ca2+, Cu2+和Cd2+对Hg2+测定有微弱的影响外, 其余离子不存在干扰。 可见, 本实验所制备的NS-CDs对Hg2+具有良好的选择性。 同时考察了不同阴离子的钠盐对Hg2+测定的影响, 发现所有阴离子对荧光均无影响, 进一步证明NS-CDs仅对Hg2+有选择性[26]。
分别取1 mL NS-CDs原液和1 mL的不同浓度的Hg2+溶液定容至10 mL, 配制出系列浓度Hg2+-NS-CDs溶液体系, 放置10 min待其反应充分后, 在390 nm激发光和5 nm狭缝下测其荧光光谱图, 见图6(a)。 由图6(a)可见, NS-CDs荧光峰值随Hg2+浓度降低而升高, 表明杂化碳点与Hg2+结合, 且Hg2+浓度越高, 猝灭效果越明显。 NS-CDs发生荧光猝灭的原理是由于Hg2+易与碳点表面的羧基、 氨基、 磺酸基等螯合形成复合物, 改变了碳点的电子结构及激子分布, 即通过有效的电子转移, 加速了导带的激发态电子和价带的空穴的无辐射重组, 导致碳点表面处于激发态的电子转移到了Hg2+的最低空轨道, 并以非辐射转移的方式在碳点表面返回到基态, 导致NS-CDs荧光强度急剧降低[27]。 鉴于NS-CDs对Hg2+具有高选择性及Hg2+对NS-CDs强荧光猝灭作用, 建立了其对Hg2+的荧光化学识别方法。
 | 图6 Hg2+浓度对NS-CDs荧光强度的影响(a)及Hg2+浓度与NS-CDs峰值曲线图(b)Fig.6 Influence of Hg2+ concentration on NS-CDs fluorescence intensity (a) and curve graph of between Hg2+ concentration and NS-CDs peak value (b) |
根据图6(a)作出Hg2+浓度与相应NS-CDs峰值曲线图[图6(b)], Hg2+浓度在10-3~10-9 mol· L-1时, 其浓度负对数与碳量子点荧光峰值呈线性关系[图6(b)], 其线性方程为y=5.559 02x-13.860 39, R2为0.994 7, 其中, y为荧光强度, x为lg[c(Hg2+)]。 标准偏差SD为1.317× 10-10, 检出限的计算公式D=3SD/K=7.11× 10-2 nmol· L-1。 本实验构建的Hg2+传感器与有关文献[28, 29]报道的Hg2+的荧光碳点传感器相比, 具有检出限低和线性范围宽等优点。
为了考察本实验所建立的NS-CDs对Hg2+浓度检测方法的可行性, 先用0.22 μ m微孔滤膜对自来水、 矿泉水及芳名湖水先进行过滤, 再在5 000 r· min-1下离心1 h除去水样中悬浮小颗粒, 发现水样中并无Hg2+存在。 对样品进行加标处理, 检测结果详见表2。 加标回收率和相对标准偏差分别在98.3%~101.0%和1.27%~2.12%之间, 表明水样中存在的离子和杂质不干扰Hg2+测定。 可见此方法可用于实际水样中Hg2+的测定。
| 表2 水样中Hg2+的分析结果 Table 2 Analytical results of Hg2+ in water samples |
以磺胺作为氮源和硫源, 成功制备了氮、 硫共掺杂碳点(NS-CDs)。 该NS-CDs具有类石墨结构及良好的分散性, 平均粒径为(4.78± 0.98) nm。 该碳点对Hg2+具有良好的选择性。 实验依据Hg2+对NS-CDs的荧光猝灭作用建立了一种新型光化学检测Hg2+离子的新方法, 其线性方程为y=5.559 02x-13.860 39, 具有识别线性浓度范围广和检出限低的优点。 该碳点制备方法简单, 可用于实际水样中Hg2+的检测, 在生物和环境分析领域具有良好的应用前景。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|