作者简介: 王玉田, 1952年生, 燕山大学电气工程学院教授 e-mail: y.t.wang@163.com
农药的广泛使用是防治病虫害的一种必要手段, 在保证农业增产增收的同时, 也给人们健康带来了威胁, 寻求更加灵敏的农药残留检测方法至关重要。 三维荧光光谱分析法选择性好、 灵敏度高、 快捷、 取样少, 可用于农药残留的分析与检测中。 以自制标准浓度的克百威农药溶液作为测试样本, 乙腈为溶剂, 利用荧光光谱仪对样本进行测量, 将实验获得的三维数据用MATLAB进行处理获得其三维荧光光谱图。 实验发现乙腈作为溶剂对实验影响不大且荧光光谱的强度与克百威溶液浓度呈现良好的线性关系, 相关系数 r=0.997 4, 接近于1。 因此三维荧光光谱分析法可以检测出克百威溶液的浓度以及农药的含量。
As a necessary means of preventing and controlling diseases and insect pests, the widespread use of pesticides has brought great threat to the people’s health, so finding some more sensitive methods of pesticide residues is of great significance. Fluorescence spectrometry has the advantages of good selectivity, high sensitivity, quick sampling and less sampling. It can be used in the analysis and detection of pesticide residues. In this paper, Carbofuran of self-made standard pesticide solution concentration as test samples, acetonitrile as solvent were measured on samples by fluorescence spectrometer, 3D datas will be obtained by MATLAB to get the 3D fluorescence spectra. The experimental results show that using acetonitrile as solvent has little effect on the experiment and the intensity of the fluorescence spectrum has a good linear relationship with the concentration of carbofuran solution. The coefficient of correlation R2=0.997 4 and it is close to 1. So it is a feasible and reliable method to detect the carbofuran pesticide with the three-dimensional fluorescence spectrometry.
农药的使用在防治农作物的病虫害、 保障农作物的生长方面起到重要作用的同时, 也给目前的生态环境发展带来了威胁[1, 2, 3]。 所以强化对食品中农药残留的检测与控制、 提高检测农药的速度和检测结果的精密度, 对保障人们自身的健康、 维护生态环境来说是极其重要的。
检测农药残留的比较有代表性的方法有有活体检测法、 气液色谱法、 生物传感器法和免疫分析法[4, 5, 6], 这些检测方法具有准确度较高、 检测较为灵敏等优点, 但它们存在耗时长、 测试成本高、 前期操作复杂和难以满足实际检测相关要求方面的不足。 而采用荧光光谱法进行检测, 具有检出限低、 检测选择性好、 灵敏度高等特点, 尤其适用于同时对多种微量农药进行检测, 成为了目前用于农药残留检测的一个研究的热点[6, 7, 8, 9]。 本文将实验获得的三维数据用MATLAB进行处理获得三维荧光光谱图, 发现荧光光谱的强度与克百威溶液浓度呈现良好的线性关系, 因此用三维荧光光谱检测克百威农药含量是可行的。
当某一波长的入射光照射到分子结构不同的物质的时候, 该物质会吸收一定波长的能量, 并随后发出一定的特定波长的光谱
式中: h为普朗克常数; λ 为物质所吸收的入射光波长; ν 为物质所吸收的入射光频率; c为光在真空当中的传播速度; E1为吸收能量以后所达到的较高能级; E0为物质处在基态时的能级。
在自然界中, 并不是所有物质分子受到激发后都能产生相应的荧光光谱。 即使有些物质能发出荧光, 但由于发出荧光的强度不大, 检测难度较大而导致其无法应用于实验中, 故只有那些能少数能发出极强荧光的物质才能用于荧光光谱的分析。
物质分子是否能发射出荧光光谱, 以及该物质所发射荧光光谱的强弱大小主要是由该物质本身的分子结构来决定, 但除此之外, 该荧光光谱的强度也会受到众多外界因素的影响, 如温度、 溶液酸碱性、 介质、 溶剂和散射光等。 详细的了解并掌握这些因素的对实验影响, 充分利用其中有利的并且尽量规避不良因素对测试的影响, 会极大的提高分析实验数据的准确度。
样品使用Edinburgh Instruments 公司生产的FS-920荧光分光光度计进行测试, 测定波长范围200~900 nm; 克百威农药(北京凯利农生物科技有限公司)作为溶液, 乙腈(武汉江北试剂有限公司)为溶剂。
实验所用的克百威标准溶液采用乙腈作为溶剂进行配置, 具体方法为: 先配置标准浓度为200 μ g· mL-1的克百威溶液, 使用电子分析天平准确的称取0.050 0 g的克百威标准样品, 再用无水乙腈进行溶解, 最后将溶解的克百威-乙腈溶液转移到250 mL的容量瓶中, 定容后进行摇匀, 放于冰箱中保存。 使用时取一定量的该溶液, 以乙腈为溶剂, 分别将其稀释成为浓度为4.0, 3.0, 2.0, 1.0, 0.50, 0.30, 0.20, 0.10, 0.05和0.025 μ g· mL-1这十组不同浓度的溶液。
实验主要采用三维荧光光谱分析法, 是一种三维的立体荧光矩阵。 光谱曲线图中X轴代表该物质荧光的发射波长, Y轴代表该物质荧光的激发波长, Z轴代表对应的荧光光谱的强度。 该荧光光谱图主要描述了物质荧光强度随发射波长和激发波长变化的三维变化关系。 通过该三维图, 可以直观的看出不同物质的荧光特征峰的高度、 峰面积、 峰位置和峰斜度等荧光信息。 而等高图则是三维荧光光谱的另外一种表达方式, 该表示方式是用线将荧光强度相等的点连接起来, 从而形成一个在以发射波长为X轴、 激发波长为Y轴的二维平面上的闭合曲线, 该闭合等高曲线的内层代表荧光光谱特征峰所在的位置, 曲线由内向外, 代表对应荧光强度的逐渐减小。 较之二维的荧光光谱, 三维荧光光谱具有选择性好、 灵敏度高、 重现性更好的优点, 并且在光谱重叠的情况下可以进行多组分的分析。
进行荧光测试的具体步骤为: 分别将不同浓度的克百威溶液滴入规格为1 cm× 1 cm的石英比色皿当中, 再放进荧光分光光度计中测量。 测试波长范围为200~900 nm, 仪器的发射和激发狭缝设定为0.25 nm, 测试时实验温度控制在20 ℃左右。
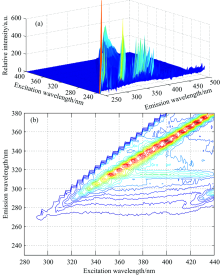
分别将浓度为3.00 μ g· mL-1和浓度为0.025 μ g· mL-1的克百威溶液置于荧光分光光度计中进行测量, 并将测试的数据采用MATLAB软件进行绘制, 如图1和图2所示。
 | 图1 浓度为3.00 μ g· mL-1克百威溶液三维荧光光谱图Fig.1 Three dimensional fluorescence spectrum of carbofuran solution with concentration of 3.00 μ g· mL-1 |
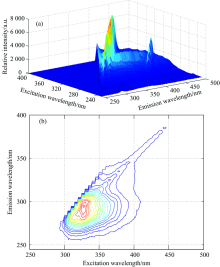 | 图2 浓度为0.025 μ g· mL-1克百威溶液三维荧光光谱Fig.2 Three dimensional fluorescence spectrum of carbofuran solution with concentration of 0.025 μ g· mL-1 |
每组图的(a)为三维立体图, (b)为等高图。 在三维立体图中, 激发波长为x轴, 发射波长为y轴、 荧光强度为z轴。 在等高线图中, 则通常是采用平面图来进行表示的, 其中激发波长为x轴, 发射波长为y轴。 两种克百威溶液虽然浓度不同, 但它们在特征吸收峰上都存在相同的地方。 从x轴的激发波长来看, 随着激发波长的不断增加, 荧光强度先增大后减小, 在280 nm处, 其对应的物质的荧光光谱强度出现最大; 从y轴的发射波长来看, 同样随着发射波长的不断增加, 其荧光强度也呈现先增大后减小的趋势, 在波长为305 nm处对应荧光光谱强度最大, 所以实验选用激发波长为280 nm、 发射波长为305 nm作为最佳吸收波长。
克百威的名称为2, 3-二氢-2, 2-二甲基-7-苯并呋喃, 该物质属于典型的甲氨基甲酸酯类物质, 其结构为典型的芳香化合物结构, 故存在π → π * 的跃迁, 再加上酚酯结构的存在, 故同样也存在n→ π * 的跃迁。 同时该分子中存在一个刚性的平面和给电子基— OR等的影响, 能极大的增强该物质对应的荧光光谱强度。
实验所用克百威废水是配置浓度不同的标准克百威溶液, 以便验证克百威溶液浓度与荧光光谱的关系。 分别将浓度不同克百威溶液置于荧光分光光度计当中, 并以280 nm的最佳激发波长和305nm左右的最佳发射波长来进行实验测试, 其相关的测试数据如表1所示。
| 表1 克百威溶液浓度及其测定的荧光强度 Table 1 Concentration of carbofuran solution and the fluorescence intensity |
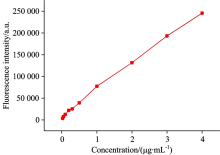
将表1中的数据用Origin 8.0软件将其绘制出以乙腈作为溶剂、 克百威荧光强度随该溶液浓度变化的关系曲线图(图3), 可以清楚的看出在测试的浓度范围中, 克百威的荧光强度基本上与其浓度呈线性关系。
与其他的分光光度法测量一样, 在进行荧光光谱分析时, 也要求溶剂对实验的影响较小。 由于克百威是典型的芳香烃有机物, 分子量大, 分子的极性小, 而水为强极性分子, 按照“ 相似相溶” 规律, 其在水中的溶解度较小, 故通常在溶解克百威物质时使用的是有机溶剂, 在查阅大量的文献资料的基础上, 确定选用乙腈作为本实验中的溶剂。 不加除荧光物质克百威之外的所有物质, 在荧光分光光度计中对该溶剂进行荧光光谱测试, 测试的数据使用MATLAB软件进行绘制, 如图4所示。
乙腈在发射波长为380 nm左右, 激发波长为350 nm左右, 其对应的荧光光谱强度为310, 而在其他的位置则其荧光强度相对较低, 其中在激发波长为280 nm左右, 发射波长为305 nm左右处, 乙腈的荧光强度为205。 乙腈的荧光吸收对实验的影响干扰较小, 因此选用乙腈作为溶剂。
扣除掉溶剂乙腈的荧光吸收后得到表2中的数据, 采用Origin软件进行作图, 绘制出克百威— 乙腈的标准工作曲线图, 如图5所示。
| 表2 消除空白后克百威溶液浓度及其对应的荧光强度 Table 2 The concentration of carbofuran solution and the corresponding fluorescence intensity after elimination of blank |
乙腈作为溶剂, 克百威溶液的回归方程式为
经过分析, 该回归方程的线性相关系数为
该线性系数R2非常接近于1, 符合朗伯-比尔定律。
分析三维荧光光谱图得知, 克百威溶液在最佳激发波长为280 nm、 最佳发射波长为305 nm时测得对应物质的荧光光谱强度最大, 配置不同浓度的克百威溶液, 用荧光分光光度计测试荧光强度后发现, 在浓度为0.025~4 μ g· mL-1范围内, 克百威溶液的浓度与其荧光强度成正比, 且乙腈作为溶剂对于实验干扰忽略不计, 因而采用三维荧光光谱可以分析克百威溶液的浓度以及农药的含量。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|