作者简介: 陈 琢, 1993年生, 内蒙古大学化学化工学院硕士研究生 e-mail: 792287062@qq.com
使用浊点萃取的方法分离富集水环境中痕量的锰离子, 创新性地使用钙羧酸(CCA)与阳离子表面活性剂氯代十六烷基吡啶(CPC)为络合剂与锰离子形成更稳定的三元络合物, 以TritonX-114为萃取剂浊点萃取分离富集水环境中的痕量锰, 同时采用火焰原子吸收法进行测定, 建立了测定水环境中痕量锰的新方法。 对影响浊点萃取的主要因素如pH、 TritonX-114的用量、 CCA用量、 CPC用量、 NaCl用量、 共存离子影响、 加热温度、 加热时间、 离心时间、 冰浴时间进行了优化。 在优化的实验条件下, Mn2+-CCA-CPC体系分离富集锰有很好地效果, 能够很好的克服基体干扰, 浊点萃取体系在锰含量0.3~1.5 mg·L-1时呈现良好的线性关系。 方法的灵敏度为1.939 mg·L-1, 精密度为0.39%, 检出限为(3 σ)0.27 μg·L-1。 测定自来水与井水中的锰含量的结果为33.5和64.5 μg·L-1, 同时做加标回收实验, 回收率在99.1%~101.5%之间。 符合国际标准, 因此该方法能够成功应用到水环境中的锰含量的测定, 结果令人满意。
In this work, a simple and novel cloud point extraction (CPE) method for the separation and preconcentration of manganese in aquatic environment was developed and combined with flame atomic absorption spectrometry (FAAS). Manganese was formed a complex with Calcon carboxylic acid (CCA) in the presence of Cetyl pyridinium chloride (CPC) and Triton X-114. The main factors affected the CPE, such as pH, the dosage of Triton X-114, CCA, CPC, NaCl, coexisting ions, and the heating time and heating temperature. After optimization of the experimental conditions, the system of Mn-CCA-CPC was able to overcome the matrix interference and showed the significant effect of separation of enrichment. The precision of the method was 0.39% and the limit of detection was 0.27 μg·L-1 of Mn. The results of the determination of manganese content in tap water and groundwater were 33.5 and 64.5 μg·L-1, which was in line with the international standards, so the method can be successfully applied for the determination of manganese in the water environment.
样品的预处理是一个比较困难的问题, 它既要求有较高的分析技术又要求要有着熟练操作的专业技术人员。 因此, 寻找一种操作简单、 价格便宜、 方法稳定又快速新的预处理技术成为分析化学中重要的研究内容[1, 2, 3]。 浊点萃取技术是最近新出现的一种新型的液-液萃取技术, 它具有不使用有毒有害的有机溶剂, 有着所用试剂价格便宜、 萃取率高、 富集倍数大等特点, 因此浊点萃取是一种很有发展的预处理技术[4]。 随着工业化的快速发展, 越来越多的有毒重金属离子排放到了水环境中[5]。 锰是一种对于人类健康起着重要作用的微量元素, 对于人体发育、 新陈代谢、 抗老化系统都起着非常重要的作用。 然而过多锰元素的吸收会引发DNA突变、 神经上的错乱、 幻听、 抑郁症、 终生残疾和极端的疾病[6, 7, 8]。 因此, 精确地检测出环境中锰的含量成为了必须要研究的问题。 许多研究技术可应用到检测锰离子的含量, 包括火焰原子吸收法[9]、 原子捕获火焰原子吸收法[10]、 直流电极谱法、 示差脉冲极谱法等。 本文创新性地应用Mn2+-CCA-CPC三元体系以浊点萃取方法分离富集水样中痕量的锰离子, 用原子吸收光谱法进行检测。
东西AA7003型原子吸收光谱仪(北京东西分析仪器有限公司), 配有锰的空心阴极灯; PHSJ-4F型pH计(上海仪电科学仪器股份有限公司); SB-5200DT超声波清洗机(宁波新芝生物科技股份有限公司); TLE204E电子分析天平(德国赛多利斯公司); TG1850-WS台式高速离心机(湖南赛特湘仪); SHA-B恒温数显振荡器(上海比朗仪器有限公司)。
锰标准储备液: 1.0 g· L-1, GBS G 62019— 90(2502), 国家钢铁材料测试中心; 锰标准使用液: 100 mg· L-1, 用1%硝酸-乙腈溶液稀释备用; 3× 10-3mol· L-1 CCA(钙羧酸)溶液: 用95%的乙醇溶解待用; 5% TritonX-114(曲拉通X-114)溶液(V/V); 3× 10-3 mol· L-1 CPC(氯代十六烷基吡啶)溶液; 20% NaCl 溶液(W/V); 缓冲溶液: 0.1 mol· L-1 Na2CO3与0.1 mol· L-1 NaHCO3溶液; 乙腈溶液。 所用试剂均为分析纯, 水为二次去离子水。
向50 mL的离心管中分别加入100 mg· L-1锰标准液50 μ L, 0.3 mL 5%(V/V)的TritonX-114溶液、 0.8 mL 3× 10-3 mol· L-1的CCA溶液、 1 mL 20%(M/V)的NaCl 溶液、 1 mL 3× 10-3 mol· L-1的CPC溶液, 用Na2CO3-NaHCO3缓冲溶液在pH计上调pH等于9.5, 稀释至50 mL, 并将离心管放至60 ℃的恒温水浴中加热35 min后, 以3 000 r· min-1离心5 min, 离心后冰浴8 min。 冰浴完成后弃去上层水相, 所得表面活性剂富集相用0.5 mL的硝酸-乙腈溶解, 并用二次去离子水将其定容至5 mL的比色管中, 用火焰原子吸收分光光度计测定其吸光度值, 同时做空白实验。
收集的水样用0.45 μ m的滤膜过滤, 分别取30 mL的自来水和井水样品于50 mL的离心管中, 向其中加入0.3 mL 5%(V/V)的TritonX-114溶液、 0.8 mL 3× 10-3 mol· L-1 的CCA溶液、 1 mL 20%(M/V)的NaCl溶液、 1 mL 3× 10-3 mol· L-1的 CPC溶液, 调pH为9.5, 按1.3所述实验方法进行操作。
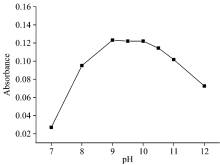
浊点萃取实验中, pH对于金属螯合物的形成以及之后的萃取过程起着至关重要的作用。 根据上述实验方法1.3对1 mg· L-1的锰进行浊点萃取, 将体系的pH分别调至7, 8, 9, 9.5, 10, 10.5, 11和12。 结果如图1所示, 选择体系pH在9~10时, Mn2+的回收率最大, 同时pH为9.5之后达到平台期, 故将体系的pH调至9.5。
根据实验方法1.3对同浓度的锰经浊点萃取, 分别选取TritonX-114的用量为0.1, 0.2, 0.3, 0.4, 0.6, 0.8和1.0 mL, 实验结果见图2, 当TritonX-114用量为0.3 mL时体系的回收率最大, 因此体系TritonX-114用量为0.3 mL。
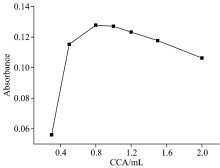
采用单一变量法, 据1.3, 只改变CCA用量, CCA取样量为0.3, 0.5, 0.8, 1.0, 1.2, 1.5和2.0 mL。 由图3分析可得, 当CCA的用量为0.8 mL时, Mn2+的回收率达到最大。
选用NaCl为盐析剂, 实验方法同上, 讨论其用量在0.3~3.0 mL时对锰回收率的影响。 实验结果如图4, 当NaCl的用量为1.0 mL时对锰的回收效果最好, 故该体系选择20%(MV) NaCl的用量为1.0 mL。
讨论三种不同阳离子表面活性剂的用量对体系回收率的影响, 实验方法如1.3, 依次研究了CPC, CTMAB和DDBAC的用量在0~2.5 mL时对该体系1 mg· L-1的锰回收率效果的影响。 结果见图5, 通过对比得出应用阳离子表面活性剂与钙羧酸比单纯应用钙羧酸做螯合剂效果更好, 故选用CPC作为阳离子表面活性剂对锰离子的回收效果最好, 同时由图5所示CPC的用量为1.0 mL时回收率最大。 因此, 本体系确定CPC为阳离子表面活性剂且取样量为1.0 mL。
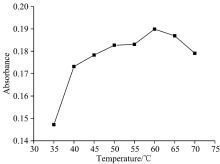
温度对于浊点萃取的影响尤为重要, 根据实验方法1.3体系研究温度在25~70 ℃之间体系回收率的变化, 结果见图6, 当温度在60 ℃时, 锰的回收率最大, 故选用60 ℃为体系的最佳温度。
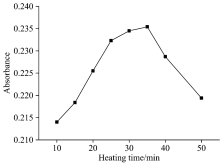
不同的加热时间对锰回收率有着很大的影响, 故根据实验方法1.3, 实验探讨加热时间从10~50 min时对锰回收率的影响。 结果表明, 当加热时间35 min时, 锰的回收率最大。
根据1.3实验方法, 讨论离心时间为2~12 min时离心时间对锰的回收率的影响。 由图8得知, 离心时间对锰离子回收率的影响不大, 在4~6 min时对锰的回收效果最好, 且当选择时间为5 min时对锰的回收率最大。 因此, 该体系选择的离心时间为5 min。
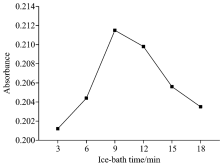
根据实验方法1.3, 讨论了冰浴时间从3~18 min对锰离子的回收率的影响, 实验结果见图9, 当冰浴时间为8 min时体系的回收率最大, 故选择的冰浴时间为8 min。
经浊点萃取会得到黏稠的有机相, 得到的有机相会对检测信号产生影响。 因此有机相需要一定的试剂将其溶解, 讨论了1:9(V/V)硝酸-甲醇、 硝酸-乙醇、 硝酸-乙腈以及浓硝酸、 甲醇、 乙醇、 乙腈对测定信号的影响, 实验结果如图10, 选用硝酸-乙腈溶解有机相时, 吸光度较好。
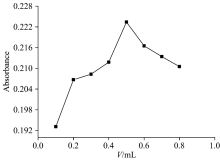
将两相分离后, 得到的有机相用硝酸-乙腈溶液溶解, 但不同硝酸-乙腈的用量会对有机相的溶解产生影响。 体系讨论了硝酸-乙腈的用量在0.1~0.8 mL时对有机相溶解的影响。 实验结果如图11, 当硝酸-乙腈的用量在0.5 mL时, 锰的回收率最大, 故有机相用0.5 mL的硝酸-乙腈溶解。
浊点萃取法测定1.0 mg· L-1的锰时, 存在大量以下离子时锰离子的回收率可达到95%以上对该体系不产生干扰(以mg· L-1计): Al3+(200), Ni+(200), Ba2+(200), Pb2+(200), Ag+(160), Cu2+(100), Co2+(40), F-(200), Br-(200), S
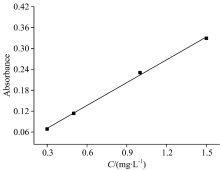
通过研究上述变量所得体系的最优实验条件, 在5个50mL的离心管中分别加入浓度为100 mg· L-1的锰标准使用液0, 30, 50, 100和150 μ L, 按1.3实验方法浊点萃取后测定其吸光度, 绘制工作曲线见图12。 实验结果表明, 锰含量在0~1.5 mg· L-1时呈现良好的线性关系, 线性回归方程为A=0.202 35c+0.002 24(r=0.999 4), 同时测定浓度为1 mg· L-1的锰和空白溶液的吸光度13次。 结果表明该方法的精密度为0.39%, Mn2+的检出限(3σ )为0.27 μ g· L-1。
对自来水和井水样品按照1.3实验方法进行测定, 并同时做加标回收实验。 实验结果见表2, 测得自来水与井水中锰的含量为33.50和64.50 μ g· L-1。
| 表2 水样中锰含量的分析及加标回收实验(n=6) Table 2 Manganese found in water samples and test for recovery (n=6) |
实验结果表明, Mn2+-CCA-CPC三元浊点萃取体系能成功应用到测定水环境中的痕量锰, 从实验结果可以看出本文成功地以CCA、 阳离子表面活性剂CPC为络合剂, 相比于传统的只用CCA为络合剂富集效果更好、 回收率更高。 通过大量实验数据得出形成三元络合体系更稳定, 富集效果更好, 大量存在的阴阳离子没有干扰, 对几乎痕量重金属离子都有很好的回收率。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|