作者简介: 毕卫红, 女, 1960年生, 燕山大学信息科学与工程学院教授 e-mail: bwhong@ysu.edu.cn
采取标准锌显色剂与锌发生显色反应, 生成不溶于水的絮状络合物。 用光谱仪测它的吸光度, 研究其特征谱与吸光度的特点, 建立其浓度与特征波长吸光度间的数学模型。 本文所采用的显色剂主要与锌、 铜、 镉、 镍四种离子发生络合反应。 因此分别探索了四种离子高浓度以及低浓度时显色反应的吸光度, 最终通过得到锌离子浓度与吸光度的关系式以及锌离子浓度与四波长下四种离子混合溶液显色后的吸光度的关系式, 给出了锌离子的吸光度与总吸光度的关系式。 显色反应能否满足分光光度法的要求, 主要与显色剂的性质有关, 同时显色反应的条件也至关重要。 因为在显色反应过程中, 主要是锌离子与锌显色剂发生络合反应形成络离子, 进而形成絮状络合物。 络离子一般比较稳定, 但在水溶液中也存在着电离平衡, 也就是说当显色条件发生变化时, 既有可能形成络离子, 也有可能发生络离子的分解, 从而影响络合反应的程度。 显色条件包括显色剂用量、 pH值、 反应温度、 显色时间、 待测溶液的盐度以及浊度等。 重点研究待测溶液的盐度对锌离子浓度测量值的影响, 并通过实验给出影响规律以及校正模型。
In this paper, the standard zinc coloring reagent and zinc color reaction result in water-insoluble flocculent complex. In addition, the absorbance was measured by spectrophotometer, the characteristic spectrum and the absorbance were studied, and the mathematical model was established between the concentration and the absorbance of characteristic wavelength. In this paper, color reagent mainly makes complexing reaction with zinc, copper, cadmium, nickel ion, so this study mainly explores the absorbance of four kinds of ions, such as high concentration and low concentration. Finally, through capturing the relationship between the concentration of zinc ions and the absorbance of the zinc ion, and getting the relationship between the concentration of zinc ions and the absorbance of the zinc ion as well as the absorbance of the four kinds of ions with four wavelengths, the relationship between the absorbance and the total absorbance of the zinc ion is given. During the experiment, the color reaction can meet the requirements of spectrophotometry, which is mainly because of the nature of the reagent, while the color reaction conditions are also essential. In the color reaction process, it is mainly zinc ions and zinc coloring agent complexation react to form complex ions, and flocculent complex. The ion is generally stable, but there is also ionization balance in the aqueous solution, that is when the color conditions change, the formation of complex ions may also occur in the decomposition of complex ions, thus affecting the degree of complex reaction . Color conditions include the amount of reagent, PH value, reaction temperature, color time, the salinity of the solution and turbidity. In conclusion, this paper focuses on the salinity of the solution to be measured on the measurement of zinc ion concentration, and gives the influence rule and calibration model through experiments.
近年来, 重金属污染已经成为突出的环境问题[1], 尤其是其中含量较多、 污染较重的重金属锌(Zn2+)更是亟待解决的问题。 随着科学技术的发展, 海水中锌离子的检测传感技术有了质的飞跃, 现在常用的主要包括分光光度法[2], 原子发射光谱法[3], 阳极溶出伏安法[4]和原子吸收光谱法[5]等分析法[6], 但是每种方法都很少考虑环境变化与测量条件变化对测量结果的影响。 本工作在基于分光光度法的基础上, 研究锌离子光谱特性和特征峰吸光度的变化规律, 重点研究在其他条件不变的情况下, 待测溶液的盐度的改变对锌离子浓度值测量的影响规律[7], 并给出相应的校正模型, 以提高测量精度, 为痕量锌离子的检测传感技术奠定基础。
采用分光光度法实现对水体中的可溶态重金属锌(Zn2+)测量。 由于金属水合离子本身的吸光系数值很小, 为提高测量精度, 需要加入一定量的显色试剂加大溶液的吸光度, 这是常用的方法; 待显色试剂与被测离子完成显色反应, 再测量吸光度分析待测重金属离子的浓度。 依据朗伯-比尔定律[8], 其数学表达式如式(1), 物理意义是: 对于均匀的有色溶液, 经一束平行单色光照射后, 该溶液的吸光度与有色物质的浓度和溶液光程的乘积成正比。
式(1)中: A为该溶液的吸光度; I0为平行单色光的入射强度; It为平行单色光的透射强度; K为摩尔吸光系数(L· mol-1· cm-1); b为溶液液层厚度(cm); c为溶液浓度(mol· L-1)。
搭建的实验平台如图1所示, 一是用于确定锌离子浓度的特征谱, 二是分析特征谱与吸光度的关系。 图中卤素光源是Avantes, 它的波长范围为200~1 100 nm。
实验测得了Zn2+在不同波长的吸光度, 显色后的Zn2+吸光光谱如图2所示。
从图2可得锌离子峰值波长出现在626.21 nm处。 因此, 取Zn2+金属离子溶液最大吸收波长626.00 nm对应的中心波长620 nm特征波长进行吸光度测量。
在实际应用中, 被测水样的环境参数以及测量条件变化可能对离子吸光度产生不容忽略的影响。 为此, 重点研究Zn2+溶液的吸光度在不同盐度下的变化规律, 以探索环境参数与测量条件对分光光度法锌离子检测的影响规律。
用图1所示实验平台; 经测试, 显色后的Zn2+吸收光谱的吸收峰出现在550~650 nm区间。 选用中心波长为620 nm滤光片进行吸光度测量; Zn2+重金属离子的标准溶液来自于国家标准物质中心, 浓度为1 000 μ g· mL-1。 选用硼酸-氯化钾-氢氧化钠溶液作为缓冲剂, 邻2-(2-羟基-5-磺基苯偶氮)亚苄基肼基苯甲酸作为显色剂。
对溶液中锌离子浓度值的检测, 在实验室内可以提供纯锌离子溶液, 在实际待测溶液中不可能仅含锌离子。 如在海水中, 含有丰富的重金属离子。 在建立传感模型时, 需要先行探索液体中其他离子与显色剂的反应情况及其吸光度。 因此, 选用海水中常见的重金属离子溶液与邻2-(2-羟基-5-磺基苯偶氮)亚苄基肼基苯甲酸显色液反应, 观察测量反应情况。
经实际测量, 邻2-(2-羟基-5-磺基苯偶氮)亚苄基肼基苯甲酸显色液与Zn2+, Cu2+, Ni2+, Cd2+, Pb2+, Fe2+, Mn2+, Hg2+和Al3+等单独作用时, 前四种离子Zn2+, Cu2+, Ni2+和Cd2+都有明显的显色反应, 而后几种离子Pb2+, Fe2+, Mn2+和Hg2+等吸光极其微弱, 当单种离子浓度小于1 mg· L-1时它的影响可忽略。 所以, 在选用邻2-(2-羟基-5-磺基苯偶氮)亚苄基肼基苯甲酸做显色液, 硼酸-氯化钾-氢氧化钠溶液做缓冲剂测量溶液中锌离子含量时, 只需要考虑溶液中Cu2+, Ni2+和Cd2+的干扰, 即可从总吸光度中得到锌离子的吸光度。
显色后的Zn2+, Cu2+, Ni2+和Cd2+吸光光谱曲线如图3所示。
 | 图3 Zn2+, Cu2+, Ni2+, Cd2+溶液吸收光谱Fig.3 Absorption spectrum of coloring solution of Zn2+, Cu2+, Ni2+, Cd2+ |
由图3可知, 在620 nm锌离子特征波长处, Cu2+, Ni2+和Cd2+也有吸光度, 传感器最终得到的是四种离子的总吸光度, 因此需要探索锌离子吸光度和总吸光度的关系。
由于待测溶液的浓度值不同, 所得的结果也会不同, 因此将实验分为低浓度和高浓度两组进行。
低浓度实验时, 首先, 配置溶液。 浓度从0 μ g· L-1开始, 依次增加10 μ g· L-1, 直到浓度为100 μ g· L-1的四种离子溶液; 然后向25 mL容量瓶中分别加入5 mL缓冲液, 2 mL显色液; 再按浓度从低到高分别加入刚配好的10 mL浓度的四种离子溶液, 依次取最大吸收波长626.00 nm对应的中心波长为620 nm的滤光片进行吸光度测量, 光程为1 cm。 四种重金属离子显色后的溶液在不同浓度时的吸光度, 如图4所示。
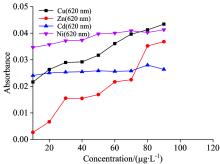 | 图4 低浓度Zn2+, Cu2+, Ni2+, Cd2+吸光度Fig.4 Absorption spectrum of coloring solution of Zn2+, Cu2+, Ni2+, Cd2+ (Low Conc) |
高浓度的实验中, 配置的溶液浓度从0 μ g· L-1开始, 依次增加100 μ g· L-1, 直到浓度为1 000 μ g· L-1的四种离子溶液; 然后向25mL容量瓶中分别加入5 mL缓冲液, 2 mL显色液; 其他均与低浓度实验相同。 四种重金属离子显色后的溶液的吸光度如图5所示。
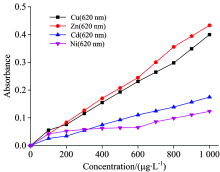 | 图5 高浓度Zn2+, Cu2+, Ni2+, Cd2+ 吸光度Fig.5 Absorption spectrum of coloring solution of Zn2+, Cu2+, Ni2+, Cd2+ (High Conc) |
由上述两组实验可知四种离子在不同浓度下显色后的吸光度, 可以看出在低浓度实验中, 无法有效检测出镉、 镍离子的吸光度随浓度的变化, 但是锌离子检测是十分理想的, 因此锌离子检测下限为10 μ g· L-1, 分辨率< 10 μ g· L-1, 准确度为92.619%。 所以本方法主要探索高浓度检测时锌离子吸光度与总吸光度的关系。 实验得到Zn2+浓度-吸光度各点对应值及拟合曲线如图6所示。
由图6可知, Zn2+浓度与吸光度间是线性关系。 其线性拟合方程为
式(2)中, x1为溶液中Zn2+的浓度, 单位为μ g· L-1; y1代表Zn2+显色后的溶液在620 nm中心波长的吸光度。 由图3可知, 四种离子在四个特征波长处均存在较好的吸光度, 因此通过检测溶液分别在四个特征波长下的吸光度, 即可反向推演锌离子的吸光度。 本课题组在前期的工作中已经完成了通过检测四波长下混合溶液的总吸光度而得到锌离子浓度的推演, 参见文献[9], 所以结合式(2), 即可得到锌离子在620 nm波长处吸光度与溶液总吸光度的关系, 其方程为
式(3)中, y2为锌离子的吸光度, x2, x3, x4, x5分别代表混合溶液在 575, 605, 620和650 nm处的吸光度。
取Zn2+重金属离子溶液10 mL, 与显色剂、 缓冲剂, 按10∶ 2∶ 5的比例混匀后静置待测。 将配制好的待测溶液放入比色皿中, 依次改变Zn2+溶液的盐度; 按图1所示平台, 让检测光照射比色皿溶液, 将通过溶液的透射光送入光谱仪, 再利用计算机软件分析透射光谱的变化, 也就可以分析出不同条件对吸光度的影响。
本实验主要基于分光光度法原理, 溶液中的锌离子与标准锌显色剂邻2-(2-羟基-5-磺基苯偶氮)亚苄基肼基苯甲酸发生显色反应, 即络合反应, 生成络合物。 络合物一般指配位化合物, 由中心原子(或离子)和围绕它的称为配位体的分子或离子(或完全或部分配位键)结合形成, 是分子或者离子与金属离子结合的一类很稳定的、 具有一定化学结构的化合物。
与弱电解质的电离平衡很相似, 配位本体在溶液中的离解平衡也有平衡常数。 显色反应主要是锌离子与锌显色剂发生络合反应形成络离子, 进而形成絮状络合物。 但是配合物也存在稳定性, 这种稳定性主要体现在两方面: 一是热稳定性, 二是在溶液中配合物的组分(中心原子和配位体)是否容易被电离出。 在溶液中, 极少量的中心原子(离子)和配位体可以从配位本体微弱地离解出, 由此可知虽然络离子一般比较稳定, 但在水溶液中却也存在着电离平衡, 也就是说当溶液的盐度发生变化时, 既有可能发生络离子的形成也有可能发生络离子的分解, 从而影响络合反应的程度, 最终影响锌离子的测量值。
3.2.1 不同盐度基底溶液对吸光度的影响
经对河北省海洋与水产科学研究院的渤海近岸部分站位的海水盐度进行测量, 盐度数据如表1所示, 平均值为3.0左右。 为了分析不同盐度对吸光度可能形成的影响, 实验选用Zn2+显色溶液的浓度为500 μ g· L-1, 使用1 cm光程比色池, 进行了不同盐度溶液对吸光度的影响实验。
| 表1 盐度值 Table 1 Salinity data |
Zn2+溶液在不同盐度下的吸光度曲线如图7所示。 (图中不同M数值代表溶液的盐度值)
 | 图7 Zn2+溶液在不同盐度下的吸光度曲线Fig.7 The absorbance curves of Zn2+ color solutions with differenu concentration of 500 μ g· L-1 |
从图7中可以看出, 不同盐度对吸光度有一定影响。 从曲线M-2.81~M-3.28可看出, 当海水盐度为3.0左右, 上下波动小于0.1时, 溶液的吸光度曲线相差很小。 当盐度大于0.3时, 溶液的吸光度变化相对比较大。 一般情况下, 一个区域内海水盐度不会出现大的变化, 所以海水吸光度受盐度影响也较小。
3.2.2 不同盐度基底溶液对吸光度线性度的影响
为测定水质盐度发生变化时, 重金属浓度对吸光度的线性关系是否仍然成立, 开展了实验研究, 实验仍选用Zn2+溶液作为研究对象, 使用1 cm比色池, 依次对浓度为0, 100, 300和500 μ g· L-1的溶液, 进行了不同盐度对吸光度分析实验, 吸光光谱曲线如图8所示。
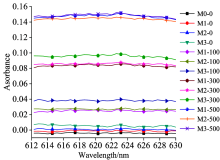 | 图8 不同盐度下的Zn2+吸光光谱Fig.8 Different salinity, the same group of Zn2+ concentration of the color solution of the absorption spectrum |
由图8可以看出, 对四种浓度的Zn2+溶液盐度变化时的斜率分别为0 μ g· L-1: 0.124, 100 μ g· L-1: 0.123, 300 μ g· L-1: 0.123, 500 μ g· L-1: 0.122, 线性关系基本保持一致。
3.2.3 校正模型的建立
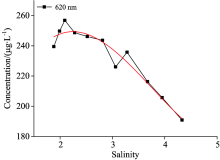
按2.2步骤配制好待测锌离子溶液, 依次改变溶液的盐度, 可以得到待测锌离子溶液在其最佳波长620 nm处的吸光度, 得到吸光度与盐度之间的关系曲线如图9所示。
由图6可知Zn2+浓度与吸光度间是线性关系, 并且得到了Zn2+浓度与吸光度间的拟合方程, 即式(2), 通过式(2), 可以利用已知的溶液中离子的吸光度, 计算得到溶液中离子的浓度, 从而可以得到盐度与测量所得离子浓度关系曲线, 关系曲线如图10所示。
实验采用的均为浓度500 μ g· L-1的Zn2+显色溶液, 因此溶液中离子的真实浓度为500 μ g· L-1, 从而可以得到测量值与真实值的误差值, 这也就是需要人为进行补偿的补偿值。 最后可以得到盐度与人为进行补偿的补偿值之间的关系曲线, 关系曲线如图11所示。
由图11我们可以得到需要进行浓度补偿的值与盐度之间的关系曲线, 通过软件进行多项式拟合, 从而得到拟合方程如下。
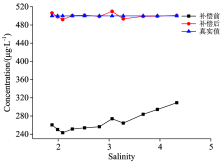
式(4)中, y为需要进行的补偿浓度值, 单位是μ g· L-1, x为溶液盐度值。 利用所得的补偿模型, 来检验补偿效果, 效果如图12所示。
从图12可以看, 在补偿之前, 测量值与真实值相差甚远, 进行补偿之后, 测量值与真实值十分接近, 可以看出补偿效果相当不错, 可以提高测量精度。
建立基于分光光度法痕量重金属(Cu2+, Zn2+, Ni2+, Cd2+)传感模型的基础上, 对锌离子检测及其影响因素进行研究, 探索如何将锌离子的吸光度与其他离子的吸光度分离, 从总体吸光度中得到锌离子吸光度的值, 重点研究盐度对锌离子检测时的影响。 结果主要有:
(1)当水中盐度在3.0上下变化小于0.1时, 吸光度光谱变化较小。
(2)一般情况下, 一个区域内海水盐度不会出现大的变化, 所以海水吸光度受盐度影响也较小。 不同盐度的Zn2+溶液与浓度线性关系基本保持一致。
(3)建立了校正模型, 可以根据测得的待测溶液的盐度值, 对最终所得的溶液中离子的浓度值进行相应补偿。
结果表明, 此补偿模型补偿效果比较显著, 合理应用此模型, 可以提高锌离子检测的检测精度。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|