作者简介: 季雨珊, 1996年生, 中央民族大学生命与环境科学学院理工科创新班学生 e-mail: emmayushanji@163.com
表层沉积物是水体污染物的源和汇。 研究表明, 太湖地区特别是梅梁湾和东太湖表层沉积物中磷等营养元素污染严重。 采用SMT法(standards measurements and testing)和钼锑抗分光光度法对太湖18个采样点表层沉积物样品进行前处理和磷形态分析, 结合我国、 加拿大和美国标准对总磷进行污染评价。 通过拟合建立了吸附-解吸动力学特征方程, 并在不同pH、 水土比的环境条件下获得磷的吸附特性。 同时也在不同温度和pH下对磷进行解吸特征研究。 结果表明: S9采样点总磷、 无机磷、 有机磷和酸磷含量均最高, S11采样点碱磷含量最高。 对于所有采样点, 各形态磷平均值大小排序为(μg·g-1): 无机磷(401.43)>酸磷(377.81)>有机磷(175.37)>碱磷(25.53)。 污染评价结果表明: 除S12, S14~S16及S18采样点外, 其余采样点均有不同程度的污染。 表层沉积物对磷的吸附-解吸过程均符合伪二级动力学方程。 吸附过程最佳水土比为25∶1, 且pH值对吸附和解吸有不同程度的影响。 研究结果为掌握太湖梅梁湾和东太湖区域磷的污染现状提供理论依据, 同时为研究磷在沉积物-水界面的迁移规律提供可信的实验数据。
The surface sediments are the source and sink of many pollutants of water. Studies have shown that phosphorus and other nutrient elements in surface sediments of Taihu Lake area, specially in Meiliang Bay and East Taihu Lake, are seriously polluted.SMT method (Standards Measurements and Testing) and molybdenum antimony anti-spectrophotometry were used to pretreat and analyze phosphorus of the 18 surface sediment samples in Taihu Lake, China, and the total phosphorus pollution was evaluated in comparison with the standards of China, Canada and the United States, respectively. Moreover, the adsorption and desorption kinetics equations were established by linear fitting, the adsorption characteristics of phosphorus under different pH and soil/water ratio were obtained. And we also studied the desorption characteristics of phosphorus under different temperature and pH conditions. The results showed that the highest contents of total phosphorus, inorganic phosphorus, organic phosphorus and acid phosphorus all appeared in S9 sampling sites, the highest content of alkali phosphorus was found in S11 sampling site. For all sampling sites, the order of average contentof each fraction phosphorus was (μg·g-1): inorganic phosphorus (401.43)>acid phosphorus (377.81)>organic phosphorus (175.37)>alkali phosphorus (25.53). The results of pollution evaluation showed that except for S12, S14~S16 and S18, other sampling sites suffered varying degrees of contamination. Both adsorption and desorption processes of phosphorus on the surface sediments followed the pseudo-second-order kinetics equation. The optimum soil/water ratio was 25∶1. The pH had different effects on adsorption and desorption, respectively. The results provided not only a theoretical basis for governing the phosphorus pollution but also credible experimental data for studying the migration of phosphorus at the sediment-water interface in Meiliang Bay and Taihu Lake.
太湖是我国第三大淡水湖, 位于长江三角洲南部苏浙皖三省交界处, 兼具饮用、 养殖、 灌溉、 防洪等诸多功能。 近年来, 太湖主要河道和湖区的水体富营养化日益加剧, 严重影响沿湖地区居民的生活、 生产和环境保护。 2007年太湖爆发蓝藻事件后, 环保部门加强了对太湖污染的治理。 2015年数据显示, 太湖经国家重点治理后, Ⅳ 类水质占64.4%, Ⅴ 类水质占16.8%[1]总氮不参加评价。
磷是影响水体富营养化的主要因子之一。 沉积物中无机磷主要为铁(Fe)、 铝(Al)结合态磷(简称碱磷, NaOH-P)和钙(Ca)结合态磷(简称酸磷, HCl-P)。 当环境条件变化时, NaOH-P能转化为可溶性磷进入水体, 而HCl-P难被分解, 短时间内对水体磷含量影响较小。 磷的来源主要有外源磷输入和内源磷释放。 其中内源磷是指由于动力学和热力学因素的改变引起水和沉积物间动态平衡被破坏而释放的磷。 内源磷比外源磷的危害更大。 在不同条件下, 沉积物对磷的吸附和解吸表现出不同的规律。 近年来国内外学者对沉积物中磷的形态和沉积物-水界面吸附-解吸研究较多, 但对于太湖水体的综合研究还需要进一步深入。
采用SMT分级提取法和钼锑抗分光光度法研究了太湖18个采样点表层沉积物样品中总磷含量及形态分布特征, 并进行污染评价。 同时研究了表层沉积物对磷的吸附-解吸动力学特征。 研究结果为太湖磷的来源、 水环境污染现状和综合治理提供一定的科学依据。
MDS-10高通量微波消解炉(上海新仪微波化学科技有限公司), 高速冷冻离心机(AVanti-j25, 美国贝克曼公司), Spectrumlab 22pc可见光分光光度计(上海棱光技术有限公司), Milli-Q纯水系统(Millipore, USA)。
磷(P)元素标准溶液(1 000 μ g· mL-1, 国家标准物质研究中心)、 抗坏血酸、 钼酸铵、 KH2PO4、 K2S2O8等。 所用试剂均为分析纯, 实验用水为超纯水。
2016年4月29日使用柱状底泥采样器采集了太湖18个采样点表层沉积物样品(见图1), 风干研磨过200目筛, 备用。 按照文献[2]方法进行样品的预处理和总磷及形态磷的测定; 并根据《地表水环境质量标准》(GB3838— 2002)进行污染评价。
2.1.1 表层沉积物中总磷含量及污染评价
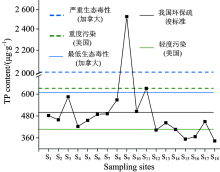
各采样点表层沉积物中总磷含量如图3, 平均值为576.79 μ g· g-1。 其中S9采样点(渔民生态园)总磷含量最高(2 524.82 μ g· g-1), S18采样点(渔业村)含量最低(343.43 μ g· g-1)。 S9采样点位于梅梁湾最北部, 周边是渔民集中生活地。 渔民日常生活使用洗衣粉和洗涤剂等产生的废水和人畜粪便不经处理直接排入太湖。 磷在水中沉积或被吸附后迁移至表层沉积物中, 导致S9采样点表层沉积物中磷含量最高。 采样点总磷含量分布自北向南呈现从高到低的趋势, 大部分梅梁湾湖区富营养化程度高。 这是由于梅梁湾水域主要分布在沿岸人口聚居的地带, 虽相对于贡湖等占水面积较小, 但多为饮用水源, 受到人类活动的影响, 污染程度大; 另外, 梅梁湾入湖河道(如塘柳河、 庄渎河等)为Ⅳ -Ⅴ 类水质, P随河水进入湖中加剧了梅梁湾水域的污染。
与我国国家环保疏浚标准(TP=500 μ g· g-1)比较, 采样点S3, S8, S9和S11需要进行环保疏浚。 对比加拿大评价标准, S9采样点有严重生态毒性效应(TP=2 000 μ g· g-1), S11采样点呈最低生态毒性效应(TP=600 μ g· g-1)。 对比美国评价标准, S1~S8, S10, S11, S13和S17采样点有轻度污染(TP=420 μ g· g-1), S9有重度污染(TP=640 μ g· g-1)。
2.1.2 表层沉积物中磷形态分布
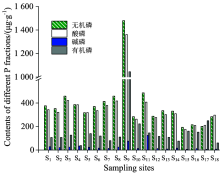
表层沉积物中磷形态分布如图4。 其中无机磷(IP)平均含量为401.43 μ g· g-1, S9采样点无机磷含量最高(1 479.96 μ g· g-1), S15采样点(苏州湾大桥西)无机磷含量最低(192.94 μ g· g-1)。 有机磷(OP)平均含量为175.37 μ g· g-1, 其中S9采样点有机磷含量也最高(1 044.87 μ g· g-1), S4采样点(马山)最低(37.08 μ g· g-1)。 HCl-P平均含量为377.81 μ g· g-1, 其中S9采样点酸磷含量最高(1 361.33 μ g· g-1), S15采样点最低(176.05 μ g· g-1)。 NaOH-P平均含量为25.53 μ g· g-1, 其中S11采样点(水仙台)碱磷含量最高(176.05 μ g· g-1), S17采样点(303乡道)最低(176.05 μ g· g-1)。 各形态磷平均值的大小顺序为: 无机磷> 酸磷> 有机磷> 碱磷。 无机磷约占总磷的69.60%, 酸磷约占无机磷的93.12%。 这是因为, 有机磷只有在有机质矿化时才能被释放进入水体, NaOH-P会与OH-和有机配体发生交换。 通常情况下, 释放的OP和NaOH-P可以转化为生物可利用的磷直接或间接地被藻类利用。 HCl-P主要来源于碎屑岩或原位合成, 不易被释放或被生物体利用[3]。 IP含量受自然和人为因素的影响, 可来自地壳表层风化、 解磷细菌对IP的积累、 磷肥等诸多途径。 因此, OP和NaOH-P含量较低, IP和HCl-P含量较高。
2.2.1 水土比对吸附的影响
图5是在不同水土比条件下得到的沉积物对磷吸附影响的实验结果。 当初始磷浓度c0≤ 0.50 mg· L-1时, 吸附量(Q)顺序为: 水土比25∶ 1> 水土比100∶ 1> 水土比50∶ 1, 当c0≥ 1.00 mg· L-1时, 随着P初始浓度的增大, 水土比为100∶ 1时的吸附量最大, 水土比25∶ 1时最小。 这是因为水土比的减小意味着沉积物的质量浓度增大, 此时溶液的组成会随着沉积物质量浓度的增大而改变, 溶液中会存在更多的小颗粒, 一部分以溶解态、 大分子或胶态形式存在的磷从固相进入液相, 而且这部分的磷不能通过离心过滤去除。 当沉积物质量浓度增大时, 这部分在液相中的磷的含量会增大, 所以磷的吸附量会随着水土比的增大逐渐增大, 产生“ 固体浓度效应” [4]。
2.2.2 磷的吸附动力学
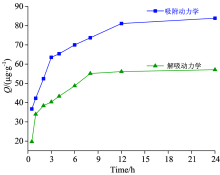
图6是磷的吸附-解吸动力学实验结果。 从图中可以看出吸附主要发生在前8 h, 其吸附量占实验所得最大吸附量的87.87%, 且吸附量随时间的增加而明显增大。 8 h以后, 吸附逐渐趋于平缓, 12~24 h内吸附量基本不变。 各时间段P吸附速率表现为, 0~0.5 h内吸附速率最大, 随着时间的增长, 吸附速率逐渐减小。 Froelich认为吸附过程分为快反应过程(表面吸附反应)和慢反应过程(被吸附的磷酸盐在固体状态下扩散到颗粒内部)[5]。 0~8 h内属于快反应过程, 此时沉积物上吸附点充足, P的浓度大, 吸附速度快。 8 h以后, 随时间的增加, 沉积物表面可吸附P的位点减少, 溶液中可被吸附的P浓度降低, 吸附变慢直至达到平衡。 对吸附动力学进行拟合, 结果表明: 沉积物对磷的吸附动力学更好的符合伪二级方程, 说明磷的内扩散是吸附过程中主要的速率控制步骤。
2.2.3 pH对吸附的影响
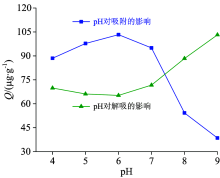
图8给出了pH对吸附的影响结果。 当pH为4~7时, 磷主要以H2P
2.2.4 磷的解吸动力学
由图6可以看出, 沉积物对P解吸过程主要发生在前8 h, 它的解吸量占实验所得的最大解吸量的98.28%, 8 h以后解吸量变化不大。 12 h解吸达到平衡。 这是因为P从沉积物表面的解吸属于快速解吸、 缓慢平衡的动态过程。 解吸过程中, P首先会快速地与结合的金属离子解离而从沉积物表面解吸出来, 然后再从沉积物表面缓慢释放进入水体[9]。 所以前8 h解吸速率快, 解吸量多。 随着解吸的进行, 快反应过程基本完成, 12 h后属于慢反应过程, 解吸逐渐趋于平缓, 解吸量降低。 解吸动力学符合伪二级动力学方程(如图7)。
 | 图7 磷的吸附-解吸伪二级拟合Fig.7 Pseudo-second-order kinetics equation fitting result of phosphorus adsorption-desorption dynamics |
2.2.5 温度对解吸的影响
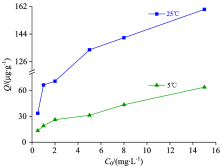
图9是温度对解吸的影响。 由图可以看出, 在一定的初始磷浓度条件下, 沉积物对磷的解吸量表现为: 25 ℃解吸量大于5 ℃。 在温度一定时, 初始磷浓度越大, 解吸量越多, 但当初始磷浓度大于5 mg· L-1后, 解吸量变化缓慢。 随着温度升高, 水体和表层沉积物中的细菌、 藻类等生物的活性增高, 微生物的活跃加速了有机物分解, 分解所需的氧消耗量增加, 氧化还原电位降低, Fe3+被还原成Fe2+, 结合在沉积物表面的Fe/Al-P被释放。 有研究指出温度升高有利于有机物的矿化, 促进OP的转化, P会从磷酸盐和金属氢氧化物中释放出来, 解吸量增加[10]。 当温度低时, 除生命体活动减缓使解吸量减少外, 沉积物粒子运动缓慢, 有效碰撞减少, 环境提供的能量不足以使P从沉积物表面解吸, 解吸程度减小且速度缓慢。
2.2.6 pH对磷解吸的影响
pH对磷解吸影响的实验结果示于图8。 从图中可以看出, 解吸量随pH的增大有先减小后增大的变化趋势。 在酸性和碱性条件下, 表层沉淀物中P的解吸量较大, 中性条件对P的解吸不利。 当4< pH≤ 6时, 磷的解吸量随着pH的升高而减小, 当6< pH≤ 9, 磷的解吸量随着pH的升高而增大, 在pH值为6时磷的解吸量最小。 分析可能的原因是: 沉积物表面会结合Ca2+, Fe3+, Al3+等金属离子, 这些离子及其氧化物、 阴离子(OH-和Cl-等)化合物会通过化学或物理反应与P结合。 P的解吸受到沉积物颗粒表面电荷的影响, 而电荷又与pH值相关。 当pH≤ 6时, H+的浓度大于OH-浓度。 在酸性条件下, 由于金属化合物发生的水解作用, 原被吸附在沉积物中与金属氢氧化物结合的磷的溶解度会增大, 所以低pH对Ca-P从沉积物中解吸的影响更大, 磷的解吸量随着pH的降低而增大, 反之亦然。 中性条件下, 溶液中P的存在形式为HP
(1) S9采样点总磷、 无机磷、 有机磷和酸磷含量均最高, S11采样点碱磷含量最高, 所有采样点均有: 无机磷> 酸磷> 有机磷> 碱磷。 污染评价结果表明除S12, S14, S15, S16及S18采样点外, 其余采样点均有不同程度的污染;
(2) 磷的吸附-解吸动力学均较好的符合伪二级方程, 且不同的环境条件对磷的动力学影响不同。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|