作者简介: 唐青, 1975年生, 贵州大学烟草学院讲师 e-mail: qingt428@163.com
基于七元瓜环可使中性红的荧光增强从而设计荧光探针, 当在荧光探针中加入百草枯后荧光强度又逐渐降低, 利用此种超分子配合物的荧光“开-关”效应, 从而建立了一种新颖的检测百草枯的荧光方法。 当百草枯浓度在(1~8)×10-6 mol·L-1范围内, 百草枯浓度与探针的荧光强度具有良好的线性关系, 且检出限为1.4×10-8 mol·L-1, 加标回收率为104%~108%, 可在河水样品中检测百草枯的含量。
We have now shown that a host-guest complex between cucurbit[7]uril (Q[7]) and neutral red (NR) can be used as a fluorescent probe for detecting the herbicide paraquat. The Q[7]/NR complex can be used to detect paraquat with high selectivity using fluorescence spectrometry. A linear correlation (Δ F=4.98+0.32 c, r=0.999 1) was observed between the fluorescence intensity and the concentration of PQ over the concentration range (1~8)×10-6 mol·L-1. The detection limit for PQ was 1.40×10-8 mol·L-1. Recoveries obtained with the proposed method in river water examples were 104%~108%. Such method provides a rapid, selective and sensitive strategy for herbicide detection in real samples.
引 言
百草枯(Paraquat, PQ) 是一种快速灭生性除草剂, 在自然环境中的残留对生态环境造成严重影响。 百草枯在世界很多国家被限制使用, 如美国环境保护署规定, 在饮用水中最大残留限量为0.3 μ g· L-1 [1, 2]。 目前常用的检测百草枯的分析方法包括: 液质联用(LC-MS)、 高效液相色谱法(HPLC)、 毛细管电泳光学免疫法、 气质联用(GC-MS)等[3, 4, 5, 6, 7] 。 上述检测方法检测仪器昂贵, 分析成本高, 有机溶剂使用过多。 因此发展一种简单、 快速、 灵敏度高的检测百草枯农药残留的方法是十分必要的。
近年来, 通过超分子识别作用构筑荧光探针, 因其具有快速、 灵敏度高及操作简易等特点, 而得到迅速发展。 如以β -环糊精或杯芳烃作为主体分子, 与染料、 镧系金属离子等构建荧光探针, 可直接对葡萄糖、 蛋白质及金属离子等进行检测[8, 9, 10]。
瓜环是一类由苷脲单元通过亚甲基桥联起来的大环主体化合物, 具有特殊的疏水性空腔和亲水性端口结构[11, 12, 13]。 七元瓜环因其具有良好的水溶性, 可与客体分子形成超分子配合物, 超分子配合物的形成能改变客体分子的光化学及光物理学性质[14]。 利用客体竞争作用组装瓜环超分子荧光探针体系可用于检测目标物质, 如当七元瓜环与异喹啉类生物碱(黄连素、 盐酸巴马亭)等荧光物质形成主客体配合物后, 体系的荧光发生增敏, 但当加入青霉胺、 索他洛尔、 雷尼替丁、 金刚烷胺等药物或农药分子后, 体系荧光又发生猝灭。 利用体系的荧光猝灭可建立灵敏、 简便的荧光方法来检测上述药物[15, 16, 17, 18, 19]。 在农药残留检测方面, 七元瓜环/吖啶橙超分子荧光探针可检测环境水样中的百草枯含量, 其检出限低至~10-9 mol· L-1 [20]。 七元瓜环(Q[7])与中性红(NR)可形成主客体配合物, 且七元瓜环对中性红有着荧光增敏作用[21]。 据此构筑了Q[7]-NR超分子荧光探针, 利用百草枯对Q[7]-NR超分子荧光探针荧光猝灭现象, 实现对环境水样中百草枯的快速检测三种除草剂的分子结构如图1所示。
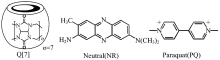 | 图1 七元瓜环、 中性红与百草枯的分子结构式Fig.1 The molicules structure of cucurbit [7] uril(Q[7]), neutral (NR) and paraquat (PQ) |
Varian Inova-400M核磁共振仪(Varian, America), Agilent 8453型紫外-可见分光光度计(Agilent, America), Cary Eclipse荧光光谱仪, Nano ITC等温量热滴定仪(TA, 美国)。 七元瓜环(Q[7])由本实验室按照文献合成分离得到[22, 23], 中性红, 百草枯, 硫酸胺, 甲醇, 甲酸及乙腈均购自Sigma-Aldrich试剂公司, 实验用水为去离子水。
1.2.1 荧光发射光谱
分别配制1.0× 10-3 mol· L-1的Q[7]、 NR和PQ水溶液备用。 固定染料cNR=2.0× 10-5 mol· L-1, 采用摩尔比法改变Q[7]的浓度, 即cQ[7]/cNR=0.0, 0.1, 0.2, 0.3, 0.4, 0.5, 0.6, 0.7, 0.8, 0.9, 1.0, 1.2, 1.5, 加入pH 7的磷酸铵缓冲液, 分别配制一系列不同物质的量之比的pH 7的溶液, 以λ ex=464 nm, 激发及发射狭缝均为5 nm, 电压=600 V, 在室温下测定Q[7]-NR作用体系的荧光发射光谱。 采用固定探针Q[7]-NR(1∶ 1)的浓度为2.0× 10-5 mol· L-1, 改变PQ的浓度: (0, 0.4, 0.8, 1.2, 1.6, 2.0, 2.4, 2.8, 3.2, 4.0)× 10-5 mol· L-1, 加入pH 7的磷酸铵缓冲液, 配制一系列不同物质的量之比的pH 7的溶液, 以λ ex=528 nm, 激发及发射狭缝均为5 nm, 电压=600 V, 测定探针加入百草枯后体系的荧光发射光谱。
1.2.2 1H NMR
氢核磁共振谱以氘代水为溶剂, 配制NR, Q[7], Q[7]/NR(1∶ 1), Q[7]/PQ(1∶ 1)及Q[7]/NR/PQ(1∶ 1∶ 1)溶液, 在25 ℃下测定实验体系的氢核磁共振谱。
1.2.3 ITC等温量热滴定
分别用水配制浓度为1.0× 10-3 mol· L-1的Q[7], NR及PQ母液, 备用。 取Q[7]母液, 浓度稀释至1.0× 10-4 mol· L-1, 在参比池中加入水, 用NR或PQ溶液滴定Q[7]。 使用Nano ITC测定上述体系的热力学参数。 测试条件为: 25 ℃, 10 μ L· d-1, 间隔时间250 s, 搅拌速度为250 r· min-1。
1.2.4 百草枯的测定
固定荧光探针Q[7]/NR(1∶ 1)浓度为2.0× 10-5 mol· L-1, 改变PQ的浓度(1~8)× 10-6 mol· L-1, 测定体系的荧光强度。 以Δ F(Δ F为Q[7]/NR探针荧光强度与Q[7]/NR-PQ荧光强度的差值)为纵坐标, PQ浓度为横坐标, 绘制得到校正典线。 依照IUPAC规定, 计算出检出限, 用加样法对河水中农药的含量进行测定。
在花溪湿地公园采集水样, 离心, 过滤, 水样放入采样瓶中, 在4 ℃冰箱中保存, 待用。 从采样瓶中移取100 mL水样至锥形瓶, 分别加入0.1, 0.2和0.4 mL的0.1 mol· L-1百草枯标准样品, 逐滴加入磷酸铵缓冲液(1.0 mol· L-1, pH 7), 调节pH 7, 得到水样品。 用甲醇(2 mL)和水(2 mL)分别活化和平衡WCX固相萃取小柱, 把上述水样品100 mL缓慢倒入WCX固相萃取小柱上, 先用1 mL水淋洗小柱, 再用1 mL甲醇淋洗小柱, 滤液弃去。 最后用5 mL 2%甲酸乙睛洗脱目标组分, 收集溶液, 水浴锅蒸干, 加入去离子水稀释并定容至5 mL, 得到待测样品。 试验均设置3个平行。
称取26.8 mg七元瓜环与5.8 mg中性红混合, 用去离子水配制成100 mL荧光探针溶液; 取50 μ L水样品与1 mL荧光探针放入10 mL容量瓶中, 用二次蒸馏水定容至刻度, 摇匀, 室温放置10~20 min后, 以λ ex=528 nm, 激发及发射狭缝均为5 nm, 电压=600 V, 对样品的荧光发射光谱强度进行测定。 根据荧光强度在标准曲线上查出样品溶液中百草枯的浓度, 实验平行测定3次, 取平均值。
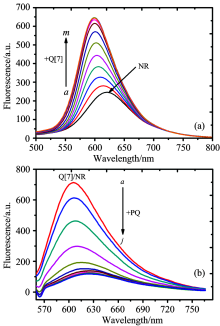
中性红是一种细胞染色染料, 在620 nm处具有特征的荧光发射峰, 当中性红在pH 7的磷酸铵缓冲液(2.00× 10-5 mol· L-1)中加入七元瓜环后, 随着Q[7]浓度的增加, 体系的荧光强度不断增强, 同时伴随着最大荧光发射峰从620 nm逐渐移到604 nm, 蓝移了16 nm。 当Q[7]浓度达到2.00× 10-5 mol· L-1时, 体系的荧光强度不再变化[图2(a)], 其原因是Q[7]与NR形成包结计量比为1∶ 1的主客体配合物, 这与文献[21]报告的结果一致。 但当在Q[7]/NR(1∶ 1)溶液中逐渐滴加PQ, 体系的荧光强度降低, 最大荧光发射峰从604 nm逐渐移到620 nm, 红移了16 nm, 如图2(b)所示。 从上述分析可知, 七元瓜环与中性红形成主客体复合物(Q[7]/NR)而使超分子体系的荧光增强, 当在Q[7]/NR体系中加入百草枯后荧光强度又发生猝灭, 利用此种超分子配合物的荧光“ 开-关” 效应, 构筑一种新颖的超分子荧光探针来检测百草枯的含量。
2.2.1 溶液酸度, 温度及浓度对荧光探针检测PQ的影响
在pH 2~12的范围内考察了酸度对Q[7]/NR荧光探针检测PQ的影响。 结果表明, 在pH 5~8时, 荧光强度最大且基本不变, 因此选择pH 7的磷酸铵缓冲液作为检测介质。 同时考察了温度对荧光探针检测性能的影响, 在15~25 ℃范围内, 荧光强度最大且稳定, 本实验选择25℃作为检测温度。
固定中性红的浓度为20 μ mol· L-1, 逐渐增加Q[7]的浓度, 测定其荧光光谱变化情况。 实验结果发现Q[7]的浓度为20 μ mol· L-1时体系的荧光最强。 固定Q[7]的浓度为20 μ mol· L-1, 改变NR浓度, 当NR浓度达到20 μ mol· L-1时, 增加NR的量, 荧光强度不再变化。 因此Q[7]及NR的最佳使用浓度均为20 μ mol· L-1。
2.2.2 线性范围与检出限
PQ能使Q[7]/NR探针的荧光强度减弱, 当PQ在(1~80)× 10-5 mol· L-1的浓度范围内, 探针Q[7]/NR的荧光强度变化(Δ F)与PQ浓度(c)呈现直线关系, 线性方程为: Δ F=4.98+0.32c(R=0.999 1)。 PQ的检出限为1.4× 10-8 mol· L-1。
2.2.3 干扰实验
为了考察水体中常见金属离子对Q[7]/NR(20 μ mol· L-1)超分子荧光探针检测PQ(20 μ mol· L-1)的干扰情况, 当相对误差为± 5%时, 干扰影响较小。 结果如表1所示。 从表1数据可知, 40倍探针浓度的Ca2+, 50倍探针浓度的Fe3+, 60倍的N
| 表1 离子选择性结果 Table 1 The result of selectivity study |
2.2.4 样品测定
按试验方法分别测定了河水样品中百草枯的含量, 通过加标样处理后测回收率, 同时利用HPLC方法作对比, 结果如表2所示。 从表2样品测试结果可知, 采用荧光探针法检测, 取得较好的结果(RSD< 5%), 且该结果与高效液相色谱法检测结果相符, 表明Q[7]/NR超分子荧光探针能较好地用于PQ的检测。
| 表2 样品分析结果 Table 2 Analytical results of PQ in samplesa |
为了确认Q[7]/NR超分子荧光探针对PQ的作用机制, 采用氢核磁共振波谱(1H NMR)及等温量热滴定法(ITC)探讨了Q[7]/NR超分子荧光探针对百草枯检测机理。 图3显示了Q[7]/NR超分子荧光探针与PQ之间的超分子相互作用情况。 由图可看出, 向Q[7]当中加入等浓度的NR后, NR分子甲基上的Ha质子共振峰向高场移动~0.3 ppm, Hb质子共振峰向低场移动了~0.3 ppm, 而环上的Hc-g质子共振峰均向低场移动[图3(a)和(b)], 表明NR的甲基部分进入Q[7]空腔而形成主客体配合物。 Q[7]中加入同浓度的PQ时, PQ吡啶环上Ha质子共振峰向高场移动~0.06 ppm, Hb质子共振峰向高场移动了~1.6 ppm, 甲基上质子共振峰向低场移动了~0.2 ppm[图3(e)和(d)], 表明PQ吡啶环部分包结于Q[7]空腔内, Q[7]与PQ形成了主客体包合物。 当PQ加入到探针Q[7]/NR中时, NR甲基上的Hb, Ha质子共振峰向低场移动, 化学位移向游离客体靠近, 而PQ的Hb质子共振峰仍处于高场[图3(c)], 表明当PQ加入Q[7]/NR体中后, 原有在Q[7]空腔中的NR分子被PQ挤出, 从而形成了Q[7]/PQ超分子复合物, 其可能作用模式如图3(f)所示。
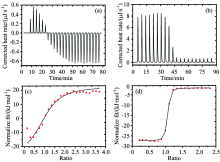 | 图4 25 ℃时Q[7]与NR(a, c)和Q[7]与PQ(b, d)在水溶液中等温量热滴定Fig.4 Isothermal titration calorimetry profiles for the complexation of Q[7]/NR (a, c) and Q[7]/PQ (b, d) in aqueous solution at 25 ℃ |
ITC给出了Q[7]/NR及Q[7]/PQ体系的热力学参数(表3, 图4)。 Q[7]与NR及Q[7]与PQ的作用比均约为1, 表明Q[7]与NR, Q[7]与PQ均形成1: 1的主客体配合物。KQ[7]/PQ> KQ[7]/NR, 表明Q[7]与PQ的作用强于Q[7]与NR的作用, 即PQ可把Q[7]中的NR挤出空腔而形成Q[7]/PQ主客体配合物, 该结果与1H NMR测试结果相符。
| 表3 Q[7]/NR及Q[7]/PQ主客体配合物相关参数 Table 3 Thermodynamic binding data for Q[7]/NR and Q[7]/PQ complexes |
基于超分子识别作用构筑了七元瓜环/中性红荧光探针, 研究了百草枯对七元瓜环/中性红荧光探针的荧光猝灭作用, 荧光探针具有检测线性良好, 检出限低, 快速、 灵敏的优点, 实现了对除草剂百草枯的实际样品检测。 氢核磁共振波谱及等温微量量热法证实了七元瓜环/中性红荧光探针对百草枯荧光响应机理。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|