作者简介: 刘兴斌, 1977年生, 沈阳农业大学土地与环境学院农业资源利用博士后流动站 e-mail: liu_xingbin@163.com
目前国内外对脲甲醛肥料肥效的快速评价方法均采用基于脲甲醛水溶性的活度系数法, 但不同国家和地区具体的操作规程和技术指标不尽相同, 究其原因在于活度系数法的局限性。 脲甲醛肥料的养分释放速率与脲甲醛结构有直接的关系, 与其在不同温度水溶液中的溶解性没有直接关联, 因此从脲甲醛结构入手研究其养分释放更为合理。 通过考察傅里叶变换红外光谱评估不同水分、 尿素量和甲醛存放时间三个因素下尿素与甲醛产物结构的可行性, 以寻求一种新的脲甲醛肥效评价方法。 研究了不同反应条件下产物红外吸收光谱图、 产物生成量和酸性环境下不同尿素加入量反应产物养分释放间的关系。 谱图能够反映出反应过程中不同的水分和尿素加入量及甲醛存放时间对特征基团吸收峰相对强弱产生的细微变化, 通过这些变化可以判断脲甲醛组成变化。 这些判断能够从产物的量得到印证, 同时土培试验的结果也进一步证实通过红外谱图判断的正确性。 以上研究结果表明用红外吸收光谱研究脲甲醛结构的细微变化是可行的, 如果将脲甲醛红外光谱的细微变化与其在土壤中养分释放情况间建立起相应的数学模型, 将为脲甲醛肥料肥效准确、 快速评估提供一个新的手段。
At present, the rapid evaluation methods of urea formaldehyde fertilizer (UFF) efficiency are based on the activity coefficient method of urea formaldehyde (UF) water solubility, but the specific operating rules and technical indexes are different in different countries and regions because of activity coefficient method limitation. The nutrient release rate of UFF is directly related to the structure of UF, which is not directly related to its solubility in aqueous solution at different temperatures. Therefore, it is more reasonable to study the nutrient release from UF structure. In this study, we investigated the feasibility of fourier transform infrared spectroscopy (FTIR) to evaluate the structure of UF under different factors of water content, urea content and formaldehyde storage time, so as to find a new UFF evaluation method. We investigated the relationship between the infrared absorption spectra of the product under different reaction conditions, the amount of product produced and the nutrient release of the reaction product of different urea in the acidic environment. It can be seen from the research results that the spectrum can reflect the change of water and urea addition and the change of formaldehyde storage time on the relative strength of the absorption peak of the characteristic group of UF. Through these changes, the change of UF composition can be judged. These judgments can be confirmed from the amount of the product, and the results of the soil culture experiments were further confirmed by the infrared spectrum to determine the correctness. The above results showed that it was feasible to study the fine change of UF structure by infrared absorption spectroscopy. If the mathematical model was established between the fine changes of urea formaldehyde infrared spectrum and UF nutrient release in the soil, a new means to assessment UFF fertilizer efficiency would be provided accurately and rapidly.
施肥过量造成的面源污染、 农产品品质下降的问题日益受到国家的重视[1], 化学肥料零增长也已经成为国家战略, 新型肥料日益受到重视。 脲醛肥料作为新型肥料的一员, 因能够提高肥料利用率, 且生产工艺简单、 环境友好受到格外关注[1, 2]。
目前国内外关于脲醛类新型肥料研究多局限于脲醛肥料施用对环境的影响[3, 4, 5]和施用效果[6, 7, 8, 9]。 就脲醛肥料肥效评价而言, 田间试验能够直观评判, 但耗时较长, 不适于肥料生产线的品质控制。 目前生产上通常以脲醛水溶性为依据的活度指标评价脲甲醛肥料的缓释性能[1]。 脲醛肥料氮素的释放主要受微生物分解的影响[1, 10], 与土壤水分及温度没有直接关系, 因此常常出现以活度指标评价的脲醛肥料肥效没有差异, 但在不同年份、 不同土壤和地域应用时却出现截然不同的田间表现的情况, 影响肥料的应用推广。
脲醛肥料氮素释放主要受土壤微生物对脲醛肥料分解的影响, 而影响微生物分解脲醛的主要因素是脲醛结构和基团组成[1, 11, 12]。 因此从研究脲醛结构差异的角度入手寻找脲醛肥效的评价方法, 更贴近生产实践。
红外光谱作为表征物质结构的手段, 具有方便高效的优点[13]。 如果能利用红外光谱实现脲甲醛肥料肥效的准确评估, 则能为脲甲醛肥料生产企业品质管控提供便捷高效的方法。 段路路等[14]曾研究过利用红外光谱评价脲甲醛的肥效, 但没有成功。 他们的工作极具创新性, 之所以失败, 可能是因为采集的红外图谱数量较少及采用的土培方法有待完善。
由于脲甲醛制造过程中涉及的参数比较多, 本方案针对工业化生产中脲甲醛红外谱图不足现状, 加大脲甲醛红外谱图的测定工作, 选择工业化生产过程中基层操作人员广为涉及的尿素加入量、 水分加入量和甲醛存放时间三个参数开展研究。 试图采集尿素与甲醛在不同反应条件下产物的红外光谱图, 通过红外光谱图解析反应产物的结构及组成变化, 并利用不同条件下反应产物的生成量和土培试验中反应物速效氮的释放量, 验证红外谱图解析的合理性; 通过三种方式的相互验证, 考察红外光谱在评估脲甲醛养分释放方面的可行性。 为寻找肥料生产过程中控制的关键因素, 实现脲甲醛肥料肥效的快速评估, 促进脲醛肥料肥效稳定探索行之有效的检测方法。
1.1.1 试验材料
尿素: 辽宁华锦化工(集团)有限责任公司生产。
甲醛: 分析纯, 8%~14%, 国药集团化学试剂有限公司。
硫酸: 分析纯, 西陇化工股份有限公司
氢氧化钠: 分析纯, 国药集团化学试剂有限公司。
1.1.2 仪器
pH计: PHS-3G, 上海仪电科学仪器股份有限公司。
恒温水浴锅槽: ZSBB-726, 上海智城分析仪器制造有限公司。
红外吸收光谱仪: 美国Thermo Nicolet公司生产的Nexus 470傅里叶变换红外光谱仪。
1.1.3 样品制备步骤
称取20 g尿素三等份, 分别溶于盛有30, 35和40 mL蒸馏水的烧杯中, 把烧杯置于50 ℃的恒温水浴锅中, 在尿素水溶液达到设定温度后, 向烧杯中加入14%的甲醛溶液35 mL。 分别用稀硫酸或稀氢氧化钠水溶液调节反应体系酸碱度, 达到pH 5。 待体系温度再次达到设定温度后, 记录反应时间和反应现象。 反应结束后将反应产物过滤, 并将反应产物放在阴凉干燥处风干称重, 粉碎待用。
1.1.4 脲甲醛红外光谱的测定
取少量1.1.3中制得的脲甲醛粉末与KBr粉末一起研磨压片, 用Thermo Nicolet公司生产的Nexus 470红外光谱仪进行测定。
1.2.1 供试土壤
供试土壤为典型棕壤, 采自沈阳农业大学后山试验田0~20 cm耕层, 将采集的新鲜土样剔除杂物及残留根系, 风干, 过10目筛备用。 试验前土壤基础肥力性状为: 有机质16.43 g· kg-1, 全氮1.09 g· kg-1, 铵态氮4.07 mg· kg-1, 硝态氮13.3 mg· kg-1, 速效磷11.65 mg· kg-1, 速效钾96.86 mg· kg-1, pH 6.42。
1.2.2 试验处理
试验选取酸性条件下不同质量尿素与甲醛反应物为考察对象。 设5个处理: (1)CK, 不加脲甲醛; (2)尿素添加量为10 g的脲甲醛; (3)尿素添加量为20 g的脲甲醛; (4)尿素添加量为30 g的脲甲醛; (5)尿素添加量为40 g的脲甲醛。
1.2.3 试验实施
脲甲醛用量按1.00 gN· kg-1干土施用, 每个处理18次重复。 将相当于300 g烘干土的鲜土与设定脲甲醛充分混匀后装入带有密封盖的塑料盒中, 用密封盖封口, 并用打孔器在密封盖上均匀打上小孔, 以使土壤在培养过程中保持充分好气的条件, 然后将塑料盒置于25 ℃培养箱中恒温培养。 培养期间, 每天放气1 h后, 采用称重法补水一次, 使土壤含水量始终保持在田间持水量的60%。 在土壤培养试验开始后第10, 20, 30, 60, 90和120天取样, 每个处理每次取三个培养, 测定土壤中速效氮(铵态氮和硝态氮)含量。 培养至4个月时试验结束。
1.2.4 测定项目与方法
本试验测定土壤中硝态氮和铵态氮, 测定方法: 每次取样后, 立即用2.0 mol· L-1 KCl溶液浸提土样, 连续流动分析仪(AutoAnalyzer 3, BRAN+LUEBBE)测定土壤中的N
试验所得数据采用excel处理和spss13软件进行统计分析。
2.1.1 不同水分添加量对脲甲醛红外吸收的影响
反应体系中水分加入的多少直接影响反应体系中各物质的浓度, 物质浓度的不同通常会对反应产生一定的影响, 进而影响工艺路线的设计。 因此, 研究反应体系中水分添加量具有重要意义。
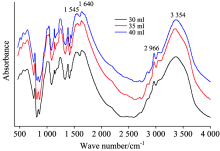
通过红外光谱发现, 不同水分加入量对反应产物中各吸收峰位置没影响, 但对各特征基团相对吸收强度有一定的影响。 不同水分添加量反应产物中1 545 cm-1处仲酰胺(CO— NH)中C— NH弯曲振动吸收峰和1 640 cm-1附近— C=O伸缩振动吸收峰的相对吸收强度几乎没有变化。 当水量较少时(添加30 mL水)3 354 cm-1处酰胺的N— H伸缩振动吸收峰和2 966 cm-1处受N原子影响的C— H伸缩振动吸收峰相对强度有所增强; 尤其是C— H伸缩振动吸收峰的强度显著增加, 表明水分较少时参与到反应中的甲醛量有所增加, 这反映出水分减少有利于甲醛参与反应, 而甲醛的参与是提高脲甲醛分子量的关键。
从以上现象可以看出水分的增加有助于降低脲甲醛的分子量; 相反, 降低反应体系中的水分含量, 则有助于提高反应产物的分子量。 因此可以根据需求适当调整反应体系中水分的加入量。
2.1.2 酸性条件下不同尿素加入量对脲甲醛红外吸收的影响
反应体系中某一反应物浓度的不同在一定程度上会影响反应产物的组成, 不同尿素添加量改变了尿素/甲醛的比例, 对反应产物组成的影响究竟有多大, 弄清楚这个问题对脲甲醛肥料的生产有着重要意义。 样品制备与1.1.3所述基本相同, 但这里是称取10, 20, 30和40 g的尿素分别溶于35 mL蒸馏水中, 与35 mL的甲醛在pH 5下反应。
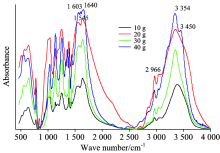
从不同数量尿素与甲醛反应产物的红外吸收谱图(图2)可以看出, 指纹区各吸收峰数量和位置几乎没有变化。 随着尿素量的增加, 1 545 cm-1处仲酰胺(CO— NH)中C— NH弯曲振动吸收峰和1 640 cm-1附近— C=O伸缩振动形成的吸收峰的相对吸收强度差距逐渐缩小, 说明参与到反应中的尿素数量逐渐增多, 随尿素量增加导致反应产物仲酰胺和羰基含量的差异逐渐缩小。 在尿素添加量为30和40 g时在1 603 cm-1处出现了伯酰胺的面内弯曲振动, 且随尿素量增加, 该处的吸收强度有所增加, 说明尿素加入量过多导致未参与反应的— NH2有所增加。
3 354 cm-1处酰胺中N— H伸缩振动相对强度随尿素加入量的增加呈先降低后升高的走势, 在添加量为10与40 g时相对吸收强度基本一致, 这说明在尿素少量加入时, 反应产物空间结构简单, N— H键的伸缩振动受空间位阻的影响较小, 所以该处的红外吸收强度相对较高。 随着尿素的加入, 反应产物结构相对复杂, 空间位阻抑制了N— H的伸缩振动, 但随着尿素添加量的进一步增加, 反应产物中N— H增多和分子量的下降, 共同促成N— H伸缩振动红外吸收强度的回升。 另一个重要特征是当尿素添加量达40 g时, 3 450 cm-1处出现— OH的特征吸收峰, 说明随着尿素添加量的增加, 反应产物中— NH2含量增加, 导致产物中产生吸附水所致。
与其他吸收峰相比, 随着尿素加入量的增加, 2 966 cm-1处CH伸缩振动吸收峰的相对强度有逐渐降低的趋势, 这说明随尿素添加量增加, 反应产物中以氨基封端的情况逐步增多。
由以上各特征峰变化可以看出, 在一定范围内尿素添加量的增加可以增加反应产物结构的复杂程度, 但随着尿素加入量的增加, 产物的分子量存在降低的趋势, 这同增加尿素/甲醛的值有利于增加脲甲醛水溶性[2]的结果一致。 这也反映利用红外吸收光谱研究脲甲醛组成变化的可行性。
2.1.3 碱性条件下不同尿素加入量对脲甲醛红外吸收的影响
由图3可知, 如样品制备的其他条件不变, 但是碱性环境中进行, 所得产物的红外吸收的变化趋势与酸性条件下(图2)几乎一致。 1 545 cm-1处仲酰胺(CO— NH)中C— NH弯曲振动吸收峰和1 640 cm-1附近— C=O伸缩振动形成的吸收峰的相对吸收强度差距逐渐缩小, 当尿素添加30和40 g时在1 603 cm-1处出现了伯酰胺的面内弯曲振动, 且随着尿素加入量的增加, 该峰的吸收强度有所增加。
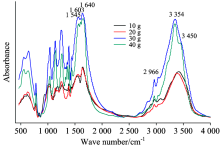 | 图3 碱性条件下不同数量尿素(10, 20, 30和40 g)与 甲醛反应产物红外吸收光谱Fig.3 FTIR spectra of the products of formaldehyde reacting with different urea quantities (10, 20, 30, 40 g) in the alkaline environment (pH 9) |
3 354 cm-1处酰胺中N— H伸缩振动相对强度随尿素加入量的增加有微弱的下降趋势。 与在酸性反应体系相同, 在尿素添加量为40 g时, 在3 450 cm-1处也出现了— OH的特征吸收峰。
结合酸性反应体系的红外图谱可以看出: 对于尿素和甲醛的反应而言, 反应体系的酸碱环境虽然能够影响尿素与甲醛产物的结构, 但影响有限。 酸碱环境对产物红外吸收的影响远没有改变反应体系中尿素添加量的影响大。 因此, 调整反应体系中尿素加入量实现脲甲醛产品组成的调节是较为有效的措施。
2.1.4 不同甲醛存放时间对脲甲醛红外吸收的影响
了解原料存放时间是否会对反应产物产生影响, 对企业原材料采购和生产成本控制有极大的帮助。 为评价不同存放年限甲醛对反应产物的影响, 样品在pH 6条件下制备, 如1.1.3所述, 20 g尿素分别和35 mL存放5年的甲醛和新生产的甲醛在30 mL水中反应15 min。
图4是产物的红外吸收光谱, 通过红外谱图的比对: 新甲醛与存放5年甲醛反应产物谱图中峰的个数和出峰位置没有变化, 相对其他各吸收峰而言, 新甲醛产物中3 354 cm-1处酰胺的N— H伸缩振动相对强度, 1 545 cm-1处仲酰胺(CO— NH)中C— NH弯曲振动吸收峰和1 640 cm-1附近O— C伸缩振动形成的吸收峰相对旧甲醛有较强的增加, 表明采用新甲醛的处理中参于反应的尿素比例有所上升。 1 640 cm-1处O— C伸缩振动吸收峰的增加幅度高于1 545 cm-1仲酰胺中C— NH弯曲振动吸收峰, 证明新甲醛有助于更多的甲醛参与到反应中去, 提高产物的聚合度, 这一点从新甲醛反应产物的质量(28.7 g)大于旧甲醛反应产物的质量(26.9 g)也可以得到印证。
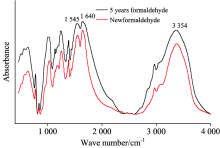 | 图4 不同存放时间的甲醛与尿素反应物的红外吸收光谱Fig.4 FTIR spectra of the products of urea and formaldehyde with different storage times in acidic environment (pH 6) |
由此可以看出, 如果要生产高聚合度的脲甲醛产品, 可以选择新生产的甲醛溶液, 如果要生产低聚合度的脲甲醛产品, 可以选择前期库存的甲醛, 这样不仅有利于反应条件的控制, 也可以物尽其用。
2.2.1 不同反应环境下尿素加入量的变化对脲甲醛产量的影响
由图5可以看出: 无论酸性或碱性反应环境, 在尿素添加量10~30 g时, 尿素添加量与反应产物生成量间几乎成线性关系, 但在尿素加入量达到40 g时, 反应产物增加趋势均有所减缓。 这可能是因为尿素加入量为40 g时, 反应产物中溶于水的成分所占比例有所增加, 从而导致反应物增量趋缓。
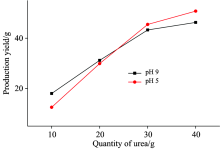 | 图5 不同pH下不同尿素添加量脲甲醛产量Fig.5 The yield of urea-formaldehyde produced by formaldehyde with different quantities of urea and different pH values |
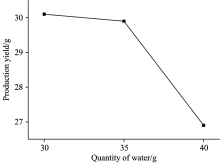 | 图6 不同水分加入量脲甲醛的生成量Fig.6 The yield of urea-formaldehyde produced by urea and formaldehyde with different quantities of water |
从图5中可以看到, 在尿素加入量较少(10~20 g)时维持碱性反应环境有利于提高产物的产率, 而酸性环境则有助于提高较高尿素加入量(30~40 g)时产物的产率。 这告诉我们针对不同的尿醛比分步调控反应体系的pH将有助于提高脲甲醛的产率。
单就酸性或碱性体系下尿素加入量与反应物产量变化的结果而言, 与红外图谱各峰强度相对变化的解析基本吻合, 这反映出利用红外光谱推测尿素与甲醛反应产物的性质具有可行性。
2.2.2 不同水分加入量对脲甲醛生成量的影响
虽然本试验反应体系中水分加入量的变化幅度(10 mL)相对于反应溶液的总体积而言较小, 但当水分加入量由35 mL增加到40 mL时脲甲醛产物的生成量较水分由30 mL增加到35 mL时有明显的下降, 这说明反应体系中水分含量的变化对尿素与甲醛反应影响较大。
随水分加入量的增加, 脲甲醛产物的生成量快速减少, 可能是水分的增加使甲醛参与反应的比例减少所致。 这一点可以从二者红外吸收谱图的变化上得到佐证。
由表1可以看出: 施脲甲醛的四个处理土壤中铵态氮的变化趋势相似, 铵态氮的含量均呈现由高到低的变化过程, 且随培养时间的延长, 土壤中的铵态氮下降趋势逐渐变缓。 这表明在培养初期, 脲甲醛中铵态氮的释放速度较快, 随着培养时间的延长, 脲甲醛的分解速度逐渐趋于稳定。 同样这4个处理土壤中硝态氮变化趋势也较为一致, 硝态氮的含量在培养前期急剧上升, 在培养后期硝态氮含量的上升趋势有所缓和。 且土壤中速效氮的总量也呈现前期增长迅速后期增速趋缓的规律。 这反映出在培养前期, 脲甲醛中易于降解的组分快速分解转化, 随着培养时间的延长, 易分解组分逐渐减少, 土壤中速效氮的变化趋于缓和。
| 表1 酸性条件下不同尿素加入量脲甲醛土培试验土壤速效氮含量 Table 1 Soil availabme N content of soil culture experiment with urea formaldehyde produced by formaldehyde with different quantities of urea in acidic environment |
不同施肥处理间养分释放速率差异较为明显。 在相同的采样时间, 尿素加入量较大的脲甲醛处理土壤中硝态氮和铵态氮的含量均较高。 土壤中速效氮的含量状况说明尿素加入量的增加有助于提高脲甲醛中氮元素的释放、 提高脲甲醛的速效性, 尿素添加量的减少则可以使脲甲醛的养分释放期延长。 这一点在不同尿素加入量的红外吸收光谱图上也有所体现。
因此, 我们可以通过选择不同的特征基团红外吸收峰的相对强弱判断脲甲醛基团组成的变化, 从而判断出不同脲甲醛之间养分释放速率、 肥效长短的不同。
从不同反应条件尿素与甲醛反应产物红外谱图可知: 不同反应条件下尿素与甲醛反应产物结构的变化在其红外吸收光谱图上均有所体现。 如减少反应体系中水分的含量, 有助于提高甲醛参与反应从而提高脲甲醛的分子量, 相反增加体系中水的量则降低了甲醛在反应中的参与度。 这一点在产物生成量中也得到了印证。
在尿素的添加量方面, 无论是酸性或碱性反应体系, 一定范围内尿素数量的增加都可以增加反应产物结构的复杂程度, 但随着尿素加入量的增加, 产物的分子量存在降低的趋势, 这与随着尿素加入量的增加反应产物重量的增幅有所减缓的趋势相吻合。
不同甲醛的存放时间对脲甲醛中基团相对组成的影响在红外吸收峰上也有所体现, 且各特征吸收峰相对强弱的解析结果也与反应产物的质量数据极为吻合。
从酸性条件下甲醛不同量尿素生成的脲甲醛土培试验结果可以看出: 在120 d的培养期内, 尿素加入量的增加能够显著增加脲甲醛氮素的释放, 这与尿素增加引起脲甲醛结构的变化有关, 这一判断可以从红外光谱中特征吸收峰的相对强弱变化得到支撑。
通过对不同反应条件下尿素与甲醛反应产物的红外光谱解析, 并利用产物生成数量及土培数据进行验证, 说明通过比较脲甲醛红外光谱中各特征吸收峰相对强弱的变化, 可以对脲甲醛产品的养分释放情况做出较为准确的推测。 而脲甲醛在土壤中的养分释放也极为接近脲甲醛的实际应用情况; 如果我们能在脲甲醛红外光谱的细微变化与其在土壤中养分释放情况间建立起相应的模型, 将会为脲甲醛肥料肥效快速、 准确评估提供一个新的手段。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|