作者简介: 何磊, 1992年生, 华东理工大学煤气化及能源化工教育部重点实验室硕士研究生 e-mail: notte_hl@163.com
OH*自由基是火焰中主要的激发态自由基之一, 它所产生的化学发光可用于描述火焰的结构、 拉伸率、 氧燃当量比和热释放速率等特征信息, 因此被广泛应用于火焰燃烧状态的在线诊断。 以甲烷/氧气层流同轴射流扩散火焰作为研究对象, 采用GRI-Mech 3.0机理结合OH*自由基生成和淬灭反应进行数值计算, 对OH*自由基的二维分布特性进行研究, 分析不同区域内OH*自由基的生成路径, 并探讨不同氧燃当量比例和不同喷嘴出口尺寸对OH*自由基强度和分布特性的影响。 模拟结果与实验研究基本吻合, 表明计算模型能够准确描述火焰中OH*自由基的二维分布。 结果表明: 在甲烷/氧气层流同轴射流扩散火焰中, OH*自由基存在两种不同形态的分布区域, 分别由反应CH+O2=OH*+CO和H+O+M=OH*+M生成; 随着氧燃当量比提高, OH*自由基的分布区域逐渐向火焰下游扩张, 根据其分布形态的变化可以对火焰燃烧状况进行判断; 如果OH*自由基仅分布于火焰的上游区域且呈断开形态, 则说明火焰处于贫氧燃烧状态。 如果OH*分布呈环状形态, 则说明火焰处于富氧燃烧状态; 相同氧气流量条件下, 缩小喷嘴出口的环隙尺寸有助于加强燃料和氧气的化学反应程度, 从而使火焰中OH*自由基的摩尔分数显著提高, 增强OH*化学发光的辐射强度, 提高火焰光谱诊断的准确性。
OH* is one of the major excited radicals in flame. The chemiluminescence information is generally applied in combustion diagnostics to indicate the flame structure, strain rate, equivalence ratio, heat release rate, etc. In this paper, the numerical study on OH* radicals was conducted in the laminar methane/oxygen co-flowing jet diffusion flames. The detailed GRI 3.0 mechanism combined with OH* radicals reaction mechanism was used in the numerical model. Based on the two-dimensional OH* distributions, the pathways of OH* formation in different area were analyzed. The effects of oxygen-fuel equivalence ratio and coaxial nozzle structure on OH* intensity and distribution were also discussed. The simulation results were consistent with the experiment results, indicating that the numerical model can effectively describe the two-dimensional OH* distributions. The results show that there are two different types of OH* distribution areas, and the OH* radicals in these two areas are formed respectively through the reactions CH+O2=OH*+CO and H+O+M=OH*+M. The flame structure can be indicated according to the distribution area of OH* radicals. With increasing the oxygen-fuel equivalence ratio, the distribution area of OH* radicals gradually expands to the downstream of flame. The distinctions of OH* distribution can be used to characterize the combustion condition. If OH* radicals only distribute over the upstream of the flame and appear discrete in shape, the flame is under the oxygen-deficient combustion. If OH* radicals distribution appears as a ring shape, the flame is under the oxygen-enriched combustion. Under the same oxygen flow rate, the size of annular channel has a significant impact on the mole fraction of OH*. Reducing the size of annular channel can enhance the mixture of fuel and oxygen as well as improve the radiation intensity of the OH* chemiluminescence, which makes the flame diagnosis more convenient.
火焰光谱辐射是火焰的重要特性之一, 主要包括三部分: CO2, H2O等三原子气体受热产生的带状光谱辐射(转动辐射)、 炭黑等悬浮固体颗粒产生的连续光谱辐射(黑体辐射)以及化学反应中激发态自由基的电子能级跃迁产生的离散光谱辐射(化学发光)[1, 2]。 其中, OH* , CH* 和
目前对火焰的自由基辐射特性已进行了大量的实验研究[3, 4, 5, 6], 但相关的数值研究还较少。 对火焰的自由基辐射进行数值模拟研究, 不仅有助于理解火焰中激发态自由基的生成和淬灭过程, 同时也便于研究不同操作条件下, 自由基辐射强度和分布特征的变化规律[7, 8]。 Leo等[9]对甲烷扩散火焰中OH* 和CH* 自由基的生成途径进行数值研究, 讨论了在不同条件下二者主要激发途径发生的变化。 Hossain等[10]采用三种不同的碳氢火焰详细反应机理, 结合CH* 自由基的生成和淬灭反应, 研究了对冲火焰中CH* 自由基对热释放率的表征能力。 Panoutsos等[11]对撞击火焰的自由基辐射进行研究, 比较了8种不同OH* 和CH* 自由基反应机理的准确性, 并在此基础上提出了一种新的反应机理, 能够更为准确地预测火焰中OH* 和CH* 自由基的分布。
然而, 以上有关火焰自由基辐射的数值模拟研究均采用一维火焰模型进行数值计算, 无法得到自由基在空间内的分布规律和特性, 存在着一定的局限性。 Walsh等[12]对火焰中的OH* 和CH* 自由基进行了初步的多维数值研究, 提出一种包含OH* 和CH* 自由基的反应机理, 并将其应用于甲烷层流扩散火焰的研究当中, 但由于他们误用了错误的OH* 生成速率常数, 导致最终的模拟结果远高于实验的测量值。 Luque等[13]对Walsh等[12]提出的反应机理进行改进, 得到了更为准确的模拟结果, 但该模型中仅考虑了基元反应CH* +O2=OH* +CO对OH* 生成的作用, 而忽略了基元反应H+O+M=OH* +M的影响。 Bozkurt等[14]提出了一种包含反应H+O+M=OH* +M的详细机理, 并对甲烷/氢气/氧气和乙炔/氧气预混火焰进行研究, 指出虽然碳氢火焰中的OH* 自由基主要通过反应CH+O2=OH* +CO生成, 但反应H+O+M=OH* +M仍有着不可忽视的促进作用。
本工作以甲烷/氧气层流同轴射流扩散火焰作为研究对象, 基于Bozkurt等[14]提出的OH* 自由基反应机理, 对火焰中OH* 自由基的二维分布特性进行研究, 从动力学角度对不同分布区域的OH* 自由基生成路径进行分析, 并探讨了不同氧燃当量比例和不同喷嘴出口尺寸对OH* 自由基强度和分布特性的影响。
为研究甲烷/氧气层流同轴射流扩散火焰的OH* 自由基辐射特性, 以实验室采用的同轴双通道喷嘴作为数值计算的对象。 由于层流火焰结构的对称性, 选取1/2截面构建计算域, 如图1(a)所示。 计算域的轴向和径向长度分别为100和25 mm, 其中包括一段长度为5 mm的喷嘴, 用于考虑燃料的预热效应并得到较为合理的喷嘴出口气速分布。 喷嘴出口结构如图1(b)所示, 喷嘴的中心通道为燃料通道, 内径D0=3 mm; 外通道为氧气通道, 为研究喷嘴出口尺寸对OH* 特性产生的影响, 采用两种不同的环隙结构进行计算, 分别设置为: (1) 环隙内径D1=4 mm, 外径D2=7 mm; (2)环隙内径D1=4 mm, 外径D2=5 mm。 喷嘴内外管道均简化为厚度为0.5 mm的简单几何形状。 假设喷嘴外部为同向流动的氩气, 以避免空气中的氧气和氮气对模拟结果产生影响。
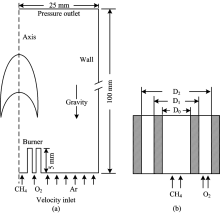 | 图1 计算域和喷嘴结构示意图 (a): 计算域和边界条件; (b): 喷嘴设置出口结构Fig.1 Schematization of the computational domain and burner structure (a): Computational domain and boundary conditions; (b): Burner structure |
气体进口的边界条件均设置为速度入口, 根据气体流量和喷嘴出口面积确定入口速度, 计算域的右边界设置为壁面边界条件, 而左边界设为对称轴, 上边界为压力出口边界条件, 操作压力为101 325 Pa。 为保证模拟的准确性, 所有网格均采用结构化网格, 网格总数约为5.2万, 最小网格尺寸为0.05 mm。
在研究甲烷流量为0.25 L· min-1时, 不同氧燃当量比例和不同喷嘴出口尺寸火焰的OH* 自由基分布特性, 具体工况如表1所示。 表中, v和u分别为气体的体积流量与入口气速, φ 为甲烷和氧气的氧燃当量比, 计算公式如式(1)所示:
其中, m为质量, n为物质的量, 下标st代表化学计量条件。
| 表1 数值计算条件 Table 1 Numerical simulation conditions |
1.3.1 气相流动和燃烧模型
层流有限速率(laminar finite-rate)模型使用Arrhenius公式计算化学反应源项, 并忽略湍流脉动的影响, 能够准确得到层流火焰中化学反应的结果。 研究的火焰工况均处于层流状态, 燃烧过程主要由燃料和氧化剂的化学反应控制, 因此采用层流模型作为流动模型, 层流有限速率模型作为燃烧模型对火焰的燃烧过程进行求解。
在层流有限速率模型中, 每个组分的输运方程为[15]
式(2)中, Yi为组分i的当地质量分数; v为速度; Ji为组分i由于浓度梯度产生的扩散通量; Si为源项; Ri为反应中组分i的净生成速率, 由NR个化学反应的Arrhenius反应源项之和计算得到[15]
式(3)中, Mw, i为组分i的分子质量;
反应r可由如下形式表示[15]
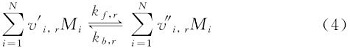
式(4)中, N为系统中化学组分的数目; v'i, r为反应r中反应物i的化学计量数; v″i, r为反应r中生成物i的化学计量数; Mi为组分i的化学式; kf, r为反应r的正反应速率常数; kb, r为反应r的逆反应速率常数。
反应r中组分i的产生/分解摩尔速度为[15]
式(5)中, Cj, r为反应r中每种反应物或生成物j的摩尔浓度; η 'j, r为反应r中每种反应物或生成物j的正向反应速度指数; η ″j, r为反应r中每种反应物或生成物j的逆向反应速度指数; Г 为第三体对反应速度的净影响, 缺省状态为不包括。
反应r的正向速率常数kf, r由Arrhenius公式计算[15]
式(6)中, Ar为指前因子, β r为温度指数, Er为反应活化能, R为气体常数。
反应r的逆向速率常数kb, r由式(7)计算[15]
其中, Kr为反应r的平衡常数。
1.3.2 详细化学反应机理
GRI-Mech3.0是气态烃氧化反应的详细反应机理, 其中包含53种基态组分和325个基元反应[16], 被广泛应用于自由基辐射的数值计算[7, 8, 9, 10]。 本研究采用的化学反应机理在GRI-Mech3.0的基础上对其进行简化, 删减其中除N2外的所有含氮物质和相关反应, 并补充OH* 自由基的生成和淬灭反应, 最终得到包含37种组分和227个基元反应的反应机理, 补充的反应动力学参数如表2所示。
| 表2 OH* 自由基化学反应动力学参数a Table 2 Kinetics parameters of OH* radicals reactiona |
1.3.3 辐射传热模型
在甲烷火焰中, 存在着CH4, CO, CO2和H2O等多原子及分子结构不对称的双原子气体组分, 这些气体具有较强的辐射和吸收能力, 会造成大量的辐射热损失, 因此在火焰模型中必须要考虑气体的辐射传热。 采用离散坐标(DO)辐射模型对火焰中的辐射传递过程求解, 并采用灰度系数加权平均模型(WSGGM)对气相介质的辐射吸收系数进行计算。
DO辐射模型从有限个立体角发出的辐射传递方程(RTE)出发求解, 每个立体角对应着坐标系下的固定方向
式(8)中,
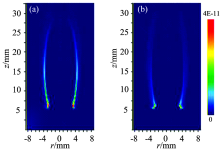
Walsh等[19]对甲烷/空气层流同轴射流扩散火焰进行研究, 指出火焰中OH* 自由基的辐射强度与其数密度呈正比关系。 他们采用高分辨率CCD相机结合中心波长为307nm的带通滤光片拍摄得到了火焰中的OH* 自由基辐射图像, 并利用瑞利散射进行标定后定量得到了火焰中OH* 摩尔分数的二维分布。 本工作利用其实验研究结果, 对计算模型的准确性进行验证, 详细的燃烧器尺寸参数和实验工况参见文献[19]。
图2为火焰中OH* 摩尔分数二维分布的模拟结果与实验结果对比, 图2(a)为本研究的模拟结果, 图2(b)为文献[19]中的实验结果。 由图2可知, 数值计算得到的模拟结果与实际火焰的测量结果具有基本一致的二维分布及变化趋势, 仅在火焰推举高度的计算上略有偏差。 这主要是由于GRI-Mech 3.0机理对熄火拉伸率的预测值较高, 因此当模拟对象为推举火焰时, 其火焰根部会更接近于喷嘴出口[20]。 而对于本文研究的层流火焰, 火焰始终附着在喷嘴出口处, 该偏差对模拟结果的影响较小, 可以认为本文的数值计算模型能够准确描述火焰中OH* 自由基的分布。
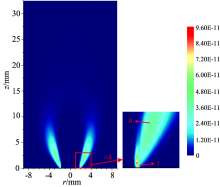
宋旭东等[21]对同轴射流扩散火焰进行研究后发现, 火焰中的OH* 自由基主要分布于甲烷和氧气之间, 标志着燃料和氧气接触并发生化学反应的火焰峰面位置。 图3为工况2时, 模拟得到的OH* 摩尔分数分布云图。 根据图中所示的OH* 摩尔分数分布, 可将其分布范围划分为两个主要反应区(Ⅰ 区和Ⅱ 区)。 在I区中, OH* 自由基靠近于甲烷一侧, 摩尔分数较高但分布区域较为狭窄, 主要位于喷嘴出口处; 在Ⅱ 区中, OH* 自由基则靠近于氧气一侧, 分布区域相对较宽且与基态OH自由基具有相同的二维分布。 为解释这种OH* 分布的形成原因, 需对火焰不同高度处的OH* 自由基浓度进行比较。 选取以下高度处的径向OH* 摩尔分数分布和主要反应的反应速率分布进行对比分析: (a) z=0.26 mm, (b) z=0.90 mm, (c) z=1.87 mm, (d) z=4.00 mm, 其中, 高度A为Ⅰ 区OH* 峰值的所在高度, 高度C为Ⅱ 区OH* 峰值的所在高度。 比较结果如图4所示, 图中OH* 生成反应的反应速率以正数表示, OH* 淬灭反应的反应速率以负数表示。
 | 图4 不同高度处的径向OH* 摩尔分数分布和反应速率分布Fig.4 The radial profiles of OH* mole fraction and chemical reactionrateat different height |
经分析后发现, Ⅰ 区和Ⅱ 区的OH* 自由基分别由两种不同的反应途径生成。 在Ⅰ 区内, 反应R2为生成OH* 自由基的主要途径, 而反应R1在此区域内几乎不会发生。 这是由于R2的反应物CH主要分布在I区, 离开喷嘴出口的氧气会首先与CH接触并迅速发生反应生成OH* 自由基, 因此I区的OH* 自由基主要集中于喷嘴出口处, 且具有较高的摩尔分数。 随着火焰不断向下游方向传播, CO和H2等中间物质在火焰中心轴线处生成, 氧气在参与反应后逐渐转变为游离氧, 导致R2的反应物不断减少, 而R1的反应物不断增加, 所以OH* 自由基的生成区域逐渐向游离氧较为丰富的Ⅱ 区移动。 在甲烷/氧气火焰中, 氧元素主要以游离氧的形式存在, 因此Ⅱ 区相比I区具有更大的OH* 分布区域。 上述结果也表明, 以氧气作为氧化剂有助于促进反应R1进行, 由此可认为反应R1是甲烷/氧气火焰中OH* 生成的主要路径。
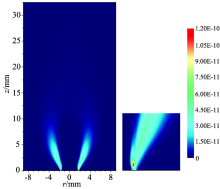
图5为氧燃当量比分别为0.7, 1.0, 1.3时, OH* 摩尔分数的分布云图。 图中, φ =0.7时, Ⅰ 区OH* 峰值摩尔分数为9.44× 10-11, Ⅱ 区OH* 峰值摩尔分数为2.82× 10-11; φ =1.0时, Ⅰ 区OH* 峰值摩尔分数为9.78× 10-11, Ⅱ 区OH* 峰值摩尔分数为3.95× 10-11; φ =1.3时, Ⅰ 区OH* 峰值摩尔分数为9.92× 10-11, Ⅱ 区OH* 峰值摩尔分数为4.57× 10-11。 随着氧燃当量比的增加, Ⅱ 区OH* 自由基的摩尔分数显著提高, 而Ⅰ 区OH* 自由基的摩尔分数变化不大。 这是因为喷嘴出口处的甲烷和氧气尚未完全扩散, 化学反应仅发生在甲烷和氧气间薄薄的一层接触面上, 受接触面积限制, 氧燃当量比增加对接触面上的氧气量影响较小, 因此Ⅰ 区OH* 自由基的摩尔分数不会产生明显变化。 而对于Ⅱ 区OH* 自由基, 氧气量的提高使火焰中的游离氧含量增加, 对反应R1起到促进作用, 有助于Ⅱ 区OH* 自由基的生成。
此外, 如图5所示, 不同氧燃当量比下Ⅱ 区OH* 分布呈现出不同的形态特征。 在贫氧条件(φ =0.7)下, 由于甲烷的不充分燃烧会产生大量的CO和H2, 火焰下游的游离氧会首先与之发生反应而被完全消耗, 进而抑制OH* 自由基的生成, 因此在低氧燃当量比火焰中, Ⅱ 区OH* 自由基仅分布于火焰的上游区域。 当φ =1.0时, 火焰下游区域的Ⅱ 区OH* 自由基逐渐向火焰中心轴线扩张, 说明在该区域内, 随着氧气量的增加, 甲烷燃烧更加充分, CO和H2等中间物质不断减少, 仅有少量存在于火焰的中心轴线处。 当氧气量提高到富氧条件(φ =1.3)时, 火焰下游的CO和H2已被完全转化为CO2和H2O, 过剩的游离氧和游离氢发生三体碰撞反应R1, 从而使OH* 自由基能够在火焰的中心轴线处生成, 形成环状的Ⅱ 区OH* 分布。 根据火焰中Ⅱ 区OH* 分布形态的变化可以对火焰的燃烧状况进行判断, 如果OH* 自由基仅分布于火焰的上游区域且呈断开形态, 则说明火焰处于贫氧燃烧状态; 如果OH* 分布呈环状形态, 则说明火焰处于富氧燃烧状态。
图6为缩小喷嘴出口的环隙尺寸后, 工况4时OH* 摩尔分数的分布云图。 图中, Ⅰ 区OH* 峰值摩尔分数为1.24× 10-10, Ⅱ 区OH* 峰值摩尔分数为4.48× 10-11。 比较图5和图6可知, 缩小环隙尺寸后, OH* 自由基的分布特征没有产生明显变化, 但Ⅰ 区和Ⅱ 区OH* 自由基的摩尔分数均显著提高, 其中Ⅰ 区OH* 摩尔分数的增长幅度远大于Ⅱ 区。 对于同轴射流火焰而言, 环隙气体由喷嘴射出后, 会形成沿径向扩散的流场, 使环隙氧气与中心通道甲烷混合并发生反应。 缩小环隙尺寸后, 出口气速的大幅度增加引起氧气径向扩散的增强, 使喷嘴出口处燃料与氧气的混合程度提高, 二者的化学反应更加剧烈, 从而促进Ⅰ 区OH* 自由基的生成。 随着火焰向下游方向传播, 燃料和氧气已经能够充分混合, 氧气的径向扩散对二者化学反应程度的影响逐渐减弱, 但由于喷嘴出口处化学反应程度的加强导致火焰中游离氧和游离氢的浓度提高, 促进了反应R1的进行, 因此Ⅱ 区OH* 自由基的摩尔分数也发生了小幅度的提高。 OH* 摩尔分数的提高可以增强其化学发光的辐射强度, 进而使OH* 自由基辐射的检测更为方便和准确, 便于火焰的光谱诊断。
以甲烷/氧气层流同轴射流扩散火焰作为研究对象, 采用基于GRI-Mech 3.0的简化机理结合OH* 自由基生成和淬灭反应进行数值计算, 对OH* 自由基的二维分布特性进行研究。 模拟结果与实验研究基本吻合, 表明计算模型能够准确描述火焰中OH* 自由基的二维分布。 结果表明:
(1) 在甲烷/氧气层流同轴射流扩散火焰中, OH* 自由基存在两种不同形态的分布区域(Ⅰ 区和Ⅱ 区), 分别由反应CH+O2=OH* +CO(R2)和H+O+M=OH* +M(R1)生成。 其中, Ⅱ 区OH* 分布区域较宽且与基态OH自由基具有相同的二维分布, 便于在火焰诊断过程中对其进行观察, 可用于对火焰结构的表征。 以氧气作为氧化剂有助于促进反应H+O+M=OH* +M(R1)进行, 由此可认为反应H+O+M=OH* +M(R1)是甲烷/氧气火焰中OH* 生成的主要路径。
(2) 随着氧燃当量比的增加, Ⅰ 区OH* 自由基的摩尔分数变化不大, Ⅱ 区OH* 自由基的摩尔分数显著提高, 且其分布区域逐渐向火焰下游及中心轴线扩张, 说明火焰中氧气含量的变化对Ⅱ 区内OH* 的生成具有显著影响。 根据火焰中Ⅱ 区OH* 分布形态的变化可以对火焰的燃烧状况进行判断。 如果OH* 自由基仅分布于火焰的上游区域且呈断开形态, 则说明火焰处于贫氧燃烧状态; 如果OH* 分布呈环状形态, 则说明火焰处于富氧燃烧状态。
(3) 相同氧气流量条件下, 缩小喷嘴出口的环隙尺寸有助于加强燃料和氧气的混合程度, 促进化学反应进行, 从而使火焰中OH* 自由基的摩尔分数显著提高, 增强OH* 化学发光的辐射强度, 提高火焰光谱诊断的准确性。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|