作者简介: 司民真, 女, 1962年生, 楚雄师范学院教授 e-mail: siminzhen@cxtc.edu.cn
常温下, 将制备好的长柄山姜及茴香砂仁的水装片放在显微拉曼光谱仪的载物台上, 寻找油细胞, 并分析其中精油。 长柄山姜油细胞上获得的拉曼光谱, 较强峰出现在1 638, 1 600, 1 555, 1 203和1 001 cm-1, 次强峰出现在1 716, 1 577, 1 496, 1 407, 1 346, 1 307, 1 273, 1 181, 1 156, 1 029, 958, 618和218 cm-1共获得26条光谱线, 与肉桂酸甲酯拉曼光谱的29条谱线比较, 长柄山姜油细胞有22条谱线与之有对应关系; 茴香砂仁油细胞上获得的拉曼光谱较强峰出现在1 648, 1 639, 1 607, 1 174, 842和836 cm-1, 次强峰出现在1 292, 1 244, 1 235, 1 204和631 cm-1共获得24条光谱线, 与4-烯丙基苯甲醚的拉曼光谱在300~1 700 cm-1区间内的29条谱线比较, 茴香砂仁油细胞有23条谱峰与之有对应关系。 说明长柄山姜挥发油的主要成分是肉桂酸甲酯, 茴香砂仁挥发油的主要成分为4-烯丙基苯甲醚。 用密度泛函理论计算了肉桂酸甲酯、 4-烯丙基苯甲醚的拉曼光谱, 并对谱线进行了初步的归属。 姜科植物油细胞中精油不需提取就可直接快速的检测, 用此方法可对姜科植物精油的提取进行质量控制及开发研究。
Non-destructive analysis of the essential oils ingredient in oil cells at room temperature was presented. This work showed the possibility to detect in situ the main components of the essential oils in Alpinia kwangsiensis and Achasma yunnanensis oil cells by means of Raman spectroscopy. Water slice of fresh samples were prepared. The oil cells in water slice can be seen using 20 objective lens of DXR Laser confocal micro Raman spectrometer. At the Alpinia kwangsiensis oil cell, high intensity bands were present in 1 638, 1 600, 1 555, 1 203, 1 001 cm-1, and low intensity bands were present in 1 716, 1 577, 1 496, 1 407, 1 346, 1 307, 1 273, 1 181, 1 156, 1 029, 958, 618, 218 cm-1. Together 26 spectroscopic bands were obtained. The Raman spectrum of the Methyl cinnamate, together 29 spectroscopic bands, were obtained. It was found that the 22 presented spectroscopic bands of Alpinia kwangsiensis oil cell correlated very well with those obtained by the Methyl cinnamate; At the Achasma yunnanensis oil cell, high intensity bands were present in 1 648, 1 639, 1 607, 1 174, 842, 836 cm-1, and low intensity bands were present in 1 292, 1 244, 1 235, 1 204, 631 cm-1. Together 24 spectroscopic bands were obtained. The Raman spectrum of the 4-Allyl anisole, together with 29 spectroscopic bands(between 300~1 700 cm-1) was obtained. It was found that the 23 presented spectroscopic bands of Achasma yunnanensis oil cell correlated very well with those obtained by the 4-Allyl anisole. The experimental work was supported by quantum chemical calculations at the B3LYP/6-311G level of theory. The essential oils ingredient in oil cells of Zingiberaceae samples can be detected directly and quickly without extraction. This method can be use to quality control and development research for zingiberaceae plant essential oil extraction.
引 言
长柄山姜(Alpinia kwangsiensis T.L.Wu et Senjen)及茴香砂仁(Achasma yunnanense T.L.Wu et Senjen)都属于姜科植物, 长柄山姜、 茴香砂仁各属山姜属及茴香砂仁属植物。 都是植物药。 长柄山姜根茎可治脘腹冷痛、 胃寒呕吐[1]。 茴香砂仁是西双版纳的一种土著植物, 也是傣药品种之一(傣药名麻娘布)以根茎入药治疗小便热涩疼痛, 胃脘胀痛, 恶心呕吐, 不思饮食, 腹泻, 中暑[2]。 纳智利用GC-MS联用技术从长柄山姜挥发油中已鉴定出的31个成分含量, 占挥发油总量的99.59%, 主要成分是肉桂酸酯类、 单萜烯、 倍半萜烯及其含氧衍生物, 其中肉桂酸甲酯占挥发油总量的94.54%; 13个单萜成分占挥发油总量的3.00%, 其中含量最高的是芳樟醇(0.91%)[3]。 目前还未见对茴香砂仁挥发油的研究。 通常用GC-MS联用技术分离鉴定挥发油中的化学组成, 该方法所需要的前期样品的制备时间较长, 费用高, 其流程为气相色谱柱分离-质谱仪定性或定量, 气相色谱分离需要在较高的温度下进行, 可能会引起生物活性分子的结构改变。 本课题组提出了一种不通过繁杂提取且在常温下就能进行的挥发油主要挥发性物质检测方法-样品油细胞原位显微拉曼光谱检测方法, 并对姜科植物姜进行了研究, 得到姜的主要挥发物为姜烯[4]。 本工作利用该方法对姜科山姜属植物-长柄山姜, 姜科茴香砂仁属植物-茴香砂仁的精油主要成分进行研究。
长柄山姜及茴香砂仁于2015年8月采摘于西双版纳并经过专家鉴定, 采用徒手切片制样后用水装片待用。 分析纯的肉桂酸甲酯及4-烯丙基苯甲醚购于百灵威科技。 测量仪器使用美国Thermo Fisher公司的DXR 激光共焦显微拉曼光谱仪, 所用的激发波长为785 nm, 测定功率为2 mW, 曝光时间为30 s, 样品连续曝光3次。 显微镜物镜倍数为20× 。
对两个标样肉桂酸甲酯及4-烯丙基苯甲醚用Gaussian’ 03 程序进行理论计算, 并用RB3LYP方法(交换函数为Becke3, 相关函数为LYP)在6-311G 基组水平上, 对其几何结构进行优化, 在优化的基础上计算了振动频率, 肉桂酸甲酯的计算波数在2 880~3 364 cm-1之间乘以校准因子0.9572。 4-烯丙基苯甲醚的计算波数乘以校准因子0.972 7。
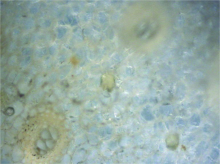
将制备好的水装片放置在显微镜的载物台上, 仔细调焦后可见长柄山姜细胞结构, 在此基础上寻找油细胞, 并将激光聚焦于油细胞见图1。 图2a是对应的油细胞的拉曼光谱。
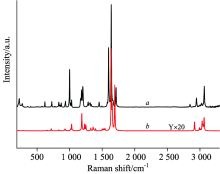
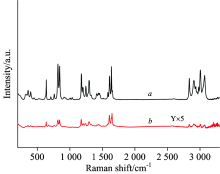
 | 图2 长柄山姜(a)及肉桂酸甲酯(b)的拉曼光谱图Fig.2 Raman spectrum of Alpinia kwangsiensis oil cell (a) and Methyl cinnamate solid (b) |
图2(b)是标样肉桂酸甲酯的拉曼光谱图, 从图2可见, 长柄山姜及肉桂酸甲酯的拉曼光谱图从峰的形状、 峰位、 峰的相对高度来看都非常相似。 为了便于比较两者之间的异同, 表1列出了他们的拉曼峰的波数。
根据图2及表1, 长柄山姜油细胞中油的拉曼峰, 较强峰出现在1 638, 1 600, 1 555, 1 203和1 001 cm-1, 次强峰出现在1 716, 1 577, 1 496, 1 407, 1 346, 1 307, 1 273, 1 181, 1 156, 1 029, 958, 618和218 cm-1。 肉桂酸甲酯的较强峰出现在1 712, 1 638, 1 597, 1 202和1 000 cm-1, 次强峰出现在1 452, 1 284, 1 182, 1 169, 1 029, 619和226 cm-1, 在油细胞中出现的强峰、 次强峰大部分与肉桂酸甲酯的拉曼峰一致, 说明长柄山姜油细胞中油的主要成分为肉桂酸甲酯。 此外还有一些较弱的峰, 这些峰在油细胞中没有出现, 可能的原因是油细胞的量太少未能检出。 同时, 长柄山姜油细胞中油的一些拉曼峰在肉桂酸甲酯中无相应的峰与之对应, 如2 952, 1 555, 1 346和958 cm-1说明长柄山姜油细胞中油的主要成分为肉桂酸甲酯外, 还有其他的成分。 肉桂酸甲酯的拉曼峰共29条, 油细胞的拉曼峰共26条, 这26条中有22条与肉桂酸甲酯的拉曼峰对应, 对应率为75.86%。
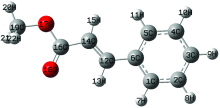
计算了肉桂酸甲酯的拉曼光谱其振动归属列于表1中, 图3给出相应的分子优化结构。 图4是肉桂酸甲酯的计算拉曼光谱和实验的光谱两者非常相似。
| 表1 肉桂酸甲酯及长柄山姜拉曼谱的初步归属 Table 1 Raman spectral assignments of Methyl cinnamate and Alpinia kwangsiensis |
根据计算的拉曼光谱将肉桂酸甲酯、 长柄山姜油细胞的拉曼谱进行初步的归属, 见表1。 3 067(3 063), 3 023(3 031), 3 007和2 990 cm-1归属为C— H伸缩振动; 1 496, 1 452(1 449), 1 408(1 407), 1 182(1 181)和871 cm-1归属为C— H摇摆振动; 1 712(1 716), 1 638(1 638) cm-1归属为C=C及C=O伸缩振动; 1 169(1 156) cm-1归属为C— H2剪切振动; 1 015 cm-1归属为C— O及C— C伸缩振动; 935(936) cm-1归属为C— O伸缩振动及C— C— C的弯曲振动; 1 029(1 029), 834和575(588) cm-1归属为环呼吸振动; 725 cm-1归属为环的伞型振动; 1 022(1 023) cm-1归属为C— H2摇摆振动; 1 597(1 600), 1 331, 1 000(1 001)和507(507)cm-1归属为环的变形振动; 226(218) cm-1归属为骨架振动。
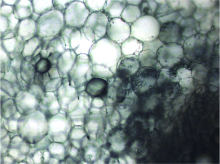
图5是显微镜下茴香砂仁油细胞, 图6b是相应的拉曼光谱。
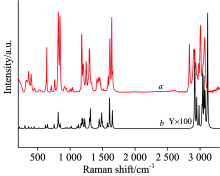
图6a是标样4-烯丙基苯甲醚的拉曼光谱图, 从图6可见, 4-烯丙基苯甲醚和茴香砂仁拉曼峰的形状、 峰位、 峰的相对高度都非常相似。 为比较两者之间的异同, 表2中给出各自的波数。
 | 图6 4-烯丙基苯甲醚(a)及茴香砂仁(b)的拉曼光谱Fig.6 Raman spectrum of 4-Allyl anisole liquid (a) and oil cell of Achasma yunnanense T.L.Wu et Senjen (b) |
根据图6及表2, 茴香砂仁油细胞中油的拉曼峰, 较强峰出现在1 648, 1 639, 1 607, 1 174, 842和836 cm-1, 次强峰出现在1 292, 1 244, 1 235, 1 204和631 cm-1。 4-烯丙基苯甲醚的较强峰出现在1 639, 1 611, 1 259, 1 177, 1 039, 844, 817和638 cm-1, 次强峰出现在1 653, 1 585, 1 455, 1 441, 1 413, 1 246, 1 198, 398和359 cm-1, 在茴香砂仁油细胞中出现的强峰、 次强峰大部分与4-烯丙基苯甲醚的拉曼峰一致, 说明茴香砂仁油细胞中油的主要成分为4-烯丙基苯甲醚。 此外还有一些峰如: 1 325, 1 111, 1 039, 1 013, 996和938 cm-1, 这些峰在油细胞中没有出现, 可能的原因是油细胞的量太少未能检出。 同时, 茴香砂仁油细胞中油拉曼峰1 235 cm-1在4-烯丙基苯甲醚中无相应的峰与之对应, 说明茴香砂仁油细胞中油的主要成分为4-烯丙基苯甲醚外, 还有其他的成分。 4-烯丙基苯甲醚的拉曼峰在300~1 700 cm-1区间内共29条, 油细胞的拉曼峰共24条, 这24条中有23条与4-烯丙基苯甲醚的拉曼峰对应, 对应率为79.3%。
| 表2 4-烯丙基苯甲醚及茴香砂仁拉曼谱的初步归属 Table 2 Spectral assignments of 4-Allylanisole and Achasma yunnanense T.L.Wu et Senjen |
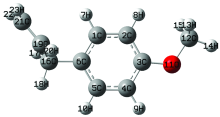
计算了4-烯丙基苯甲醚的拉曼光谱并将其振动归属列于表2中, 图7是相应的分子优化结构。 图8是计算的4-烯丙基苯甲醚的拉曼光谱和实验的光谱, 从图中可见两者非常相似。 由此, 在表2中将4-烯丙基苯甲醚、 茴香砂仁油细胞的拉曼光谱作了初步的归属。
 | 图8 4-烯丙基苯甲醚的实验(a) 及计算(b)的拉曼光谱Fig.8 Raman spectrum of 4-Allylanisole liquid (a) and calculated Raman spectrum (b) |
1 653(1 648) cm-1归属为C=C伸缩振动及C— H2剪切振动, 1 411 cm-1归属为C=C伸缩振动及C— H摇摆振动; 1 611(1 607), 1 585(1 584), 1 295(1 292), 1 013, 844(842), 708(709)和638(637) cm-1归属为环的变形振动; 996 cm-1归属为C— O伸缩振动; 1 512(1 512), 1 455(1 453) cm-1归属为C— H3的伞型振动; 1 441(1 440) cm-1归属为C— H2剪切振动; 1 198(1 204)和938 cm-1 归属为C— C伸缩振动; 1 177(1 174)和1 111 cm-1归属为C— H摇摆振动; 817和816 cm-1归属为环呼吸振动; 761(759), 450(444)和359(357)cm-1归属为骨架振动; 524(523) cm-1归属为C— H2扭曲振动。
不需要复杂的提取植物精油的过程, 只需将拉曼光谱仪的激光聚焦在用水装片的植物的油细胞上, 即可获得植物油细胞的拉曼光谱。 长柄山姜油细胞的拉曼光谱与与肉桂酸甲酯的拉曼光谱相似, 其对应率为75.86%; 茴香砂仁油细胞的拉曼光谱与4-烯丙基苯甲醚的拉曼光谱相似, 其对应率为79.31%。 该方法由于在常温常压下检测, 可避免精油活性成分的变化, 值得做进一步的深入研究。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|