作者简介: 龚爱琴, 女, 1974年生, 扬州工业职业技术学院副教授 e-mail: 578288049@qq.com
琥珀酸曲格列汀(QGLT)是一种新型降糖药, 基于其能够猝灭牛血清白蛋白(BSA)的荧光, 用荧光法研究了两者的相互作用。 对影响荧光猝灭的因素如溶液酸度、 介质性质等进行了优化。 猝灭机理探讨发现QGLT主要通过静态猝灭降低BSA的荧光, 并推导出两者的结合位点数为 n=1, 结合常数分别为4.529×104 L·mol-1(298k)和2.958×104 L·mol-1(303 k)。 热力学参数测定结果显示吉布斯自由能变、 焓变和熵变均为负值, 表明QGLT和BSA的结合主要是通过氢键与范德华力自发结合的。 研究中发现Lineweaver-Burk方程具有良好的线性关系, 线性方程为: ( F0- F)-1=2.711×10-4+3.51×10-3 cQGLT-1( cQGLT: μg·mL-1), r=0.998 9, 检出限为0.13 μg·mL-1(S/N=3), 线性范围为0.5~10.0 μg·mL-1。 回收率实验结果表明方法的准确性较好(回收率为94.0%~97.5%)。 用该方程测定了药片和人血清中QGLT含量, 结果令人满意。 本研究拓展了QGLT含量测定的新方法。
In this paper the interaction between trelagliptin succinate (QGLT) and bovine serum albumin (BSA) was studied by fluorescence spectrometry. The factors affecting fluorescence quenching such as solution acidity and medium characteristics were optimized. The examination results of quenching mechanism showed that the fluorescence intensity of BSA was quenched strongly by QGLT mainly through a static quenching procedure, the number of binding sites was 1, and the biding constants was 4.529×104L·mol-1 (298 k) or 2.958×104 L·mol-1 (303 k), respectively. The determination results of thermodynamic parameters show that the change of Gibbs free energy, enthalpy or entropy was negative, which clarified there was an automatic reaction happened between QGLT and BSA, and both hydrogen bonds and van der Waals force played a role in the binding of QGLT to BSA. It was also found in the examination that Lineweaver-Burk equation [( F0- F)-1=2.711×10-4+3.51×10-3
琥珀酸曲格列汀(trelagliptinsuccinate)是一种长效二肽基肽酶IV(DPP-4)抑制剂, 由日本武田公司(Takeda)研发, 用于治疗2型糖尿病, 于2015年3月在日本上市, 每周只需要服用一次, 其结构式如图1[1, 2]。
药物在体内的运输一般是由血清白蛋白承担的, 研究其与血清白蛋白的作用对了解药物在体内的分布、 阐明药物的作用机制、 药代动力学和药物的毒性都有重要意义[3, 4, 5, 6]。 目前还没有文献报道血清与琥珀酸曲格列汀的相互作用, 本研究采用荧光分析法探讨了QGLT与BSA的相互作用, 通过荧光数据计算了两者的结合常数K、 结合位点数n、 热力学参数(熵变、 焓变、 吉布斯自由能)。 实验发现BSA的荧光强度与琥珀酸曲格列汀的浓度在0.5~10.0 μ g· mL-1范围内有良好的关系, 由此提出了测定QGLT含量的新方法。 目前报道的测定QGLT含量的分析方法很少, 文献[1, 4]提出用HPLC法测定鼠血清和药片中QGLT含量, 其他方法尚未见报道。 本方法的提出拓展了QGLT含量测定方法, 运用本方法测定了琥珀酸曲格列汀药片和人血清中QGLT含量, 结果令人满意。
F-4500荧光仪(日本Hitachi), pH S-25酸度计(上海精科雷磁)。
1.00 mg· mL-1琥珀酸曲格列汀(QGLT)标准溶液(江苏万川医疗健康产业集团有限公司提供的标准物质), 以高纯水为溶剂。
2.00 mg· mL-1牛血清白蛋白标准溶液(BSA)(国药集团化学试剂有限公司), 以高纯水为溶剂。
pH值为7.4缓冲溶液: 称取3.4 g KH2PO4, 用适量水溶解, 再加入0.78 g NaOH, 用水溶解稀释至500 mL, 于酸度计上调节pH值为7.4。
琥珀酸曲格列汀片(江苏万川医疗健康产业集团有限公司提供): 规格: 100 mg· 片-1, 批号: 20160701。
1.2.1 试样处理
QGLT药片: 取5片QGLT, 研成粉末后称取相当于一片重量的药品粉末, 用高纯水溶解定溶至100.0 mL, 过滤, 取续滤液供分析用。
人血清: 取健康自愿者的血清, 稀释10倍后测试。
1.2.2 荧光测定
于10 mL离心试管中, 分别加入0.20 mL 2.00 mg· mL-1 BSA溶液、 2.0 mL pH值为7.4缓冲溶液、 一定量适量的QGLT样品或标准溶液, 用高纯水稀释至10.0 mL, 固定狭缝宽度为5.0 nm, 在激发波长280 nm时扫描所配制溶液的荧光发射峰, 测定荧光发射峰的强度。
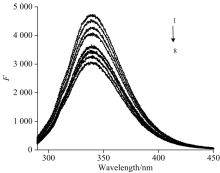
BSA在280 nm激发时荧光发射峰位于340 nm附近, 而QGLT在340 nm无荧光。 图2为不同浓度QGLT存在时BSA的荧光谱图, 随着QGLT浓度增加BSA的荧光峰强度F逐渐降低, 据此可知QGLT对BSA的荧光强度产生了猝灭作用, 猝灭的原因可能是两者发生了相互作用。
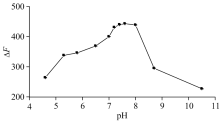
由图3可知荧光猝灭值Δ F(加与不加QGLT时BSA荧光峰强度差值)开始随pH值增大而增大, 在pH值为7.0~8.0范围内Δ F达到最大并基本保持不变, 之后随pH值增大Δ F下降, 故在以下实验中选用生理pH值(pH 7.4)作进一步研究。
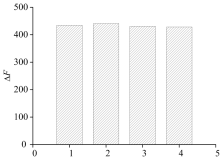
固定BSA、 QGLT浓度, 试验了pH值为7.4的NH3-NH4Cl、 柠檬酸-Na2HPO4、 KH2PO4-NaOH、 Tris-HCl缓冲体系对Δ F的影响, 结果显示介质对Δ F(加与不加QGLT时BSA荧光强度差值)无明显影响。 实验中选用KH2PO4-NaOH(人体中的缓冲体系)。
对缓冲溶液用量的影响进行了研究, 发现当溶液总体积为10.0 mL时, 其用量超过1.0 mL Δ F基本保持不变, 实验中选用缓冲溶液用量为2.0 mL。
2.4.1 荧光猝灭类型
一般荧光猝灭可分为动态和静态两种类型, 通过方程
其中F0和F: 加入猝灭剂前后体系的荧光强度; Ksv: 动态猝灭常数; Kq: 动态猝灭速率常数, 一般都小于2.0× 1010 L· (mol· s)-1; τ 0: 猝灭剂不存在时荧光分子平均寿命, 生物大分子τ 0约为10-8 s; cQ: 猝灭剂浓度; KLB: 静态猝灭结合常数。
如果荧光猝灭主要是通过单一动态猝灭进行, 在一定浓度范围内,
图5和表1为不同温度下BSA与QGLT作用的S— V曲线和L— B曲线及线性方程和相关系数。 根据表1计算出的Kq≈ 1012(> 1010)且L— B方程线性关系略优于S— V方程, 表明QGLT主要通过静态猝灭方式降低BSA的荧光强度[8, 9]。
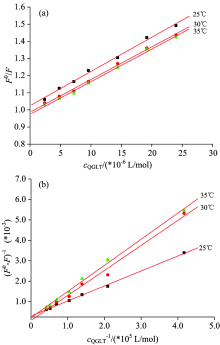 | 图5 不同温度时S— V(a) 与L-B(b) 曲线(cBSA: 40.0 μ g· mL-1)Fig.5 The S— V(a) and L— B(b) curves at different temperatures (cBSA: 40.0 μ g· mL-1) |
| 表1 不同温度时S— V和L— B曲线线性方程 Table 1 Linear equation of S— V and L— B curve at different temperatures |
由Ksv也可判断猝灭类型。 一般对于静态猝灭来说Ksv随温度升高而降低, 动态猝灭时正好相反[9, 10]。 不同温度下测得QGLT与BSA作用的Ksv(L· mol-1)为: 1.977× 104(25 ℃), 1.910× 104(30 ℃), 1.889× 104(35 ℃)。 随着温度升高Ksv降低, 进一步说明QGLT可能与BSA结合发生了静态猝灭。
2.4.2 结合常数与结合位点数
根据文献[11], 荧光强度F与猝灭剂浓度cQ满足下列关系
K与n即为反应的结合常数与结合位点数。 BSA与QGLT在不同温度时结合反应的K和n如表2所示。 n接近1, 表明BSA中可能有一个位点与QGLT结合, 而K随温度升高而降低, 表示BSA与QGLT形成的结合物稳定性可能随着温度升高而降低。
| 表2 结合常数与热力学参数 Table 2 The binding reaction constant and thermodynamic parameters |
2.4.3 热力学参数与作用过程
当温度变化不大时, 反应的焓变可认为是一常数, 根据
2.5.1 工作曲线与检出限
因为室温下Lineweaver-Burk曲线的线性关系更好, 实验中用该曲线测定QGLT含量。 曲线回归方程为: (F0-
F)-1 = 2.711× 10-4+3.51× 10-3
2.5.2 回收率实验及样品测定
取QGLT药片溶液, 用高纯水稀释100倍后, 取2.00 mL溶液用所研究方法测定, 结果见表3。 将测定结果换算为每片含量为99.0 mg, 标示量为100 mg· 片-1, 两者无显著性差异。 取10 mL离心管18支, 分别加入2.0 mL经稀释100倍后且已测定出含量的QGLT药片溶液及处理后的空白人血清溶液各9份, 然后加入QGLT标准溶液, 使其浓度分别为2.0, 4.0, 6.0 μ g· mL-1, 每个浓度平行配制3份, 用所研究方法测定, 结果见表3, 回收率为94.0%~97.5%, 可见, 本法测定结果可靠, 且操作快速简便, 可用来测定药片及血清中琥珀酸曲格列汀含量。
| 表3 回收率及样品测定结果(n=3) Table 3 Recoveries and sample determination results (n=3) |
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|